
- •Глава 1. Загальні положення. Класифікація гравіметричних методів
- •Метод виділення
- •Метод відгонки
- •Методи осадження
- •Вимоги до осадженої форми
- •Вимоги до гравіметричної форми
- •Вимоги до осаджувача
- •Умови осадження кристалічних осадів
- •Умови осадження аморфних осадів
- •Послідовність аналітичних операцій в гравіметричному методі осадження
- •Практична робота розрахунок величини наважки в гравіметричному аналізі
- •Приклади розв'язування задач
- •Задачі для самостійної роботи
- •Практична робота розрахунок кількості осаджувача
- •Приклад розв'язування задач
- •Задачі до самостійної роботи
- •Практична робота розрахунок результатів аналізу в гравіметрії
- •Приклади розв'язування задач
- •Задачі до самостійної роботи
- •Лабораторна робота визначення масової частки кристалізаційної води в кристалогідраті
- •План експерименту:
- •Лабораторна робота визначення масової частки сульфат-іонів у магній сульфаті гравіметричним методом осадження
- •План експерименту:
- •Лабораторна робота визначення масової частки феруму в кристалогідраті ферум(іі) сульфату
- •План експерименту:
- •Контрольні питання:
- •Глава 2. Основні положення титриметричного аналізу
- •Вимоги до реакцій у титриметричному аналізі
- •Класифікація методів титриметрії в залежності від типу реакції
- •Класифікація методів титриметрії за способом титрування
- •Способи приготування стандартних розчинів
- •1. Приготування первинних стандартних розчинів
- •2. Приготування вторинних стандартних розчинів
- •3. Приготування стандартних розчинів із фіксаналів
- •Глава 3. Розрахунки в титриметричному аналізі
- •3.1. Способи виразу вмісту речовин у розчинах
- •3.2. Розрахункові формули титриметрії
- •Глава 4. Метод кислотно–основного титрування
- •4.1. Теоретичні основи методу
- •Індикатори методу кислотно-основного титрування
- •Показник індикаторів рК, показник титрування рН
- •Класифікація індикаторів
- •Криві титрування
- •1. Титрування сильних кислот сильними основами (Рис 1.)
- •2.Титрування слабких основ сильними кислотами. (Рис 2.)
- •3. Титрування слабких кислот сильними основами. (Рис 3.)
- •4. Титрування слабких кислот слабкими основами.
- •5. Титрування багатоосновних кислот (Рис 4.)
- •Кислотно-основне титрування в неводних середовищах
- •Робочі розчини у методах неводного титрування
- •Практичне використання методів кислотно-основного титрування в аналізі фармацевтичних препаратів
- •Практична робота способи виразу вмісту речовин у розчинах
- •Приклади розв’язання задач
- •Задачі для самостійної роботи
- •Рішення:
- •І Метод окремих наважок
- •Використаний прийом – метод окремих наважок.
- •Розв’язання задачі
- •Задачі для аудиторної роботи
- •Індивідуальні завдання для самостійної роботи студентів з теми «Метод кислотно-основного титрування»
- •Лабораторна робота калібрування мірного посуду. Визначення вмісту піпетки
- •План експерименту
- •Розрахунок маси наважки натрій гідроксиду
- •Взяття наважки лугу
- •Приготування розчину лугу
- •Приготування робочого розчину лугу
- •Висновок лабораторна робота аналіз мінеральної кислоти
- •Хімізм процесу
- •План експерименту
- •Зважувати концентровані кислоти треба в скляному бюксі із закритою кришкою і дуже обережно!!!
- •Лабораторна робота приготування і стандартизація розчину хлоридної кислоти
- •Хімізм процесу
- •План експерименту
- •II. Приготування розчину первинного стандарту натрій тетраборату
- •III. Стандартизація розчину хлоридної кислоти
- •IV. Висновок.
- •Визначення масової частки натрій карбонату у препараті проводять за II-ю точкою еквівалентності План експерименту
- •Лабораторна робота визначення вмісту аніліну в досліджуваному зразку
- •Хімізм процесу
- •План експерименту
- •Глава 5. Методи окисно-відновного титрування
- •5.1. Теоретичні основи методу
- •Окисно-відновні індикатори
- •5.2. Перманганатометрія
- •Приготування розчину kMnO4
- •Стандартизація розчину kMnO4
- •Задачі для самостійної роботи
- •Лабораторна робота приготування та стандартизація розчину калій перманганату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок.
- •Лабораторна робота
- •Визначення вмісту гідроген пероксиду
- •В лікарському препараті
- •Хімізм процесу
- •План експерименту
- •Лабораторна робота
- •Гептагідраті методом перманганатометрії
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •5.3. Хроматометрія
- •Лабораторна робота аналіз солі Fе(II) методом хроматометрії
- •Хімізм процесу
- •План експерименту
- •5.4. Цериметрія
- •5.5. Йодометрія
- •Приготування розчину Na2s2o3
- •Приготування розчину і2
- •Використання методу
- •Лабораторна робота приготування та стандартизація робочого розчину натрій тіосульфату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок. Лабораторна робота приготування та стандартизація розчину йоду
- •Хімізм процесу
- •План експерименту
- •IV. Висновок
- •План експерименту
- •V. Висновок.
- •План експерименту
- •Лабораторна робота аналіз аскорбінової кислоти методом йодометрії
- •Аскорбінова кислота
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.6. Броматометрія
- •Лабораторна робота визначення вмісту стрептоциду в препараті методом броматометрії
- •Хімізм процесу
- •Принцип методу заміщення
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.7. Нітритометрія
- •Умови проведення реакції діазотування
- •Визначення точки еквівалентності
- •Лабораторна робота приготування та стандартизація робочого розчину натрій нітриту
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання до самостійної роботи
- •Глава 7. Методи осаджувального титрування
- •7.1. Теоретичні основи методу
- •Класифікація методів осадження
- •Вимоги до реакцій, що використовуються в методах осадження
- •Індикатори методів осадження
- •5.2. Аргентометрія
- •Метод Мора
- •Умови титрування за методом Фаянса–Ходакова
- •6.3. Тіоціанатометрія Метод Фольгарда
- •Умови титрування за методом Фольгарда
- •6.4. Меркурометрія
- •Приготування та стандартизація розчину титранту
- •Переваги та недоліки меркурометрії перед іншими методами осадження
- •Завдання для самостійної роботи
- •План експерименту
- •Лабораторна робота визначення масової частки калій йодиду методом фольгарда
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 7. Методи комплексоутворення
- •7.1. Теоретичні основи методу
- •7.2. Комплексонометрія (трилонометрія)
- •Принцип дії металохромних індикаторів
- •7.3. Меркуриметрія
- •Задачі для самостійної роботи
- •Лабораторна робота приготування і стандартизація розчину комплексону ііі (трилону б, едта)
- •Хімізм процесу
- •План експерименту
- •III. Стандартизація титранту комплексону ііі.
- •Висновок.
- •Лабораторна робота
- •Аналіз кальцій хлориду гексагідрату
- •Комплексонометричним методом
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 8. Оптичні методи аналізу
- •8.1. Абсорбційні методи аналізу
- •8.1.1. Теоретичні основи
- •Основний закон світлопоглинання (закон Бугера - Ламберта-Бера)
- •Апаратура молекулярно-абсорбційних методів
- •Характеристика та функціональне призначення основних вузлів фотоколориметра
- •Методика вимірювання оптичної густини на фотоколориметрі
- •Основні прийоми обробки аналітичного сигналу при фотометричних визначеннях
- •Контрольні питання
- •Задачі для самостійної роботи
- •Лабораторна робота визначення молярної концентрації іонів феруму (ііі) у розчині методом градуювального графіку
- •План експерименту
- •8.2. Рефрактометричний метод аналізу
- •8.2.1. Теоретичні основи методу
- •Апаратура рефрактометрії
- •Контрольні питання до теми:
- •8.3. Поляриметричний метод аналізу
- •8.3.1.Теоретичні основи методу
- •Основне рівняння поляриметричного методу аналізу
- •Апаратурне оснащення поляриметричного методу
- •Застосування поляриметричного методу аналізу
- •Лабораторна робота ідентифікація речовини за величиною питомого обертання
- •План експерименту
- •Контрольні питання
- •Глава 9. Хроматографічні методи аналізу
- •9.1. Теоретичні основи методу
- •Класифікація хроматографічних методів
- •9.2. Хроматографія в тонкому шарі сорбенту (тонкошарова хроматографія)
- •Етапи проведення аналізу методом тшх
- •6 . Проведення кількісного аналізу
- •Якісний аналіз барвників у суміші методом тонкошарової хроматографії
- •План експерименту
- •9.3. Іонообмінна хроматографія
- •Лабораторна робота визначення концентрації натрій хлориду методом іонообмінної хроматографії
- •План експерименту
- •Додатки
- •Класифікація методів кількісного аналізу
- •Класифікація титриметричних методів аналізу за типом хімічної реакції, яка лежить в основі методу
- •Класифікація титриметричних методів аналізу за способом титрування
- •Кислотно-основне титрування
- •Методи окисно-відновного титрування
- •Перманганатометричне титрування
- •Йодометричне титрування
- •Нітритометричне титрування
- •Броматометричне титрування
- •Цериметричне титрування
- •Хроматометричне титрування
- •Аргентометричне титрування
- •Тіоціанатометричне титрування (за методом Фольгарда)
- •Меркурометричне титрування
- •Комплексонометричне титрування
- •Меркуриметричне титрування
- •Список цитованої літератури
- •Глава 1. Загальні положення. Класифікація гравіметричних методів ….…4
- •Глава 2. Основні положення титриметричного аналізу …………………...…30
- •Глава 3. Розрахунки в титриметричному аналізі
- •Глава 4. Метод кислотно – основного титрування
- •Глава 5. Методи окисно-відновного титрування
- •Глава 6. Методи осаджувального титрування
- •Глава 7. Методи комплексоноутворення
- •7.1. Теоретичні основи методу……………………………………………..…173
- •Глава 8. Оптичні методи аналізу
- •Глава 9. Хроматографічні методи аналізу
Лабораторна робота визначення масової частки кристалізаційної води в кристалогідраті
Мета: визначити масову частку кристалізаційної води в кристалогідраті, розрахувати абсолютну і відносну похибки аналізу.
Суть методу: визначення кристалізаційної в кристалогідраті води відноситься до методу непрямої відгонки. Наважку кристалогідрату висушують при температурі 115°С до постійної маси та зважують. Через різницю в масі до та після висушування розраховують масову частку кристалізаційної води в кристалогідраті.
План експерименту:
1. Розрахунок маси наважки кристалогідрату:
![]()
де: m(H2O) = 0,1 г – норма видаленої води, за методом відгонки;
Wтеор.(Н2О) – приблизна теоретична масова частка кристалізаційної води в кристалогідраті, %.
![]()
де: z – кількість молекул води.
2. Взяття наважки.
Спочатку розраховану наважку кристалогідрату зважити на технохімічних терезах, а потім на аналітичних у межах mн ± 0,1 г.
Результати зважування занести в лабораторний журнал.
-
mб з н
=
mб
=
mн
=
Висушування наважки кристалогідрату в сушильній шафі при t°= 115°С протягом 1 години.
Охолодження бюкса з сіллю в ексикаторі протягом 15 хвилин і зважування на аналітичних терезах.
Результат зважування:
-
m б з гр.ф.
=
Повторне висушування бюкса з сіллю, охолодження в ексикаторі і зважування.
Результат зважування:
-
m´б з гр.ф.
=
Увага: сушити до постійної маси!
Розрахунок результатів аналізу.
6.1. Розрахунок практичного вмісту води:

6.2. Розрахунок абсолютної похибки аналізу:
![]()
6.3. Розрахунок відносної похибки аналізу:
![]()
7. Висновки.
Лабораторна робота визначення масової частки сульфат-іонів у магній сульфаті гравіметричним методом осадження
Мета: визначити масову частку сульфат-іонів у препараті, розрахувати абсолютну і відносну помилки експерименту.
Суть методу: визначення сульфат-іонів в препараті магній сульфату відноситься до методу осадження та засновано на практично незворотній хімічній реакції:
MgSO4 + BaCl2 → BaSO4↓ + MgCl2
SO42- + Ba2+ → BaSO4↓
Наважку препарату магній сульфату розчиняють у дистильованій воді, SO42--іони осаджують розчином барій хлориду у вигляді малорозчинного осаду барій сульфату; одержаний осад фільтрують, промивають, висушують, прожарюють до постійної маси та зважують. Через масу зваженого осаду барій сульфату розраховують вміст сульфат-іонів.
Схема аналізу:
![]()
осаджена форма гравіметрична
форма
План експерименту:
1. Розрахунок маси наважки кристалогідрату магній сульфату:

де: 0,4 г – норма важкого кристалічного осаду;
Wтеор.(SO42-) – приблизна теоретична масова частка сульфат-іонів в кристалогідраті, %:
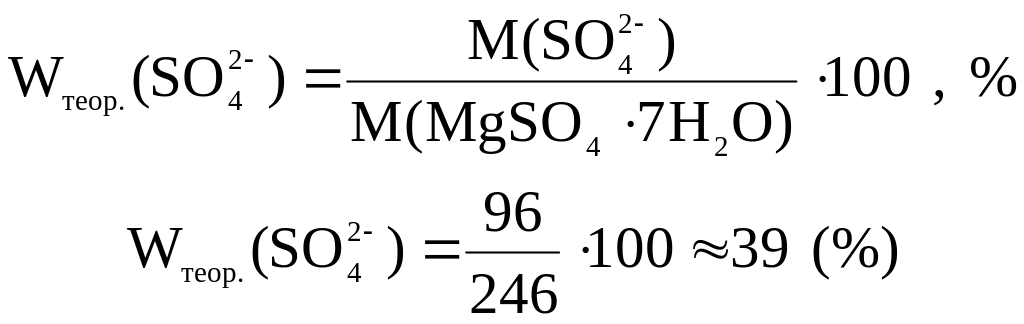
![]() –
гравіметричний
фактор:
–
гравіметричний
фактор:

2. Взяття наважки препарату на аналітичних терезах у межах mн ± 0,1 г.
Результати зважування занести в лабораторний журнал.
-
mб з н
=
mб
=
mн
=
3. Приготування розчину MgSO4 в термостійкому хімічному стакані об'ємом 150 см3.
Наважку MgSО4·7H2O кількісно перенести у хімічний стакан, розчинити в 30 см3 дистильованої води, додати 2 см3 10 % розчину хлоридної кислоти.
4. Розрахунок об'єму розчину осаджувача.
![]()
де: 1,5 – коефіцієнт надлишку осаджувача (розчин барій хлориду нелеткий, тому розрахований об'єм осаджувача збільшують на 50 %);
с(1/2ВаСl2) – молярна концентрація еквіваленту 1 моль/дм3.
![]()
5. Приготування розчину осаджувача в термостійкому хімічному стакані об'ємом 100 cм3.
У хімічний стакан за допомогою мірного циліндру відмірити 5 cм3 розчину барій хлориду з с(1/2ВаСl2) = 1 моль/дм3 та додати 50 cм3 дистильованої води.
6. Осадження іонів SO42- згідно до умов одержання кристалічних осадів.
Обидва стакани з розчинами одночасно нагріти на водяній бані до 60ºС.
Потім до розчину MgSO4 повільно, по краплях, при безперервному перемішуванні скляною паличкою, додати розчин барій хлориду.
7. Перевірка на повноту осадження.
Коли рідина над осадом посвітлішає, перевірити повноту осадження.
8. Дозрівання осаду – це процес збільшення кристалів осаду за розрахунок розчинення дрібних кристалів та осадження їх на більш великих кристалах. Це пасивний процес, тому зводиться до перебування осаду у теплі на протязі доби.
Стакан з осадом і скляною паличкою накрити папером, щоб виключити попадання пилу, і залишити для дозрівання осаду до наступного заняття.
9. Декантація, фільтрування та промивання осаду.
Зібрати установку для фільтрування. Використовувати беззольний фільтр «синя стрічка». Спочатку відділення осаду від розчину вести декантацією – зливати по скляній паличці на фільтр розчин до тих пір, доки осад не почне змучуватися. Коли майже увесь розчин злитий і осад починає змучуватися, у стакан з осадом додати 50 см3 промивної рідини (суміш дистильованої води та декількох крапель розчину осаджувача) і перемішати осад скляною паличкою, дати відстоятися та знов декантувати. Цю операцію повторити тричі.
Далі осад перенести на фільтр, при цьому направляти струмінь з промивалки на стінки стакану. Потім осад на фільтрі ще раз промити дистильованою водою.
10. Висушування осаду на фільтрі.
Фільтр з осадом разом із лійкою підсушити в сушильній шафі при температурі 105ºC так, щоб папір не був пересушений.
11. Озолення фільтру – це процес спалювання фільтру.
Фільтр зняти з лійки, згорнути його та перенести у тигель доведений до постійної маси. Тигель помістити у муфельну піч і провести озолення фільтру.
12. Прожарювання осаду у муфельній печі при температурі 800ºС протягом 1 години.
13. Охолодження тиглю з осадом в ексикаторі та зважування на аналітичних терезах.
Результат зважування:
-
mт з гр.ф.
=
14. Прожарювання осаду до постійної маси.
Результати зважування:
-
m´т з гр.ф.
=
mт.
=
mгр.ф.
=
15. Розрахунок результатів аналізу.
15.1. Розрахунок практичної масової частки сульфат-іонів у препараті магній сульфату:
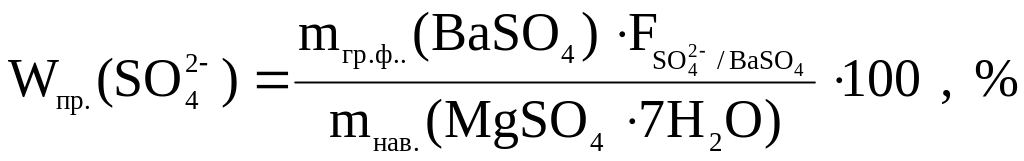
15.2. Розрахунок абсолютної похибки аналізу.
![]()
15.3. Розрахунок відносної похибки аналізу.
![]()
16. Висновки.
