
- •Глава 1. Загальні положення. Класифікація гравіметричних методів
- •Метод виділення
- •Метод відгонки
- •Методи осадження
- •Вимоги до осадженої форми
- •Вимоги до гравіметричної форми
- •Вимоги до осаджувача
- •Умови осадження кристалічних осадів
- •Умови осадження аморфних осадів
- •Послідовність аналітичних операцій в гравіметричному методі осадження
- •Практична робота розрахунок величини наважки в гравіметричному аналізі
- •Приклади розв'язування задач
- •Задачі для самостійної роботи
- •Практична робота розрахунок кількості осаджувача
- •Приклад розв'язування задач
- •Задачі до самостійної роботи
- •Практична робота розрахунок результатів аналізу в гравіметрії
- •Приклади розв'язування задач
- •Задачі до самостійної роботи
- •Лабораторна робота визначення масової частки кристалізаційної води в кристалогідраті
- •План експерименту:
- •Лабораторна робота визначення масової частки сульфат-іонів у магній сульфаті гравіметричним методом осадження
- •План експерименту:
- •Лабораторна робота визначення масової частки феруму в кристалогідраті ферум(іі) сульфату
- •План експерименту:
- •Контрольні питання:
- •Глава 2. Основні положення титриметричного аналізу
- •Вимоги до реакцій у титриметричному аналізі
- •Класифікація методів титриметрії в залежності від типу реакції
- •Класифікація методів титриметрії за способом титрування
- •Способи приготування стандартних розчинів
- •1. Приготування первинних стандартних розчинів
- •2. Приготування вторинних стандартних розчинів
- •3. Приготування стандартних розчинів із фіксаналів
- •Глава 3. Розрахунки в титриметричному аналізі
- •3.1. Способи виразу вмісту речовин у розчинах
- •3.2. Розрахункові формули титриметрії
- •Глава 4. Метод кислотно–основного титрування
- •4.1. Теоретичні основи методу
- •Індикатори методу кислотно-основного титрування
- •Показник індикаторів рК, показник титрування рН
- •Класифікація індикаторів
- •Криві титрування
- •1. Титрування сильних кислот сильними основами (Рис 1.)
- •2.Титрування слабких основ сильними кислотами. (Рис 2.)
- •3. Титрування слабких кислот сильними основами. (Рис 3.)
- •4. Титрування слабких кислот слабкими основами.
- •5. Титрування багатоосновних кислот (Рис 4.)
- •Кислотно-основне титрування в неводних середовищах
- •Робочі розчини у методах неводного титрування
- •Практичне використання методів кислотно-основного титрування в аналізі фармацевтичних препаратів
- •Практична робота способи виразу вмісту речовин у розчинах
- •Приклади розв’язання задач
- •Задачі для самостійної роботи
- •Рішення:
- •І Метод окремих наважок
- •Використаний прийом – метод окремих наважок.
- •Розв’язання задачі
- •Задачі для аудиторної роботи
- •Індивідуальні завдання для самостійної роботи студентів з теми «Метод кислотно-основного титрування»
- •Лабораторна робота калібрування мірного посуду. Визначення вмісту піпетки
- •План експерименту
- •Розрахунок маси наважки натрій гідроксиду
- •Взяття наважки лугу
- •Приготування розчину лугу
- •Приготування робочого розчину лугу
- •Висновок лабораторна робота аналіз мінеральної кислоти
- •Хімізм процесу
- •План експерименту
- •Зважувати концентровані кислоти треба в скляному бюксі із закритою кришкою і дуже обережно!!!
- •Лабораторна робота приготування і стандартизація розчину хлоридної кислоти
- •Хімізм процесу
- •План експерименту
- •II. Приготування розчину первинного стандарту натрій тетраборату
- •III. Стандартизація розчину хлоридної кислоти
- •IV. Висновок.
- •Визначення масової частки натрій карбонату у препараті проводять за II-ю точкою еквівалентності План експерименту
- •Лабораторна робота визначення вмісту аніліну в досліджуваному зразку
- •Хімізм процесу
- •План експерименту
- •Глава 5. Методи окисно-відновного титрування
- •5.1. Теоретичні основи методу
- •Окисно-відновні індикатори
- •5.2. Перманганатометрія
- •Приготування розчину kMnO4
- •Стандартизація розчину kMnO4
- •Задачі для самостійної роботи
- •Лабораторна робота приготування та стандартизація розчину калій перманганату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок.
- •Лабораторна робота
- •Визначення вмісту гідроген пероксиду
- •В лікарському препараті
- •Хімізм процесу
- •План експерименту
- •Лабораторна робота
- •Гептагідраті методом перманганатометрії
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •5.3. Хроматометрія
- •Лабораторна робота аналіз солі Fе(II) методом хроматометрії
- •Хімізм процесу
- •План експерименту
- •5.4. Цериметрія
- •5.5. Йодометрія
- •Приготування розчину Na2s2o3
- •Приготування розчину і2
- •Використання методу
- •Лабораторна робота приготування та стандартизація робочого розчину натрій тіосульфату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок. Лабораторна робота приготування та стандартизація розчину йоду
- •Хімізм процесу
- •План експерименту
- •IV. Висновок
- •План експерименту
- •V. Висновок.
- •План експерименту
- •Лабораторна робота аналіз аскорбінової кислоти методом йодометрії
- •Аскорбінова кислота
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.6. Броматометрія
- •Лабораторна робота визначення вмісту стрептоциду в препараті методом броматометрії
- •Хімізм процесу
- •Принцип методу заміщення
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.7. Нітритометрія
- •Умови проведення реакції діазотування
- •Визначення точки еквівалентності
- •Лабораторна робота приготування та стандартизація робочого розчину натрій нітриту
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання до самостійної роботи
- •Глава 7. Методи осаджувального титрування
- •7.1. Теоретичні основи методу
- •Класифікація методів осадження
- •Вимоги до реакцій, що використовуються в методах осадження
- •Індикатори методів осадження
- •5.2. Аргентометрія
- •Метод Мора
- •Умови титрування за методом Фаянса–Ходакова
- •6.3. Тіоціанатометрія Метод Фольгарда
- •Умови титрування за методом Фольгарда
- •6.4. Меркурометрія
- •Приготування та стандартизація розчину титранту
- •Переваги та недоліки меркурометрії перед іншими методами осадження
- •Завдання для самостійної роботи
- •План експерименту
- •Лабораторна робота визначення масової частки калій йодиду методом фольгарда
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 7. Методи комплексоутворення
- •7.1. Теоретичні основи методу
- •7.2. Комплексонометрія (трилонометрія)
- •Принцип дії металохромних індикаторів
- •7.3. Меркуриметрія
- •Задачі для самостійної роботи
- •Лабораторна робота приготування і стандартизація розчину комплексону ііі (трилону б, едта)
- •Хімізм процесу
- •План експерименту
- •III. Стандартизація титранту комплексону ііі.
- •Висновок.
- •Лабораторна робота
- •Аналіз кальцій хлориду гексагідрату
- •Комплексонометричним методом
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 8. Оптичні методи аналізу
- •8.1. Абсорбційні методи аналізу
- •8.1.1. Теоретичні основи
- •Основний закон світлопоглинання (закон Бугера - Ламберта-Бера)
- •Апаратура молекулярно-абсорбційних методів
- •Характеристика та функціональне призначення основних вузлів фотоколориметра
- •Методика вимірювання оптичної густини на фотоколориметрі
- •Основні прийоми обробки аналітичного сигналу при фотометричних визначеннях
- •Контрольні питання
- •Задачі для самостійної роботи
- •Лабораторна робота визначення молярної концентрації іонів феруму (ііі) у розчині методом градуювального графіку
- •План експерименту
- •8.2. Рефрактометричний метод аналізу
- •8.2.1. Теоретичні основи методу
- •Апаратура рефрактометрії
- •Контрольні питання до теми:
- •8.3. Поляриметричний метод аналізу
- •8.3.1.Теоретичні основи методу
- •Основне рівняння поляриметричного методу аналізу
- •Апаратурне оснащення поляриметричного методу
- •Застосування поляриметричного методу аналізу
- •Лабораторна робота ідентифікація речовини за величиною питомого обертання
- •План експерименту
- •Контрольні питання
- •Глава 9. Хроматографічні методи аналізу
- •9.1. Теоретичні основи методу
- •Класифікація хроматографічних методів
- •9.2. Хроматографія в тонкому шарі сорбенту (тонкошарова хроматографія)
- •Етапи проведення аналізу методом тшх
- •6 . Проведення кількісного аналізу
- •Якісний аналіз барвників у суміші методом тонкошарової хроматографії
- •План експерименту
- •9.3. Іонообмінна хроматографія
- •Лабораторна робота визначення концентрації натрій хлориду методом іонообмінної хроматографії
- •План експерименту
- •Додатки
- •Класифікація методів кількісного аналізу
- •Класифікація титриметричних методів аналізу за типом хімічної реакції, яка лежить в основі методу
- •Класифікація титриметричних методів аналізу за способом титрування
- •Кислотно-основне титрування
- •Методи окисно-відновного титрування
- •Перманганатометричне титрування
- •Йодометричне титрування
- •Нітритометричне титрування
- •Броматометричне титрування
- •Цериметричне титрування
- •Хроматометричне титрування
- •Аргентометричне титрування
- •Тіоціанатометричне титрування (за методом Фольгарда)
- •Меркурометричне титрування
- •Комплексонометричне титрування
- •Меркуриметричне титрування
- •Список цитованої літератури
- •Глава 1. Загальні положення. Класифікація гравіметричних методів ….…4
- •Глава 2. Основні положення титриметричного аналізу …………………...…30
- •Глава 3. Розрахунки в титриметричному аналізі
- •Глава 4. Метод кислотно – основного титрування
- •Глава 5. Методи окисно-відновного титрування
- •Глава 6. Методи осаджувального титрування
- •Глава 7. Методи комплексоноутворення
- •7.1. Теоретичні основи методу……………………………………………..…173
- •Глава 8. Оптичні методи аналізу
- •Глава 9. Хроматографічні методи аналізу
Лабораторна робота приготування та стандартизація розчину калій перманганату
Мета: приготувати розчин калій перманганату з с( KMnO4)= 0,05 моль/дм3 і простандартизувати його за первинним стандартом амоній оксалатом (NH4)2C2O4·H2O.
Сутність методу: аліквотну частину розчину первинного стандарту амоній оксалату відтитрвують розчином титранту калій перманганату у сульфатно-кислому середовищі.
Аналітичні прийоми: метод прямого титрування, метод піпетування.
Хімізм процесу
5(NH4)2C2O4 + 2KMnO4+ 8H2SO4 → 2MnSO4 +10СО2↑+ 5(NH4)2SO4 + 5K2SO4 + 8Н2О
MnO + 8H+ + 5ē F Mn2+ + 4H2O |
2
|
C2O – 2ē F 2CO2↑ |
5
|
2MnO + 16H+ + C2O → 2Mn2+ + 10CO2↑ + 8H2O |
|
ЕРС
=
![]() = 1,51 –
(–
0,49)
= 2,00 В
= 1,51 –
(–
0,49)
= 2,00 В
М( КМnO4) = 31,61г/моль; fекв=1/5
М( (NH4)2C2O4·H2O) = 71,06 г/моль; fекв=1/2
Усі продукти цієї реакції безкольорові, тоді як розчин КМnО4 має червоно-фіолетове забарвлення. В ході реакції забарвлення розчину зникає. Каталізатором є Мn2+-іони – продукт реакції. Спочатку реакція проходить дуже повільно. З накопичуванням іонів Мn2+ у розчині швидкість реакції різко зростає. Реакція – автокаталітична.
План експерименту
І. Приготування розчину калій перманганату.
1. Розрахунок наважки КМnО4.
![]()
Вихідні дані: Vр-ну = 500 см3
с( КМnО4) = 0,05 моль/дм3
![]()
2. Взяття наважки.
Розраховану наважку КМnО4 зважити на технохімічних терезах на годинниковому склі. Якщо вихідний КМnО4 крупнокристалічний, його спочатку необхідно обережно подрібнити у порцеляновій ступці.
3. Приготування розчину калій перманганату.
Вихідний КМnО4 містить домішки, з яких найбільш значною є манган(IV) оксид МnО2. Крім того, у перші дні після приготування розчину відбувається відновлення КМnО4 домішками, які є навіть у дистильованій воді, в результаті концентрація розчину змінюється. Тому розчин КМnО4 готують приблизної концентрації і стандартизують його через 7-10 днів.
Наважку КМnО4 розчинити у стакані об'ємом 500 см3 у 100 см3 прокип'яченої і охолодженої дистильованої води та декантувати цей розчин у чисто вимиту склянку. Операцію повторити декілька разів до повного розчинення KMnO4, після чого об'єм розчину довести до 500 см3 дистильованою водою.
Приготований розчин КМnО4 необхідно зберігати у темній склянці з притертою пробкою.
ІІ. Приготування розчину первинного стандарту амоній оксалату.
1. Розрахунок наважки (NH4)2C2O4·H2O.
![]()
Вихідні дані: Vм.к. = 250,0 см3
с( (NH4)2C2O4·H2O) = 0,05 моль/дм3
![]()
2. Взяття наважки кристалогідрату амоній оксалату на аналітичних терезах у межах mн. ± 0,1 г.
Результати зважування занести в лабораторний журнал.
-
mб з н.
=
mб.
=
mн.
=
3. Приготування розчину.
Наважку амоній оксалату кількісно перенести за допомогою сухої лійки до мірної колби об'ємом 250 см3, додати 1/3 від об'єму колби дистильованої води, розчинити наважку, потім довести об'єм розчину до мітки дистильованою водою та ретельно перемішати.
ІІІ. Стандартизація розчину KMnO4.
1. Процес титрування.
Бюретку сполоснути розчином КМnО4 і заповнити її, встановив нульову позначку за верхнім меніском. У конічну колбу для титрування піпеткою відібрати аліквотну частину розчину амоній оксалату, 10 см3 розчину сульфатної кислоти (с( H2SO4) = 2 моль/дм3), суміш нагріти до 70-80 ºС та відтитрувати розчином KМnO4 до слабко-рожевого забарвлення.
Титрувати не менше трьох разів. Результати титрування не повинні відрізнятися більш, ніж на 0,1 см3.
2. Результати титрування записати в таблицю.
|
1 |
2 |
3 |
|
V((NH4)2С2О4), см3 |
|
|
|
|
V(КМnO4), см3 |
|
|
|
|
3. Розрахунок результатів аналізу.
3.1. Розрахунок молярної концентрації еквіваленту розчину амоній оксалату:
![]()
3.2. Розрахунок молярної концентрації еквіваленту розчину калій перманганату:
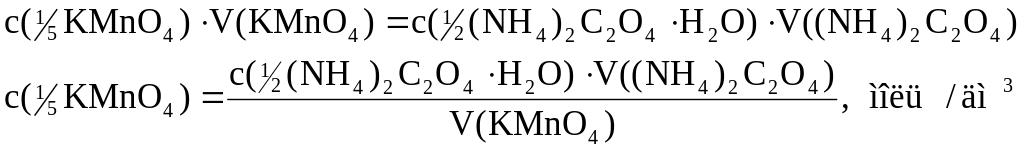
Загальна розрахункова формула:
![]()
Розрахунок коефіцієнту поправки розчину калій перманганату, якщо
стеор. = 0,05 моль/дм3:
![]()
