
- •Глава 1. Загальні положення. Класифікація гравіметричних методів
- •Метод виділення
- •Метод відгонки
- •Методи осадження
- •Вимоги до осадженої форми
- •Вимоги до гравіметричної форми
- •Вимоги до осаджувача
- •Умови осадження кристалічних осадів
- •Умови осадження аморфних осадів
- •Послідовність аналітичних операцій в гравіметричному методі осадження
- •Практична робота розрахунок величини наважки в гравіметричному аналізі
- •Приклади розв'язування задач
- •Задачі для самостійної роботи
- •Практична робота розрахунок кількості осаджувача
- •Приклад розв'язування задач
- •Задачі до самостійної роботи
- •Практична робота розрахунок результатів аналізу в гравіметрії
- •Приклади розв'язування задач
- •Задачі до самостійної роботи
- •Лабораторна робота визначення масової частки кристалізаційної води в кристалогідраті
- •План експерименту:
- •Лабораторна робота визначення масової частки сульфат-іонів у магній сульфаті гравіметричним методом осадження
- •План експерименту:
- •Лабораторна робота визначення масової частки феруму в кристалогідраті ферум(іі) сульфату
- •План експерименту:
- •Контрольні питання:
- •Глава 2. Основні положення титриметричного аналізу
- •Вимоги до реакцій у титриметричному аналізі
- •Класифікація методів титриметрії в залежності від типу реакції
- •Класифікація методів титриметрії за способом титрування
- •Способи приготування стандартних розчинів
- •1. Приготування первинних стандартних розчинів
- •2. Приготування вторинних стандартних розчинів
- •3. Приготування стандартних розчинів із фіксаналів
- •Глава 3. Розрахунки в титриметричному аналізі
- •3.1. Способи виразу вмісту речовин у розчинах
- •3.2. Розрахункові формули титриметрії
- •Глава 4. Метод кислотно–основного титрування
- •4.1. Теоретичні основи методу
- •Індикатори методу кислотно-основного титрування
- •Показник індикаторів рК, показник титрування рН
- •Класифікація індикаторів
- •Криві титрування
- •1. Титрування сильних кислот сильними основами (Рис 1.)
- •2.Титрування слабких основ сильними кислотами. (Рис 2.)
- •3. Титрування слабких кислот сильними основами. (Рис 3.)
- •4. Титрування слабких кислот слабкими основами.
- •5. Титрування багатоосновних кислот (Рис 4.)
- •Кислотно-основне титрування в неводних середовищах
- •Робочі розчини у методах неводного титрування
- •Практичне використання методів кислотно-основного титрування в аналізі фармацевтичних препаратів
- •Практична робота способи виразу вмісту речовин у розчинах
- •Приклади розв’язання задач
- •Задачі для самостійної роботи
- •Рішення:
- •І Метод окремих наважок
- •Використаний прийом – метод окремих наважок.
- •Розв’язання задачі
- •Задачі для аудиторної роботи
- •Індивідуальні завдання для самостійної роботи студентів з теми «Метод кислотно-основного титрування»
- •Лабораторна робота калібрування мірного посуду. Визначення вмісту піпетки
- •План експерименту
- •Розрахунок маси наважки натрій гідроксиду
- •Взяття наважки лугу
- •Приготування розчину лугу
- •Приготування робочого розчину лугу
- •Висновок лабораторна робота аналіз мінеральної кислоти
- •Хімізм процесу
- •План експерименту
- •Зважувати концентровані кислоти треба в скляному бюксі із закритою кришкою і дуже обережно!!!
- •Лабораторна робота приготування і стандартизація розчину хлоридної кислоти
- •Хімізм процесу
- •План експерименту
- •II. Приготування розчину первинного стандарту натрій тетраборату
- •III. Стандартизація розчину хлоридної кислоти
- •IV. Висновок.
- •Визначення масової частки натрій карбонату у препараті проводять за II-ю точкою еквівалентності План експерименту
- •Лабораторна робота визначення вмісту аніліну в досліджуваному зразку
- •Хімізм процесу
- •План експерименту
- •Глава 5. Методи окисно-відновного титрування
- •5.1. Теоретичні основи методу
- •Окисно-відновні індикатори
- •5.2. Перманганатометрія
- •Приготування розчину kMnO4
- •Стандартизація розчину kMnO4
- •Задачі для самостійної роботи
- •Лабораторна робота приготування та стандартизація розчину калій перманганату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок.
- •Лабораторна робота
- •Визначення вмісту гідроген пероксиду
- •В лікарському препараті
- •Хімізм процесу
- •План експерименту
- •Лабораторна робота
- •Гептагідраті методом перманганатометрії
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •5.3. Хроматометрія
- •Лабораторна робота аналіз солі Fе(II) методом хроматометрії
- •Хімізм процесу
- •План експерименту
- •5.4. Цериметрія
- •5.5. Йодометрія
- •Приготування розчину Na2s2o3
- •Приготування розчину і2
- •Використання методу
- •Лабораторна робота приготування та стандартизація робочого розчину натрій тіосульфату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок. Лабораторна робота приготування та стандартизація розчину йоду
- •Хімізм процесу
- •План експерименту
- •IV. Висновок
- •План експерименту
- •V. Висновок.
- •План експерименту
- •Лабораторна робота аналіз аскорбінової кислоти методом йодометрії
- •Аскорбінова кислота
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.6. Броматометрія
- •Лабораторна робота визначення вмісту стрептоциду в препараті методом броматометрії
- •Хімізм процесу
- •Принцип методу заміщення
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.7. Нітритометрія
- •Умови проведення реакції діазотування
- •Визначення точки еквівалентності
- •Лабораторна робота приготування та стандартизація робочого розчину натрій нітриту
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання до самостійної роботи
- •Глава 7. Методи осаджувального титрування
- •7.1. Теоретичні основи методу
- •Класифікація методів осадження
- •Вимоги до реакцій, що використовуються в методах осадження
- •Індикатори методів осадження
- •5.2. Аргентометрія
- •Метод Мора
- •Умови титрування за методом Фаянса–Ходакова
- •6.3. Тіоціанатометрія Метод Фольгарда
- •Умови титрування за методом Фольгарда
- •6.4. Меркурометрія
- •Приготування та стандартизація розчину титранту
- •Переваги та недоліки меркурометрії перед іншими методами осадження
- •Завдання для самостійної роботи
- •План експерименту
- •Лабораторна робота визначення масової частки калій йодиду методом фольгарда
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 7. Методи комплексоутворення
- •7.1. Теоретичні основи методу
- •7.2. Комплексонометрія (трилонометрія)
- •Принцип дії металохромних індикаторів
- •7.3. Меркуриметрія
- •Задачі для самостійної роботи
- •Лабораторна робота приготування і стандартизація розчину комплексону ііі (трилону б, едта)
- •Хімізм процесу
- •План експерименту
- •III. Стандартизація титранту комплексону ііі.
- •Висновок.
- •Лабораторна робота
- •Аналіз кальцій хлориду гексагідрату
- •Комплексонометричним методом
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 8. Оптичні методи аналізу
- •8.1. Абсорбційні методи аналізу
- •8.1.1. Теоретичні основи
- •Основний закон світлопоглинання (закон Бугера - Ламберта-Бера)
- •Апаратура молекулярно-абсорбційних методів
- •Характеристика та функціональне призначення основних вузлів фотоколориметра
- •Методика вимірювання оптичної густини на фотоколориметрі
- •Основні прийоми обробки аналітичного сигналу при фотометричних визначеннях
- •Контрольні питання
- •Задачі для самостійної роботи
- •Лабораторна робота визначення молярної концентрації іонів феруму (ііі) у розчині методом градуювального графіку
- •План експерименту
- •8.2. Рефрактометричний метод аналізу
- •8.2.1. Теоретичні основи методу
- •Апаратура рефрактометрії
- •Контрольні питання до теми:
- •8.3. Поляриметричний метод аналізу
- •8.3.1.Теоретичні основи методу
- •Основне рівняння поляриметричного методу аналізу
- •Апаратурне оснащення поляриметричного методу
- •Застосування поляриметричного методу аналізу
- •Лабораторна робота ідентифікація речовини за величиною питомого обертання
- •План експерименту
- •Контрольні питання
- •Глава 9. Хроматографічні методи аналізу
- •9.1. Теоретичні основи методу
- •Класифікація хроматографічних методів
- •9.2. Хроматографія в тонкому шарі сорбенту (тонкошарова хроматографія)
- •Етапи проведення аналізу методом тшх
- •6 . Проведення кількісного аналізу
- •Якісний аналіз барвників у суміші методом тонкошарової хроматографії
- •План експерименту
- •9.3. Іонообмінна хроматографія
- •Лабораторна робота визначення концентрації натрій хлориду методом іонообмінної хроматографії
- •План експерименту
- •Додатки
- •Класифікація методів кількісного аналізу
- •Класифікація титриметричних методів аналізу за типом хімічної реакції, яка лежить в основі методу
- •Класифікація титриметричних методів аналізу за способом титрування
- •Кислотно-основне титрування
- •Методи окисно-відновного титрування
- •Перманганатометричне титрування
- •Йодометричне титрування
- •Нітритометричне титрування
- •Броматометричне титрування
- •Цериметричне титрування
- •Хроматометричне титрування
- •Аргентометричне титрування
- •Тіоціанатометричне титрування (за методом Фольгарда)
- •Меркурометричне титрування
- •Комплексонометричне титрування
- •Меркуриметричне титрування
- •Список цитованої літератури
- •Глава 1. Загальні положення. Класифікація гравіметричних методів ….…4
- •Глава 2. Основні положення титриметричного аналізу …………………...…30
- •Глава 3. Розрахунки в титриметричному аналізі
- •Глава 4. Метод кислотно – основного титрування
- •Глава 5. Методи окисно-відновного титрування
- •Глава 6. Методи осаджувального титрування
- •Глава 7. Методи комплексоноутворення
- •7.1. Теоретичні основи методу……………………………………………..…173
- •Глава 8. Оптичні методи аналізу
- •Глава 9. Хроматографічні методи аналізу
Лабораторна робота визначення вмісту аніліну в досліджуваному зразку
Мета: визначити вміст аніліну в досліджуваному зразку методом кислотно-основного титрування в неводному середовищі.
Сутність методу: розраховану точну наважку досліджуваного зразку аніліну розчиняють у 50 см3 безводної ацетатної кислоти і титрують стандартним розчином хлоратної(VII) кислоти в присутності індикатору метилового фіолетового.
Аналітичні прийоми: метод окремих наважок, пряме титрування.
Хімізм процесу
![]()
М(C6H5NH2) = 93,14 г/моль
План експерименту
Розрахунок наважки досліджуваного зразку аніліну:
![]()
За законом еквівалентів:
![]()
![]() ,
,
![]()
Вихідні дані: V(HClO4) = Vmin = 15 см3; с(HClO4)=0,1моль/дм3.
![]()
Взяття наважки аніліну на аналітичних терезах:
Результати зважування занести в лабораторний журнал.
-
mб з н.
=
mб.
=
mн.
=
Приготування розчину.
Наважку кількісно перенести у колбу для титрування, розчинити у 50 см3 безводної ацетатної кислоти, додати 2-3 краплі розчину метилового фіолетового.
4. Процес титрування.
Приготований розчин титрувати стандартним розчином хлоратної(VII) кислоти до переходу забарвлення розчину від фіолетового до синього. Титрування проводять до одержання відтворюваних результатів.
У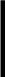 вага!
Титрування необхідно проводити в
ретельно закритих склянках або в
атмосфері інертного газу. Якщо температура
розчину хлоратної(VII)
кислоти при титруванні відрізнялась
від температури її стандартизації, то
необхідно температуру одержаного об’єму
розчину довести до температури
стандартизації.
вага!
Титрування необхідно проводити в
ретельно закритих склянках або в
атмосфері інертного газу. Якщо температура
розчину хлоратної(VII)
кислоти при титруванні відрізнялась
від температури її стандартизації, то
необхідно температуру одержаного об’єму
розчину довести до температури
стандартизації.
5. Результати титрування записати в таблицю:
|
1 |
2 |
3 |
m(C6H5NH2), г |
|
|
|
V(HClO4), см3 |
|
|
|
6.Розрахунки результатів аналізу.
Розрахунок титру відповідності:
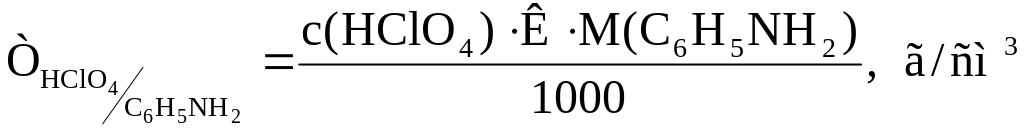
6.2. Розрахунок масової частки аніліну в досліджуваному зразку:
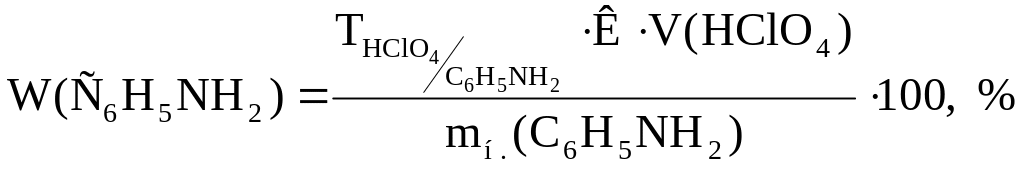
( формула у загальному вигляді наведена на ст. 37)
6.3. Розрахунок середнього результату:
![]()
Висновок.
Глава 5. Методи окисно-відновного титрування
5.1. Теоретичні основи методу
Методи окисно-відновного титрування основані на використанні реакцій, які пов’язані з переносом електронів, тобто окисно-відновних процесів.
Ці методи дозволяють визначати всі неорганічні речовини та багато органічних сполук (у тому числі і фармацевтичні препарати, переважна більшість яких, є відновниками).
Окисно-відновних реакцій відомо багато (біля 100 000). В кількісному аналізі використовують тільки ті реакції, які відповідають загальним вимогам, які висувають до реакцій в титриметричному аналізі:
1. Реакції повинні перебігати практично до кінця. Окисно-відновна реакція проходить тим повніше, чим більше константа окисно-відновної рівноваги. Чим більше різниця в значеннях стандартних окисно-відновних потенціалах редокс-пар, що беруть участь в процесі ΔЕ°= Е1° – Е2°, тим більше К рівноваги, тим повніше проходить реакція.
В кількісному аналізі використовують реакції з константами рівноваги Кр > 1·108, вони є стехіометричними. ЕРС (ΔЕ°) при хімічних способах встановлення кінця титрування повинна бути не менш, ніж 0,4-0,5 В, при інструментальних – не менш, ніж 0,2 В. В протилежному випадку реакція проходить або не до кінця, або при титруванні відсутній різкий стрибок потенціалу поблизу точки еквівалентності.
2. Реакція повинна перебігати достатньо швидко, щоб рівновага, за якої реальні редокс-потенціали були рівними, встановлювалась практично миттєво. Якщо реакція перебігає повільно, її прискорюють, підвищуючи температуру розчинів або додаючи каталізатори. Іноді каталізаторами є самі продукти реакції. Так, наприклад, при перманганатометричному титруванні оксалатів в кислому середовищі
5C2O42– + 2MnO4– + 16H+ → 2Mn2+ + 10CO2 + 8H2O
каталізатором є катіони Мангану(ІІ) – продукти реакції. Тому спочатку реакція перебігає повільно, з накопиченням Mn2+ прискорюється. Такі реакції називаються автокаталітичними.
3. Реакція повинна перебігати стехіометрично, побічні процеси виключені.
4. Кінцева точка титрування повинна визначатись точно й однозначно .
В якості стандартних речовин використовують розчини окисників або відновників.
У залежності від властивостей титранту, що використовують, розрізняють:
оксидиметрію – метод визначення відновників шляхом титрування їх стандартними розчинами окисників. Наприклад, в якості титрантів використовують стандартні розчини калій бромату, калій перманганату, калій дихромату тощо;
редуктометрію – метод визначення окисників шляхом титрування їх стандартними розчинами відновників. Наприклад, в якості титрантів використовують стандартні розчини аскорбінової кислоти, розчини солей Ферум(ІІ)-катіона.
Розроблено більш, ніж 50 методів окисно-відновного титрування (редокс-методів). Їх класифікують за типом титранту. Найбільш поширене використання отримали наступні методи:
перманганатометрія (титрант – розчин KMnO4);
йодометрія (титранти – розчини І2 та Na2S2O3);
броматометрія (титрант – розчин KBrO3);
нітритометрія (титрант – розчин NaNO2);
хроматометрія (титрант – розчин K2Cr2O7);
цериметрія (титрант – розчин Се(IV));
аскорбінометрія (титрант – розчин аскорбінової кислоти);
йодохлориметрія (титрант – розчин ICl) та ін.
В редокс-методах використовують пряме, зворотнє, замісникове титрування.
Пряме титрування використовують у тих випадках, коли швидкість реакції значна, а ЕРС ≥ 0,4 В, що забезпечує повноту її перебігу.
Прямим титруванням визначають, наприклад, дийод (титрант-відновник Na2S2O3, ЕРС ≥ 0,42 В, Кр = 1012), солі Феруму(ІІ) (титрант – розчин KMnO4, ЕРС ≥ 0,74 В, Кр = 106,4) та ін.
Зворотне титрування використовують, якщо реакція перебігає повільно, а також для визначення летких сполук та тих, що прямо не реагують з титрантом.
Наприклад, при визначенні сульфід-іонів, до їх розчину додають точно відомий надлишок стандартного розчину дийоду, залишок якого відтитровують стандартним розчином натрій тіосульфату:
Na2S + І2 + 2HCl → S + 2NaCl + 2HI
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
Титрування замісника використовують у тих випадках, коли досліджувана речовина не вступає в окисно-відновну реакцію з титрантом або реакція проходить не стехіометрично.
Наприклад, при йодометричному визначенні сильних окисників у кислому середовищі до їх розчину додають надлишок розчину КІ. Дийод, який виділився при цьому, відтитровують стандартним розчином Na2S2O3.
K2Cr2O7 + 6KI + 7H2SO4 → Cr2(SO4)3 + 3I2 + 4K2SO4 + 7H2O
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
