
- •Глава 1. Загальні положення. Класифікація гравіметричних методів
- •Метод виділення
- •Метод відгонки
- •Методи осадження
- •Вимоги до осадженої форми
- •Вимоги до гравіметричної форми
- •Вимоги до осаджувача
- •Умови осадження кристалічних осадів
- •Умови осадження аморфних осадів
- •Послідовність аналітичних операцій в гравіметричному методі осадження
- •Практична робота розрахунок величини наважки в гравіметричному аналізі
- •Приклади розв'язування задач
- •Задачі для самостійної роботи
- •Практична робота розрахунок кількості осаджувача
- •Приклад розв'язування задач
- •Задачі до самостійної роботи
- •Практична робота розрахунок результатів аналізу в гравіметрії
- •Приклади розв'язування задач
- •Задачі до самостійної роботи
- •Лабораторна робота визначення масової частки кристалізаційної води в кристалогідраті
- •План експерименту:
- •Лабораторна робота визначення масової частки сульфат-іонів у магній сульфаті гравіметричним методом осадження
- •План експерименту:
- •Лабораторна робота визначення масової частки феруму в кристалогідраті ферум(іі) сульфату
- •План експерименту:
- •Контрольні питання:
- •Глава 2. Основні положення титриметричного аналізу
- •Вимоги до реакцій у титриметричному аналізі
- •Класифікація методів титриметрії в залежності від типу реакції
- •Класифікація методів титриметрії за способом титрування
- •Способи приготування стандартних розчинів
- •1. Приготування первинних стандартних розчинів
- •2. Приготування вторинних стандартних розчинів
- •3. Приготування стандартних розчинів із фіксаналів
- •Глава 3. Розрахунки в титриметричному аналізі
- •3.1. Способи виразу вмісту речовин у розчинах
- •3.2. Розрахункові формули титриметрії
- •Глава 4. Метод кислотно–основного титрування
- •4.1. Теоретичні основи методу
- •Індикатори методу кислотно-основного титрування
- •Показник індикаторів рК, показник титрування рН
- •Класифікація індикаторів
- •Криві титрування
- •1. Титрування сильних кислот сильними основами (Рис 1.)
- •2.Титрування слабких основ сильними кислотами. (Рис 2.)
- •3. Титрування слабких кислот сильними основами. (Рис 3.)
- •4. Титрування слабких кислот слабкими основами.
- •5. Титрування багатоосновних кислот (Рис 4.)
- •Кислотно-основне титрування в неводних середовищах
- •Робочі розчини у методах неводного титрування
- •Практичне використання методів кислотно-основного титрування в аналізі фармацевтичних препаратів
- •Практична робота способи виразу вмісту речовин у розчинах
- •Приклади розв’язання задач
- •Задачі для самостійної роботи
- •Рішення:
- •І Метод окремих наважок
- •Використаний прийом – метод окремих наважок.
- •Розв’язання задачі
- •Задачі для аудиторної роботи
- •Індивідуальні завдання для самостійної роботи студентів з теми «Метод кислотно-основного титрування»
- •Лабораторна робота калібрування мірного посуду. Визначення вмісту піпетки
- •План експерименту
- •Розрахунок маси наважки натрій гідроксиду
- •Взяття наважки лугу
- •Приготування розчину лугу
- •Приготування робочого розчину лугу
- •Висновок лабораторна робота аналіз мінеральної кислоти
- •Хімізм процесу
- •План експерименту
- •Зважувати концентровані кислоти треба в скляному бюксі із закритою кришкою і дуже обережно!!!
- •Лабораторна робота приготування і стандартизація розчину хлоридної кислоти
- •Хімізм процесу
- •План експерименту
- •II. Приготування розчину первинного стандарту натрій тетраборату
- •III. Стандартизація розчину хлоридної кислоти
- •IV. Висновок.
- •Визначення масової частки натрій карбонату у препараті проводять за II-ю точкою еквівалентності План експерименту
- •Лабораторна робота визначення вмісту аніліну в досліджуваному зразку
- •Хімізм процесу
- •План експерименту
- •Глава 5. Методи окисно-відновного титрування
- •5.1. Теоретичні основи методу
- •Окисно-відновні індикатори
- •5.2. Перманганатометрія
- •Приготування розчину kMnO4
- •Стандартизація розчину kMnO4
- •Задачі для самостійної роботи
- •Лабораторна робота приготування та стандартизація розчину калій перманганату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок.
- •Лабораторна робота
- •Визначення вмісту гідроген пероксиду
- •В лікарському препараті
- •Хімізм процесу
- •План експерименту
- •Лабораторна робота
- •Гептагідраті методом перманганатометрії
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •5.3. Хроматометрія
- •Лабораторна робота аналіз солі Fе(II) методом хроматометрії
- •Хімізм процесу
- •План експерименту
- •5.4. Цериметрія
- •5.5. Йодометрія
- •Приготування розчину Na2s2o3
- •Приготування розчину і2
- •Використання методу
- •Лабораторна робота приготування та стандартизація робочого розчину натрій тіосульфату
- •Хімізм процесу
- •План експерименту
- •IV. Висновок. Лабораторна робота приготування та стандартизація розчину йоду
- •Хімізм процесу
- •План експерименту
- •IV. Висновок
- •План експерименту
- •V. Висновок.
- •План експерименту
- •Лабораторна робота аналіз аскорбінової кислоти методом йодометрії
- •Аскорбінова кислота
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.6. Броматометрія
- •Лабораторна робота визначення вмісту стрептоциду в препараті методом броматометрії
- •Хімізм процесу
- •Принцип методу заміщення
- •План експерименту
- •Контрольні питання
- •Завдання для самостійної роботи
- •5.7. Нітритометрія
- •Умови проведення реакції діазотування
- •Визначення точки еквівалентності
- •Лабораторна робота приготування та стандартизація робочого розчину натрій нітриту
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Завдання до самостійної роботи
- •Глава 7. Методи осаджувального титрування
- •7.1. Теоретичні основи методу
- •Класифікація методів осадження
- •Вимоги до реакцій, що використовуються в методах осадження
- •Індикатори методів осадження
- •5.2. Аргентометрія
- •Метод Мора
- •Умови титрування за методом Фаянса–Ходакова
- •6.3. Тіоціанатометрія Метод Фольгарда
- •Умови титрування за методом Фольгарда
- •6.4. Меркурометрія
- •Приготування та стандартизація розчину титранту
- •Переваги та недоліки меркурометрії перед іншими методами осадження
- •Завдання для самостійної роботи
- •План експерименту
- •Лабораторна робота визначення масової частки калій йодиду методом фольгарда
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 7. Методи комплексоутворення
- •7.1. Теоретичні основи методу
- •7.2. Комплексонометрія (трилонометрія)
- •Принцип дії металохромних індикаторів
- •7.3. Меркуриметрія
- •Задачі для самостійної роботи
- •Лабораторна робота приготування і стандартизація розчину комплексону ііі (трилону б, едта)
- •Хімізм процесу
- •План експерименту
- •III. Стандартизація титранту комплексону ііі.
- •Висновок.
- •Лабораторна робота
- •Аналіз кальцій хлориду гексагідрату
- •Комплексонометричним методом
- •Хімізм процесу
- •План експерименту
- •Контрольні питання
- •Глава 8. Оптичні методи аналізу
- •8.1. Абсорбційні методи аналізу
- •8.1.1. Теоретичні основи
- •Основний закон світлопоглинання (закон Бугера - Ламберта-Бера)
- •Апаратура молекулярно-абсорбційних методів
- •Характеристика та функціональне призначення основних вузлів фотоколориметра
- •Методика вимірювання оптичної густини на фотоколориметрі
- •Основні прийоми обробки аналітичного сигналу при фотометричних визначеннях
- •Контрольні питання
- •Задачі для самостійної роботи
- •Лабораторна робота визначення молярної концентрації іонів феруму (ііі) у розчині методом градуювального графіку
- •План експерименту
- •8.2. Рефрактометричний метод аналізу
- •8.2.1. Теоретичні основи методу
- •Апаратура рефрактометрії
- •Контрольні питання до теми:
- •8.3. Поляриметричний метод аналізу
- •8.3.1.Теоретичні основи методу
- •Основне рівняння поляриметричного методу аналізу
- •Апаратурне оснащення поляриметричного методу
- •Застосування поляриметричного методу аналізу
- •Лабораторна робота ідентифікація речовини за величиною питомого обертання
- •План експерименту
- •Контрольні питання
- •Глава 9. Хроматографічні методи аналізу
- •9.1. Теоретичні основи методу
- •Класифікація хроматографічних методів
- •9.2. Хроматографія в тонкому шарі сорбенту (тонкошарова хроматографія)
- •Етапи проведення аналізу методом тшх
- •6 . Проведення кількісного аналізу
- •Якісний аналіз барвників у суміші методом тонкошарової хроматографії
- •План експерименту
- •9.3. Іонообмінна хроматографія
- •Лабораторна робота визначення концентрації натрій хлориду методом іонообмінної хроматографії
- •План експерименту
- •Додатки
- •Класифікація методів кількісного аналізу
- •Класифікація титриметричних методів аналізу за типом хімічної реакції, яка лежить в основі методу
- •Класифікація титриметричних методів аналізу за способом титрування
- •Кислотно-основне титрування
- •Методи окисно-відновного титрування
- •Перманганатометричне титрування
- •Йодометричне титрування
- •Нітритометричне титрування
- •Броматометричне титрування
- •Цериметричне титрування
- •Хроматометричне титрування
- •Аргентометричне титрування
- •Тіоціанатометричне титрування (за методом Фольгарда)
- •Меркурометричне титрування
- •Комплексонометричне титрування
- •Меркуриметричне титрування
- •Список цитованої літератури
- •Глава 1. Загальні положення. Класифікація гравіметричних методів ….…4
- •Глава 2. Основні положення титриметричного аналізу …………………...…30
- •Глава 3. Розрахунки в титриметричному аналізі
- •Глава 4. Метод кислотно – основного титрування
- •Глава 5. Методи окисно-відновного титрування
- •Глава 6. Методи осаджувального титрування
- •Глава 7. Методи комплексоноутворення
- •7.1. Теоретичні основи методу……………………………………………..…173
- •Глава 8. Оптичні методи аналізу
- •Глава 9. Хроматографічні методи аналізу
Лабораторна робота аналіз аскорбінової кислоти методом йодометрії
Мета: закріпити навички використання методу йодометрії в аналізі фармацевтичних препаратів.
Сутність методу: точно зважену на аналітичних терезах наважку аскорбінової кислоти розчиняють у дистильованій воді у конічній колбі та титрують стандартним розчином йоду в присутності індикатору – крохмалю.
Аналітичні прийоми: метод прямого титрування, метод окремих наважок.
Аскорбінова кислота
(Acidum ascorbicum)

γ–лактон 2,3–дегідро–L–гулонової кислоти
Хімізм процесу

М(1/2С6Н8О6) = 88,06 г/моль; fекв=1
План експерименту
Розрахунок маси наважки аскорбінової кислоти.
![]()
Вихідні дані: с( І2) = 0,1 моль/дм3 ; Vmin(І2) ~ 15 см3
![]()
Зважування наважки 0,15 г аскорбінової кислоти в бюксі на аналітичних терезах.
Результати зважування занести в лабораторний журнал:
1) mб з н = 2) mб з н = 3) mб з н =
mб = mб = mб =
mн. = mн. = mн. =
Розчинення наважки та підготовка до титрування.
Наважку розчинити у суміші 10 см3 кислоти сульфатної розведеної і 80 см3 дистильованої води. Додати 1 см3 розчину крохмалю.
4. Процес титрування.
Дослідний розчин титрувати стандартним розчином йоду до одержання стійкого синьо-фіолетового забарвлення. Результати титрування занести у таблицю:
-
1
2
3
mнав.(аск.к-ти), г
V(I2), см3
5. Розрахунок результатів аналізу.
5.1. Розрахунок титру відповідності:
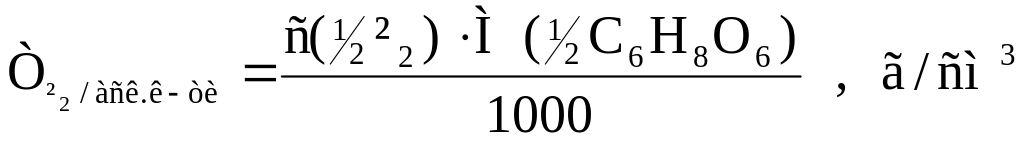
Розрахунок масової частки аскорбінової кислоти в досліджуваній субстанції:
![]()
Розрахунки проводять для кожної наважки
Розрахунок середнього результату:
![]()
6. Висновок.
Контрольні питання
Надати визначення методу йодометрії. Основна реакція методу. Визначити молярну масу еквівалента йоду.
Пояснити, чому для приготування розчинів йоду у воді додають калій йодид. Записати хімічну реакцію.
Визначення окисників методом йодометрії.
В чому полягає сутність аналітичного прийому – методу заміщення?
Записати хімічні реакції на прикладі аналізу КМnO4.
Пояснити, яким способом можна провести очищення кристалічного йоду.
Вказати особливості приготування та стандартизації розчину натрій тіосульфату.
Завдання для самостійної роботи
1. Обчислити масу наважки кристалогідрату натрій тіосульфату, що необхідна для приготування 500 см3 розчину з молярною концентрацією еквіваленту 0,05 моль/дм3 . (Відповідь: 6,2 г)
2. Обчислити масу наважки йоду (х.ч.), яка потрібна для приготування 250 см3 розчину з молярною концентрацією еквіваленту 0,1 моль/дм3. (Відповідь: 3,2 г)
3. Наважка йоду (х.ч.) масою 0,6300 г розчинена у мірній колбі об'ємом 500 см3. Обчислити титр розчину. (Відповідь: 0,001260 г/см3)
4. Наважка йоду (х.ч.) масою 1,2620 г розчинена в мірній колбі об'ємом 250 см3. Обчислити титр та молярну концентрацію еквіваленту йоду.
(Відповідь: 0,005048 г/см3, 0,03976 моль/дм3)
5. Наважка йоду (х.ч.) масою 6,3250 г розчинена у мірній колбі об'ємом 1 дм3. Обчислити молярну концентрацію еквіваленту йоду та титр йоду за кристалогідратом натрій тіосульфату.
(Відповідь:0,04982 моль/дм3; 0,01235 г/см3)
6. Обчислити масу наважки калій дихромату, що необхідна для стандартизації розчину натрій тіосульфату з молярною концентрацією еквіваленту ~ 0,1 моль/дм3, методом окремих наважок, якщо користуватися бюреткою об'ємом 50 см3. (Відповідь: 0,12 г)
7. Обчислити масу йоду в розчині, якщо на його титрування витрачено 20,00 см3 титранту з молярною концентрацією еквіваленту натрій тіосульфату 0,1040 моль/дм3. (Відповідь: 0,2640 г)
8. с(
І2)
= 0,1000 моль/дм3.
Визначити:![]() ;
масу йоду в 100 см3
розчину.
(Відповідь:
0,01269 г/см3;
1,269 г/100 см3)
;
масу йоду в 100 см3
розчину.
(Відповідь:
0,01269 г/см3;
1,269 г/100 см3)
9. На
титрування розчину аскорбінової кислоти
витрачено 10,00 см3
розчину йоду.
![]() =
0,008847 г/см3.
Визначити масу кислоти в розчині.
Записати хімічну реакцію.
(Відповідь: 0,08847 г).
=
0,008847 г/см3.
Визначити масу кислоти в розчині.
Записати хімічну реакцію.
(Відповідь: 0,08847 г).
10. с(
І2)
= 0,1 моль/дм3.
K = 1,037. Визначити:
;
![]() .
.
(Відповідь: 0,01316 г/см3; 0,03277 г/см3).
11. Наважка аскорбінової кислоти 0,1345 г розчинена у воді і відтитрована стандартним розчином йоду. = 0,00882 6г/см3. На титрування пішло 15,00 см3 розчину йоду. Визначити масову частку кислоти в наважці. Записати хімічну реакцію. Вказати індикатор. (Відповідь: 98,43%)
12. Наважка аскорбінової кислоти 0,1445 г розчинена у воді і відтитрована стандартним розчином йоду (с( І2) = 0,1 моль/дм3, К = 0,9735). На титрування було витрачено 16,70 см3 розчину йоду. Визначити масову частку кислоти в наважці. Вказати індикатор. (Відповідь: 99,07%)
13.Обчислити масу йоду в розчині, якщо на його титрування витрачено 10,12 см3 титранту натрій тіосульфату, титр якого становить 0,02318 г/см3. (Відповідь: 0,1199 г)
14. Обчислити титр натрій тіосульфату за йодом, якщо титр натрій тіосульфату становить 0,01204 г/см3. (Відповідь: 0,006156 г/см3)
15. Обчислити титр йоду за натрій тіосульфатом, якщо молярна концентрація еквіваленту йоду 0,1 моль/дм3 (К=0,9630). (Відповідь: 0,02390 г/см3)
16. Обчислити масу йоду, якщо на його титрування витрачено 19,08 см3 титранту натрій тіосульфату, титр натрій тіосульфату за йодом 0,01230 г/см3. (Відповідь: 0,2347 г)
17. Наважка калій дихромату (х.ч.) масою 1,1780 г розчинена в мірній колбі об'ємом 250 см3. На титрування 25,00 см3 цього розчину (після відповідної обробки) витрачено 23,38 см3 розчину натрій тіосульфату. Обчислити молярну концентрацію еквіваленту та коефіцієнт поправки розчину натрій тіосульфату. (Відповідь: 0,1028 моль/дм3; 1,028 до 0,1)
18. Наважка калій дихромату (х.ч.) масою 0,2486 г розчинена в мірній колбі об'ємом 500 см3. На титрування 25,00 см3 цього розчину (після відповідної обробки) витрачено 25,05 см3 розчину натрій тіосульфату. Обчислити титр, молярну концентрацію еквіваленту натрій тіосульфату та коефіцієнт поправки. (Відповідь: 0,02512 г/см3; 0,1012 моль/дм3; 1,012 до 0,1)
19. Наважка калій дихромату (х.ч.) масою 0,1180 г оброблена у кислому середовищі калій йодидом та відтитрована розчином натрій тіосульфату, якого витрачено 23,80 см3. Обчислити титр розчину натрій тіосульфату. (Відповідь: 0,02510 г/см3)
20. Наважка калій дихромату (х.ч.) масою 0,1154 г оброблена у кислому середовищі калій йодидом та відтитрована розчином натрій тіосульфату, якого витрачено 23,74 см3. Обчислити титр натрій тіосульфату, титр відповідності натрій тіосульфату за йодом. (Відповідь: 0,02461 г/см3; 0,01258 г/см3)
21. Для аналізу натрій тіосульфату на вміст основного продукту взяли наважку масою 15,9800 г та розчинили у мірній колбі об'ємом 500 см3. На титрування 25,00 см3 цього розчину витрачено 30,60 см3 титранту йоду з молярною концентрацією еквіваленту 0,1 моль/дм3 (К = 0,9780). Обчислити масову частку Nа2S2О3·5Н2О у зразку. (Відповідь: 92,96%)
22. Наважка натрій тіосульфату масою 1,4460 г розчинена у мірній колбі об'ємом 500 см3. На титрування 20,00 см3 одержаного розчину витрачено 22,15 см3 титранту йоду з молярною концентрацією еквіваленту 0,01 моль/дм3 (К = 1,0250). Обчислити масову частку Nа2S2О3·5Н2О у зразку. (Відповідь: 97,43%)
23. Для аналізу йоду, що містить нерозчинні домішки, взяли наважку масою 1,6220 г та розчинили в мірній колбі об'ємом 250 см3. На титрування 25,00 см3 цього розчину витратили 19,95 см3 розчину з молярною концентрацією еквіваленту натрій тіосульфату 0,05 моль/дм3 (К = 1,0500). Обчислити масову частку йоду у зразку. (Відповідь: 81,94%)
24. Наважка мідного купоросу масою 2,9984 г розчинена в мірній колбі об'ємом 250 см3. На титрування 10,00 см3 цього розчину (після відповідної обробки) витрачено 9,15 см3 титранту з молярною концентрацією еквіваленту натрій тіосульфату 0,04900 моль/дм3. Обчислити масову частку CuSO4·5H2O у зразку. (Відповідь: 93,34%)
25. Наважка мідного купоросу масою 10,6007 г розчинена в мірній колбі об'ємом 500 см3. На титрування 25,00 см3 цього розчину (після відповідної обробки) витрачено 23,17 см3 титранту з молярною концентрацією еквіваленту натрій тіосульфату 0,09150 моль/дм3. Обчислити масову частку CuSO4·5H2O у зразку. (Відповідь: 99,88%)
