
- •Государственное издательство медицинской литературы Ленинград
- •Работа в операционной
- •Остановка кровотечения
- •Перевязка задней больше-берцовой артерии (a. Tibialis posterior)
- •Переливание крови,
- •Подготовка аппаратуры
- •Техника вливания растворов
- •Ее годности
- •Внутривенное переливание крови
- •Пересадка кожи
- •Операции на конечностях
- •Эмболэктомия
- •Ранний вторичный шов сухожилий
- •Повреждения ахиллова сухожилия
- •Операции на нервных стволах
- •Разрезы при флегмонах кисти
- •Разрезы при флегмонах бедра
- •Разрезы при флегмонах стопы
- •Ампутации и вычленения стопы
- •Ампутация голени
- •Ампутация бедра
- •Артротомия
- •Резекция суставов
- •Операции на плечевом суставе
- •Операции на локтевом суставе
- •Открытые переломы черепа
- •Закрытые переломы черепа
- •Внутричерепные кровоизлияния
- •12 Н. И. Блинов 177
- •Операции на лице
- •1, 2, 3 И 4 — линии разреза вдоль периферических ветвей лицевого нерва.
- •1, 2, 3 И 4 —линии разреза.
- •Операции на шее
- •Нижняя трахеостомия
- •Обнажение пищевода на шее
- •Операции на молочной железе Разрезы
- •Края раны разведены крючками (1) и обнажены молочная железа и большая грудная мышца (2). Пунктиром очерчен сектор (3) молочной железы с удаляемой опухолью (4).
- •Третий этап операции.
- •Прокол плевры
- •Резекция ребра
- •Приемнике создается вакуум благодаря оттоку воды из сосуда (2) в сосуд (3).
- •Торакотомия
- •Кишечный шов
- •Операции на тонкой кишке Резекция тонкой кишки
- •Наложение свища тонкой кишки
- •Еюностомия
- •Илеостомия
- •Энтеростомия
- •Операции на желудке
- •Гастростомия по способу Витцеля
- •Гастротомия по способу Кадера
- •И тощей кишкой
- •Стенку желудка
- •К брыжейке поперечно-ободочной кишки (по а. А. Русанову).
- •Особенности резекции желудка при раке
- •Операции при аппендиците
- •Дьяконову
- •Прохода
- •Наложение калового свища
- •Закрытие каловых свищей
- •Операции на прямой кишке Оперативное лечение выпадения прямой кишки Оперативное лечение выпадения слизистой оболочки прямой кишки
- •Операция по способу а. Г. Радзиевского
- •Повреждения прямой кишки
- •Заворот тонкого кишечника
- •Заворот слепой кишки
- •Инвагинация
- •Узлообразование
- •Обтурационная непроходимость
- •Закрытие свища на слепой кишке
- •Операции при абсцессах печени
- •Холедохотомия
- •Холецистостомия
- •Шов на селезенке
- •Удаление селезенки
- •Экстирпация кист
- •Марсупиализация кисты
- •Наложение внутреннего дренажа
- •Способ Бассини
- •Бедренный доступ (способ Шварца)
- •Тораколапаротомия
- •Метод облитерации плевральных листков
- •Параплевральный доступ
- •Абсцесса.
- •Вскрытие забрюшинного пространства
- •Катетеризация
- •Промывание мочевого пузыря
- •Цистотомия
- •Закрытие пузырного свища
- •Операция фимоза
- •Парафимоз
- •Наружная уретротомия
- •Кастрация
- •Нефрэктомия
- •Повреждения мочевого пузыря
- •Разрывы уретры
- •Паранефрит
- •Методика вмешательства
Техника вливания растворов
Большая часть растворов может вводиться подкожно, внутримышечно, внутривенно и в виде капельных клизм в прямую кишку.

Растворы, содержащие спирт, нельзя вводить подкожно. Подкожно раствор вводится иногда с помощью аппарата Боброва. Не следует вводить одновременно в один участок тела более 500 мл раствора, вливание большего количества раствора может вызвать некроз кожи.
Рис. 27. Сифонная система для вливания растворов и переливания крови.
1 — сифонная трубка длиной 20 см; 2 — резиновая соединительная трубка длиной 60 см; 3 –игла; 4 — резиновая соединительная трубка длиной 10 см; 5 —стеклянная соединительная трубка длиной 5 см.
Удобнее всего раствор подкожно и внутримышечно вводить капельным путем. В этом случае раствор поступает в организм в течение нескольких часов. Таким путем в один участок тела возможно вливать до 1,5 л раствора (обычно перед-ненаружная поверхность бедра). Медленно поступающий раствор всасывается, не образуя скоплений в области вливаемого участка.
Для введения раствора капельным способом
удобнее всего пользоваться сифоном (рис. 27). На короткий конец сифонной трубки надевается резиновая длиною 80–100 см, на другой конец которой надевается игла. Сосуд с раствором в количестве 1 –1,5 л ставится на подставку около кровати боль-
51
ного на высоту 70—80 см. В сосуд вставляется сифонная трубка. Отверстие сосуда закрывается стерильным марлевым шариком; вся система сифона заполняется раствором или с помощью шприца через нижний конец резиновой трубки, или путем постепенного выжимания пальцами воздуха из резиновой трубки. Когда из иглы начинает вытекать раствор, она вкалывается подкожно или внутримышечно. Поднимая на различный уро-
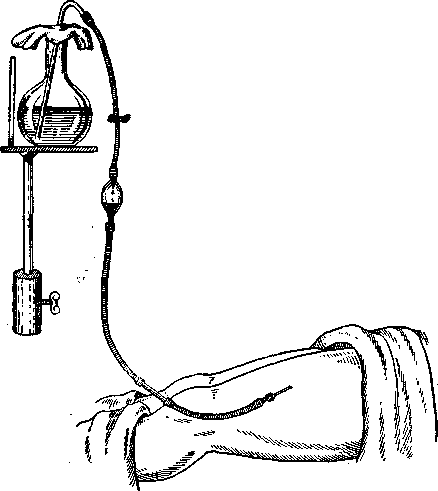
Рис. 28. Введение раствора под кожу капельным способом с помощью сифона.
вень сосуд с раствором, регулируют быстроту введения раствора. В резиновую трубку можно вставить капельницу, тогда быстрота поступления раствора регулируется количеством капель, поступающих в капельницу в 1 мин (рис. 28).
Таким же образом можно ставить и капельные клизмы. В этом случае на нижний конец системы надевается наконечник, который употребляется для постановки обычной клизмы; наконечник вводится в прямую кишку, и раствор поступает туда с определенной скоростью, которая регулируется или высотой поднятия сосуда, или количеством капель, падающих в капельнице.
Перед тем как поставить капельную клизму, необходимо очистить кишечник обыкновенной клизмой, кал в ампуле прямой кишки препятствует поступлению жидкости в прямую кишку.
52
Хранение, перевозка консервированной крови и определение
Ее годности
Консервированная кровь должна храниться в леднике при температуре от +2 до +8°. Необходимо стремиться к тому, чтобы температура была постоянной, резкие колебания температуры могут неблагоприятно действовать на консервированную кровь. В леднике, где хранится кровь, могут находиться только антибиотики и сыворотки. Категорически воспрещается вместе с кровью хранить продукты питания.
При отсутствии специального ледника кровь разрешается хранить в подвалах (в холодное время года) или в специально устроенных ямах или колодце (в теплое время года). Кровь должна находиться в специальных ящиках, запертых на замок и желательно запломбированных. При необходимости из ящика берется нужное количество крови, и ящик снова закрывается.
Ампулы с кровью желательно хранить в вертикальном положении, при нем удобнее определять видимые показатели годности консервированной крови.
При транспортировке необходимо позаботиться о том, чтобы консервированная кровь не подвергалась взбалтыванию, что может отрицательно отразиться на ее качестве. В очень холодное время года нужно перевозить кровь в отепленных (изотермических) ящиках для предохранения ее от замерзания, при перевозке в жаркое время года также следует пользоваться изотермическими ящиками. Если кровь перевозится на небольшое расстояние, то вынутые из ледника ампулы или банки с кровью можно обвернуть большим слоем ваты, чтобы сохранить низкую температуру.
Определение годности консервированной крови производится по так называемым видимым показателям крови. При стоянии в том или ином сосуде консервированная кровь разделяется на два слоя: нижний слой – эритроциты, верхний слой – плазма, на поверхности эритроцитов располагается тонкая серая пленка – лейкоциты (чаще бывает не пленка, а серые пятна, разбросанные по поверхности эритроцитов). Нижний слой эритроцитов имеет темно-вишневую окраску, верхний слой плазмы имеет светло-желтый, иногда зеленовато-желтый цвет.
Иногда в первые дни консервации слой плазмы может быть мутноватым от содержащегося в ней жира. На 4–5-й день стояния консервированной крови обычно жир собирается в виде тонкой пленки наверху плазмы и плазма делается прозрачной.
В консервированной крови, годной для переливания, должна наблюдаться резкая граница между слоем эритроцитов и слоем плазмы. Плазма должна быть прозрачная, в ней не должно быть мути, хлопьев и каких-либо пленок.
53
Консервированная кровь считается непригодной: 1) если между слоями плазмы и эритроцитов появляется розовый ободок, указывающий на наличие гемолиза в крови; 2) если плазма делается мутной, в ней появляются хлопья и нити фибрина, что бывает при бактериальном загрязнении крови.
Наличие тонкой серой пленки сверху плазмы еще не указывает на непригодность консервированной крови. Пленка может представлять собой слой жира, собравшийся наверху. Для выяснения этого следует, не перемешивая кровь перед переливанием, слегка ее подогреть, до 20–25°; жировая пленка при этом обычно расходится.
Подогретую кровь нельзя снова ставить в ледник, после подогревания кровь надо сразу употреблять. Точно так же открытая кровь должна сразу вся переливаться, оставлять ее в леднике и через некоторое время переливать нельзя.
Перед переливанием крови всегда необходимо смотреть на этикетке дату заготовки и группу крови.
Срок годности консервированной крови, приготовленной только на растворе лимоннокислого натрия, определяется в среднем 15 дней. Если для консервации употреблялся глюкозо-цитратный раствор, то срок годности удлиняется до 20–25 дней. Поэтому при получении консервированной крови со станции, заготавливающей кровь, всегда надо интересоваться средой, на которой законсервирована кровь, и выяснять возможный срок ее хранения.
Если переливания крови в лечебном учреждении производятся довольно часто, то в запасе можно держать кровь трех групп: О, А и В. Если переливания крови производятся нечасто, то целесообразно держать только кровь нулевой группы, т. е. универсального донора.
Если в лечебное заведение доставка консервированной крови затруднительна, то хирургу необходимо позаботиться о наборе донорских кадров из местного населения. По созданию донорских кадров имеются специальные инструкции на станциях переливания крови, ими и надо пользоваться.
Определение групповой принадлежности крови
Перед переливанием крови необходимо определить группу крови больного и затем подобрать ему совместимую кровь.
Определение групповой принадлежности производится с помощью стандартных сывороток. Обычно применяются сыворотки трех групп: группы 0, группы А и группы В.
Для определения группы крови необходимо иметь:
1. Ампулы со стандартными сыворотками двух различных серий.
54
Четыре пипетки, по одной пипетки для каждой сыворотки и одна для крови.
Четыре стеклянных пробирки для хранения пипеток.
Три стеклянные палочки.
Иглу Франка.
Вату, спирт, физиологический раствор.
Четыре-пять предметных стекол.
Удобнее всего указанные предметы держать в специальном ящичке, который должен находиться в операционной, чтобы хирург в любой момент мог иметь под руками все необходимое для определения групповой принадлежности. В дополнение к указанному крайне желательно иметь еще одну или две обыкновенные мелкие тарелки.
Палец, из которого будет взята кровь, тщательно обтирается спиртом, затем спиртом же обтирается острие иглы Франка, на тарелку наносят стандартные сыворотки.
Из ампулы с сывороткой группы 0 пипеткой набирается сыворотка, и одна – две большие капли ее наносятся на верхнюю часть тарелки, где предварительно чернилами или лучше восковым карандашом можно поставить 0. При отсутствии тарелки сыворотка наносится на левый край предметного стекла, после чего пипетка тотчас же обратно опускается в свою пробирку. Таким же образом поступают с сывороткой группы А и с сывороткой группы В, причем сыворотку группы А наносят на левую сторону тарелки, а сыворотку группы В – на правую. На предметном стекле сыворотка А будет посредине, сыворотка В – справа. При работе с подкрашенными сыворотками по окраске всегда можно установить, где имеется сыворотка А и В. Категорически воспрещается одновременно двумя руками наносить сыворотку двух групп, во избежание перепутывания пипеток. Точно так же не рекомендуется наносить сыворотку сразу для нескольких определений, так как сыворотка может подсохнуть, что послужит причиной ошибки.
После этого делается укол в мякоть пальца и выжимается капля крови. Острие иглы и палец должны быть сухими; если после укола палец будет еще влажным от спирта, то перед выжиманием крови необходимо палец обтереть сухим ватным шариком.
Кровь с пальца набирается в пипетку и наносится в виде небольших капель, величиной с булавочную головку, около каждой капли стандартной сыворотки, и, кроме того, на тарелку наносится еще четвертая, более крупная капля крови. Эта капля в дальнейшем используется для контроля.
Чтобы получить маленькую каплю крови, не надо капать кровь свободной каплей, а необходимо кончик пипетки плотно приставить к стеклу или тарелке и осторожно выдавливать кровь из пипетки, после чего с помощью чистой стеклянной
55
палочки производится смешивание капли крови с сывороткой каждой группы; смешивание производится до тех пор, пока смесь не примет равномерный розовый цвет. После смешивания крови с сывороткой какой-либо группы палочка должна быть обмыта физиологическим раствором и тщательно обтерта для того, чтобы сыворотку одной группы не перенести в каплю с сывороткой другой группы. Смешивание сыворотки с кровью можно произвести легким ударом по краю тарелки с последующим покачиванием тарелки.
Можно снимать кровь с пальца четырьмя углами предметного стекла, каждый угол стекла погрузить в каплю соответствующей стандартной сыворотки и им произвести смешивание крови с сывороткой; точно так же можно снимать кровь и стеклянными палочками и ими же производить смешивание. Заметив на часах время, наблюдают наступление агглютинации, покачивая тарелку или предметное стекло в течение 1–2 мин.
Место укола пальца исследуемого прикрывается небольшим ватным шариком, смоченным спиртом.
Нужно иметь в виду, что агглютинация будет четкой только при определенных соотношениях сыворотки и эритроцитов.
Если производится реакция на стекле или тарелке, то нужно помнить основное правило: сыворотки брать больше, эритроцитов – меньше. Капля эритроцитов цельной крови должна быть в 10–15 раз меньше капли стандартной сыворотки. Только в этом случае реакция будет четкой и не вызовет никаких недоразумений. Если же сыворотки берется недостаточно, то часть эритроцитов может извлечь полностью агглютинин сыворотки, а вторая часть, не вступая в реакцию, будет мешать последней, почему агглютинация делается неясной, а может быть, и совсем незаметной, что, естественно, приведет к ошибке. Агглютинация обычно появляется в течение 25–30 сек и к концу второй минуты бывает довольно четкой. Если агглютинация не наступает в течение 5 мин, то реакцию нужно считать отрицательной.
Чтобы лучше наблюдать реакцию на предметных стеклах, необходимо под них положить лист бумаги, на белом фоне агглютинация видна отчетливее, вместо обычных стекол лучше пользоваться матовыми и брать стекла большего размера – 10 X 10 см.
При оценке результатов следует в первую очередь обращать внимание на сыворотку группы 0, которая является контрольной.
Если в нулевой сыворотке наступила агглютинация, то она обязательно должна наступить или в сыворотке А, или в сыворотке В, или в той и другой, так как в нулевой оба агглютинина, а и р, имеются вместе, а в остальных двух сыворотках эти же агглютинины находятся по отдельности. Если же нулевая
56
сыворотка не дает агглютинации, то агглютинации не должно быть и в других сыворотках и эритроциты будут принадлежать к нулевой группе. Схема реакции с тремя стандартными сыворотками представлена на рис. 29.
При получении реакции, не соответствующей данной схеме, т. е. если, например, агглютинация будет только с какой-либо

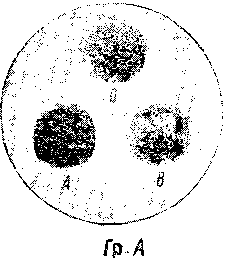

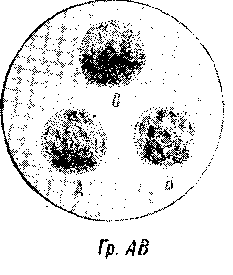
Рис. 29. Схема определения группы крови по трем стандартным сывороткам.
одной сывороткой, можно определенно говорить о какой-то технической ошибке и реакцию нужно переделать сначала с теми же сыворотками, а при получении идентичных результатов — с сыворотками других серий.
Из приведенного рис. 29 видны четыре возможные комбинации: а) если все три сыворотки дают положительные реакции, то испытуемая кровь относится к группе АВ (IV), так как ее эритроциты агглютинируются и с агглютинином α, находящимся в сыворотке группы В, и с агглютинином β,
57
находящимся в сыворотке группы А; б) когда сыворотка группы А дает отрицательную реакцию, а сыворотки групп 0 и В дают положительную реакцию, то испытуемая кровь принадлежит к группе А; если эритроциты исследуемой крови не агглютинируются сывороткой А, содержащей агглютинин β, то значит в них отсутствует фактор В и они относятся к группе А; в) когда сыворотка группы В дает отрицательную реакцию, а сыворотки групп 0 и А — положительную, то испытуемая кровь относится к группе В, так как если исследуемые эритроциты не дают агглютинации с сывороткой группы В, содержащей агглютинин а, то в этих эритроцитах отсутствует агглюти-ноген А и они принадлежат к группе В; г) если все три сыворотки дают реакцию отрицательную, т. е. все капли смеси остались равномерно окрашенными в розовый цвет, испытуемая кровь принадлежит к группе 0, исследуемые эритроциты не вступают в агглютинацию ни с одним агглютинином, т. е. они не содержат ни одного агглютиногена.
Наиболее точным будет метод двойной реакции. Групповая принадлежность определяется одновременно по стандартным сывороткам и по стандартным эритроцитам. Этим методом сразу определяется в крови содержание агглютиногенов и агглютининов, т. е. выясняется полная формула крови, но к этой реакции прибегать не приходится, так как для ее производства необходимо иметь стандартные эритроциты групп А и В.
При затруднении в определении группы крови больного для переливания всегда можно воспользоваться кровью универсального донора.
Установив групповую принадлежность больного, подбирают ему или кровь одноименной группы, или кровь универсального донора. Больному группы АВ можно переливать кровь любой группы. Чтобы убедиться в совместимости вливаемой крови •с кровью реципиента, производится проба на индивидуальную -совместимость.
Наилучшей пробой является следующая: к капле сыворотки больного прибавляют каплю вливаемой крови, при этом никакой агглютинации наступить не должно. Если наступает агглютинация, то переливать кровь нельзя.
Однако не всегда удается быстро получить сыворотку у больного, обычно для этого необходима центрифуга. Можно заранее взять кровь у больного в стерильную пробирку, дать ей свернуться и образовавшуюся сыворотку использовать для пробы на совместимость.
В практике переливания крови чаще пользуются так называемой прямой пробой, а именно: к небольшой капле консервированной крови, нанесенной на тарелку, добавляется большая капля крови больного. Обе капли тщательно перемешивают
58
и ожидают наступления агглютинации в течение 5 мин. Агглютинации быть не должно. Если при этом наступает агглютинация, то переливание данной крови делать нельзя.
Необходимо твердо помнить, что прямую пробу на совместимость можно производить только при переливании одноименной группы, т. е. когда предполагается, что кровь донора и реципиента принадлежит к одной группе. При переливании же крови от универсального донора или универсальному реципиенту, т. е. при переливании крови разноименных групп, эту пробу производить нельзя.
При смешении крови разных групп всегда наступает агглютинация. Если смешивается кровь группы 0 с кровью какой-либо другой группы, то агглютинины сыворотки нулевой группы а и р обязательно дадут агглютинацию с эритроцитами других групп, а переливать кровь нулевой группы возможно реципиентам всех групп.
Если у врача возникает подозрение на возможность возникновения в сыворотке реципиента антирезус-агглютинина, то он обязательно должен это проверить, но лучше это делать всегда при переливании крови. Подозрение на наличие антирезус-агглютинина может возникнуть в тех случаях, когда у женщины-реципиента имеется соответствующий акушерский анамнез (гемолитическая болезнь новорожденных) или в анамнезе существуют указания на наличие осложнений при повторных переливаниях крови.
Во всех этих случаях крайне необходимо для производства пробы на совместимость брать обязательно сыворотку реципиента, а не кровь.
На чашку Петри наносят две капли сыворотки и к ним добавляют одну небольшую каплю вливаемой крови. Чашку Петри опускают в сосуд с теплой водой, где она плавает, и наблюдают наступление агглютинации в течение 10 мин; температура воды должна быть 42–45° (рис. 30).
Если агглютинация не наступает в течение 10 мин, то проба показывает или отсутствие антирезус-агглютининов в сыворотке реципиента или отсутствие резус-фактора во вливаемых эритроцитах; как в том, так и в другом случае переливание крови возможно производить. Если же наступает агглютинация, то переливать кровь нельзя.
Правильное определение групповой принадлежности и проба на совместимость гарантируют от возможных осложнений при переливании крови. Этими пробами определяется соотношение крови донора и реципиента в пробирке. Но перед переливанием крови всегда необходимо сделать еще и пробу в организме.
Для определения совместимости крови в групповом отношении в организме существует биологическая проба. Проводится она следующим способом. После быстрого введения 25 мл
59
крови переливание крови на 2–3 мин прекращают. Врач наблюдает за состоянием реципиента. Если нет признаков несовместимости переливаемой крови, переливание продолжают. После введения дополнительной порции 25 мл крови вновь прекращают переливание на 2–3 мин. Затем, после введения следующих 25 мл, делают третий перерыв на 2–3 мин. При отсутствии симптомов несовместимости допускается переливание остального количества крови.
Первыми признаками биологической несовместимости крови являются беспокойство больного, покраснение лица, усиление

Рис. 30. Определение резус-фактора в эритроцитах.
инъекции сосудов конъюнктивы глаз, мелькание в глазах, чувство стеснения в груди, затруднение дыхания и очень часто кашель. Эти симптомы при быстром введении крови обычно появляются через 2–3 мин. Они постепенно начинают нарастать, к ним присоединяются боли в груди, под ложечкой и в пояснице. Возникшие в пояснице боли доминируют над прочими явлениями. Больной начинает вести себя крайне беспокойно, жалуется на резкие боли в пояснице. Указанные симптомы явно говорят о несовместимости крови. Вливание этой крови обязательно прекратить.
Для правильного проведения биологической пробы необходимо вводить первые 25 мл крови максимально быстро в течение 15—20 сек, тогда все симптомы несовместимости проявляются довольно четко. Если первая порция крови вводится медленно, то при пониженной реактивности организма симптомы несовместимости будут нечеткими и это может ввести в заблуждение врача, переливающего кровь. Однако при введении второй порции крови симптомы несовместимости обязательно выявятся.
60
