
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
2.3.2. Вращательные уровни энергии сферического волчка.
У молекул типа сферического волчка три главных момента инерции равны: IA = IB = IC . У них эллипсоид поляризуемости представляет собой сферу и отсутствует дипольный момент, поэтому они не активны в ИК- и КР-спектрах и представляют только теоретический интерес.
Однако имеется одно существенное различие молекул типа сферического волчка от линейных молекул, рассмотренных в п. 2.1, которое заключается в числе вращательных степеней свободы. Последнее будет проявляться в степени вырождения вращательных уровней энергии. Вращательные уровни молекул типа сферического волчка легко можно найти, если записать классическое выражение для энергии вращения молекулы с тремя моментами инерции, отличными от нуля. Это выражение будет иметь вид:
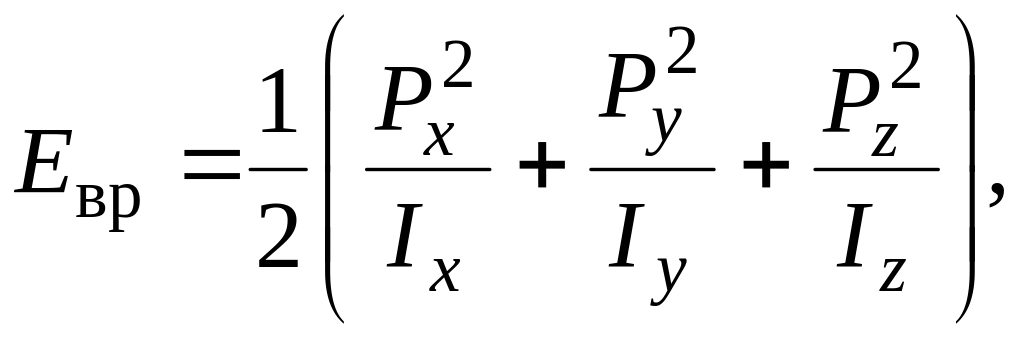 (2.34)
(2.34)
где
![]() – составляющие
механического момента по подвижным
осям, за которые выбираются главные оси
инерции, а IA
, IB
, IC
– соответствующие моменты инерции
вокруг этих осей. Учитывая тот факт, что
для сферического волчка все три момента
инерции равны (IA = IB
= IC
), формулу (2.34) можно переписать следующим
образом:
– составляющие
механического момента по подвижным
осям, за которые выбираются главные оси
инерции, а IA
, IB
, IC
– соответствующие моменты инерции
вокруг этих осей. Учитывая тот факт, что
для сферического волчка все три момента
инерции равны (IA = IB
= IC
), формулу (2.34) можно переписать следующим
образом:
![]() (2.35)
(2.35)
где
![]() .
.
Учитывая затем квантование квадрата момента количества движения, формулу (2.35) перепишем иначе
![]() (2.36)
(2.36)
где
![]() ,
что совпадает с
из выражения (2.16). Таким образом,
вращательные уровни молекулы типа
сферического волчка определяются той
же формулой, что и вращательные уровни
двухатомной линейной молекулы.
Существенное различие имеется в числе
вращательных степеней свободы.
,
что совпадает с
из выражения (2.16). Таким образом,
вращательные уровни молекулы типа
сферического волчка определяются той
же формулой, что и вращательные уровни
двухатомной линейной молекулы.
Существенное различие имеется в числе
вращательных степеней свободы.
Для характеристики вращательного движения двухатомной молекулы достаточно было двух степеней свободы. для этого вводились два квантовых числа J и mJ, определяющих значения квадрата момента количества движения и проекции момента количества движения на одну из неподвижных в пространстве координатных осей.
Молекула типа сферического волчка, как и любая нелинейная молекула, будет иметь три вращательные степени свободы. Для полной характеристики ее вращательного движения необходимо задать три квантовых числа. Два ранее названных квантовых числа J и mJ сохраняют свой смысл, а скажем k, будет определять значение проекции момента количества движения на одну из подвижных координатных осей. Направление этих осей может быть выбрано произвольно, т. е., их можно выбрать совпадающими с направлением главных моментов инерции. Необходимо только, чтобы эти оси вращались вместе с молекулой. Проекция момента количества движения на подвижную ось, которую выбирают совпадающей с осью Z, квантуется совершенно так же, как и проекция на неподвижную ось, а именно
![]() ,
(2.37)
,
(2.37)
где k = J(J – 1), ..., 0 ,...–J + 1, –J, т. е. принимает 2J + 1 значений.
Так как энергия от квантового числа k не зависит, то получается дополнительное вырождение уровней энергии кратности 2J + 1. Это вырождение имеет место наряду с вырождением mJ кратности (2J + 1)2, т. е. вырождение сохраняется относительно проекций момента количества движения на подвижную и неподвижную оси координат. Общая степень вырождения уровней энергии молекул типа сферического волчка по mJ и k равна
![]() (2.38)
(2.38)
Для каждого вращательного числа J возможны 2J + 1 ориентации момента относительно неподвижных и 2J + 1 относительно подвижных осей, что и приводит к (2J + 1)2 возможным состояниям.
Как видим в п. 2.2, число молекул во вращательном состоянии с заданным значением J будет определяться формулой:
![]() (2.39)
(2.39)
Сравнивая формулы с формулой (2.39) и (2.21) видим, что для молекул типа сферического волчка большая их доля будет находиться на высоких вращательных уровнях, чем для линейных молекул с той же вращательной постоянной B и температурой Т. Например, для вращательного уровня J = 4 различие в статистических весах уровней энергии для линейной молекулы и молекулы типа сферического волчка равно 9, а для J = 10 это различие будет более 20. Эти различия принимаются во внимание и особенно существенны при термодинамических расчетах.
Чисто вращательные спектры имеют место лишь у молекул, которые только случайно (а не в силу высокой симметрии) являются сферическими волчками. В этом случае у них дипольный момент не обязательно равен нулю, а эллипсоид поляризуемости не должен быть сферой.
