
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
Глава 2. Вращательные спектры молекул
2.1. Вращение двухатомной молекулы. Классический случай
рассмотрим
двухатомную молекулу, состоящую из двух
ядер на некотором расстоянии
![]() ,
которое назовем равновесным, и обращающиеся
вокруг ядер электроны. Связь между
атомами в такой молекуле обусловлена
электрическими силами взаимодействия
между заряженными частицами (электронами
и ядрами). Несмотря на то, что двухатомная
молекула представляет собой некоторую
динамическую систему из движущихся
электронов и ядер, для простоты изучения
картины вращения рассмотрим ее упрощенную
модель. Согласно этой модели, молекула
представляется в виде жесткого
образования, по форме напоминающего
гимнастическую гантель
(см.
рис.2.1).
,
которое назовем равновесным, и обращающиеся
вокруг ядер электроны. Связь между
атомами в такой молекуле обусловлена
электрическими силами взаимодействия
между заряженными частицами (электронами
и ядрами). Несмотря на то, что двухатомная
молекула представляет собой некоторую
динамическую систему из движущихся
электронов и ядер, для простоты изучения
картины вращения рассмотрим ее упрощенную
модель. Согласно этой модели, молекула
представляется в виде жесткого
образования, по форме напоминающего
гимнастическую гантель
(см.
рис.2.1).

С
точки зрения вращения она представляет
собой жесткий ротатор (расстояние между
атомами
![]() постоянно).
Вращается указанная система вокруг
осей, проходящих через центр тяжести.
Общее число таких осей равно трем. Однако
вращение вокруг оси, проходящей через
ядра атомов, не приводит к изменению
энергий. Ядра считаются точечными, а
массой электронов по сравнению с массой
ядер пренебрегают, поэтому момент
инерции вокруг указанной оси равен
нулю. В двухатомной молекуле будем
учитывать две различные оси вращения
(OO1
и OO2),
перпендикулярные оси молекулы, т. е. две
вращательные степени свободы.
постоянно).
Вращается указанная система вокруг
осей, проходящих через центр тяжести.
Общее число таких осей равно трем. Однако
вращение вокруг оси, проходящей через
ядра атомов, не приводит к изменению
энергий. Ядра считаются точечными, а
массой электронов по сравнению с массой
ядер пренебрегают, поэтому момент
инерции вокруг указанной оси равен
нулю. В двухатомной молекуле будем
учитывать две различные оси вращения
(OO1
и OO2),
перпендикулярные оси молекулы, т. е. две
вращательные степени свободы.
Для описания движения построенной модели двухатомной молекулы как целого необходимо получить выражения ее кинетической (Т) и потенциальной (V) энергий для данного вида движения (вращения). зная выражения, составим уравнение движения и решим его. В результате получим значения координат как функций времени, т. е. законы движения рассматриваемой модели.
Поскольку,
для жесткого ротатора
![]() const
и потенциальная энергия V
= const,
которую можно положить равной 0,
тогда полная энергия Е
ротатора равна кинетической энергии
вращающихся масс m1
и m2
вокруг одной из осей
(OO1
или
OO2),
т. е.
const
и потенциальная энергия V
= const,
которую можно положить равной 0,
тогда полная энергия Е
ротатора равна кинетической энергии
вращающихся масс m1
и m2
вокруг одной из осей
(OO1
или
OO2),
т. е.
![]() (Е
= Т,
так как V
= 0) (2.1)
(Е
= Т,
так как V
= 0) (2.1)
где
![]() и
и
![]() – линейные скорости движения атомов,
находящихся на расстоянии r1
и r2
от оси вращения. Вводя вместо линейной
скорости угловую
(
– линейные скорости движения атомов,
находящихся на расстоянии r1
и r2
от оси вращения. Вводя вместо линейной
скорости угловую
(![]() и
и
![]() ),
выражение (2.1) можно переписать следующим
образом:
),
выражение (2.1) можно переписать следующим
образом:
![]() ,
(2.2)
,
(2.2)
где выражение в скобках есть сумма моментов инерции I1 и I2 вращающихся атомов относительно оси вращения, r1 и r2 – расстояния массы атомов от оси вращения.
Можно
показать, что
![]() ,
где
,
где
![]() –
приведенная
масса молекулы, а
–
приведенная
масса молекулы, а
![]() –
равновесное расстояние между атомами.
Предоставляем это проделать читателю.
–
равновесное расстояние между атомами.
Предоставляем это проделать читателю.
С учетом сказанного равенство (2.2) можно переписать следующим образом:
![]() , (2.3)
, (2.3)
где I – момент инерции двухатомной молекулы. Таким образом, кинетическая энергия вращающейся молекулы пропорциональна квадрату угловой скорости и является функцией температуры. Это свидетельствует о том, что молекула может вращаться с любой скоростью , определяемой температурой среды.
Поглощать
или испускать радиацию могут те молекулы,
у которых при вращении будет изменяться
дипольный момент. Известно, что дипольный
момент есть вектор. Он может изменяться
и по величине, и по направлению. Так как
расстояние между атомами в двухатомной
молекуле принимается постоянным (жесткий
ротатор),
то при
вращении молекулы дипольный момент
изменяется только по направлению.
Следовательно, поглощать или испускать
радиацию будут те молекулы, которые
обладают постоянным дипольным моментом.
К таким относятся все молекулы, состоящие
из неодинаковых атомов (например, СО
NO,
HCl
и др.). У них центр тяжести положительных
зарядов не совпадает с центром тяжести
отрицательных зарядов. Все бездипольные
молекулы, состоящие из одинаковых ядер,
не обладают чисто вращательными спектрами
поглощения и испускания. Эти молекулы
имеют достаточно высокую симметрию
(![]() ),
и у них центры
тяжести положительных и отрицательных
зарядов совпадают, т. е. отсутствует
дипольный момент.
),
и у них центры
тяжести положительных и отрицательных
зарядов совпадают, т. е. отсутствует
дипольный момент.
При комнатной температуре значительная часть молекул находится на сравнительно высоких (возбужденных) уровнях вращательной энергии. Распределены они по этим уровням в соответствии с законом Больцмана. Доля молекул, имеющих вращательную энергию в интервале от Евр до Евр + dЕвр, выражается формулой
![]() , (2.4)
, (2.4)
где dЕвр= Iврdвр с учетом выражения (2.3), А – некоторая постоянная величина.
Пусть полное число молекул в единице объема с любыми вращательными энергиями равно n0. Это же число молекул мы можем найти, пользуясь выражением (2.4), если проинтегрируем по всем вращательным энергиям от 0 до .
![]() , (2.5)
, (2.5)
откуда A = n0/kT.
С учетом постоянной А формулу (2.4) можно переписать следующим образом:
![]() . (2.6)
. (2.6)
Классическое распределение интенсивностей во вращательной полосе совпадет с распределением молекул по различным вращательным состояниям, определяемым формулой (2.6), и графически представлено на рис. 2.2.
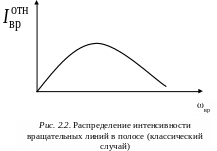
Так как по классической теории частоты вр могут изменяться непрерывно, то полоса должна быть сплошной.
