
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
Характеры приводимых представлений молекулы воды точечной группы симметрии с.
Операция симметрии |
I |
C2 |
|
2 |
Вид вращения |
Правильное |
Неправильное |
||
|
0° |
180° |
180° |
180° |
1 + 2cos |
3 |
–1 |
–1 |
–1 |
N(R) |
3 |
1 |
3 |
1 |
(R) = NR (1 + 2cos ) |
9 |
–1 |
3 |
1 |
t = (1 + 2cos ) |
3 |
–1 |
1 |
1 |
r = (1 + 2cos ) |
3 |
–1 |
–1 |
–1 |
= – t – r |
3 |
1 |
3 |
1 |
Примечание: t – трансляция, R – вращение, – колебание.
Зная совокупный характер колебательного представления (R) и пользуясь формулой (4.85) с учетом характеров неприводимых представлений группы симметрии С2, можно вычислить число возможных нормальных колебаний (n(i)) данного типа симметрии согласно формуле (4.84):
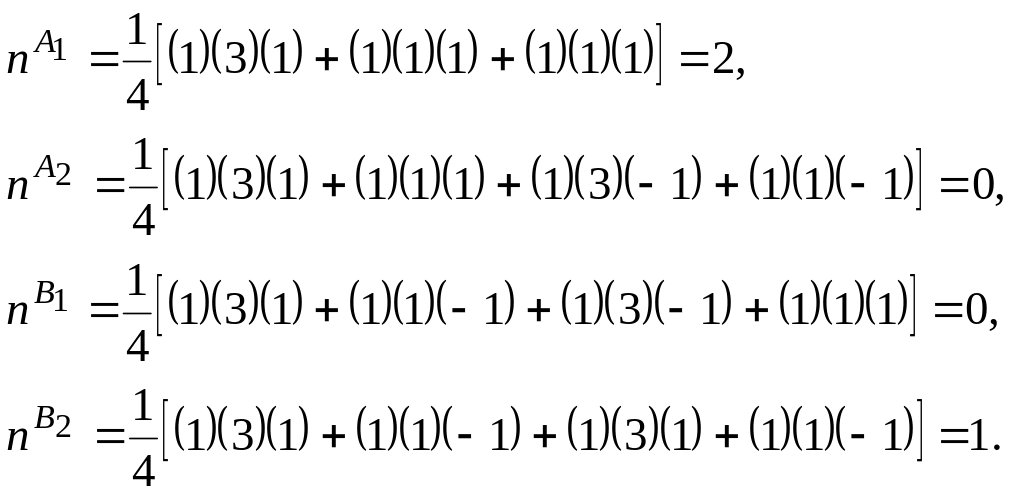
Таким образом, три колебания молекулы воды разбиваются на два колебания типа симметрии A1 и одно колебание В2.
Применим этот же метод к более сложной молекуле (например, бензола С6Н6). Молекула бензола C6H6 характеризуется тридцатью нормальными колебаниями (3N – 6), распределенными между двенадцатью типами симметрии (см. табл. 4.10).
Таблица 4.10
Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
Операция симметрии |
I |
2C6 |
2C3 |
C2 |
3C2' |
3C2 |
Вид вращения |
правильное |
|||||
φ |
0° |
60° |
120° |
180° |
180° |
180° |
1 + 2cos φ |
3 |
2 |
2 |
–1 |
–1 |
–1 |
N(R) |
12 |
0 |
0 |
0 |
4 |
0 |
= NR (1 + 2cos φ) |
36 |
0 |
0 |
0 |
–4 |
0 |
t= (1 +2cos φ) |
3 |
2 |
0 |
–1 |
–1 |
–1 |
r= (1 + 2cos φ) |
3 |
2 |
0 |
–1 |
–1 |
–1 |
= – t – r |
30 |
–4 |
0 |
2 |
–2 |
2 |
|
||||||
Операция симметрии |
i |
2S3 |
2S6 |
h |
3d |
3 |
Вид вращения |
неправильное |
|||||
φ |
0° |
60° |
120° |
180° |
180° |
180° |
1 + 2cos φ |
3 |
2 |
0 |
–1 |
–1 |
–1 |
N(R) |
0 |
0 |
0 |
12 |
0 |
4 |
= NR (1 + 2cos φ) |
0 |
0 |
0 |
12 |
0 |
4 |
t = (1 + 2cos φ) |
–3 |
–2 |
0 |
1 |
1 |
1 |
r = (1 + 2cos φ) |
3 |
2 |
0 |
–1 |
–1 |
–1 |
= – t – r |
0 |
0 |
0 |
12 |
0 |
4 |
Применяя формулу (4.84), получим:
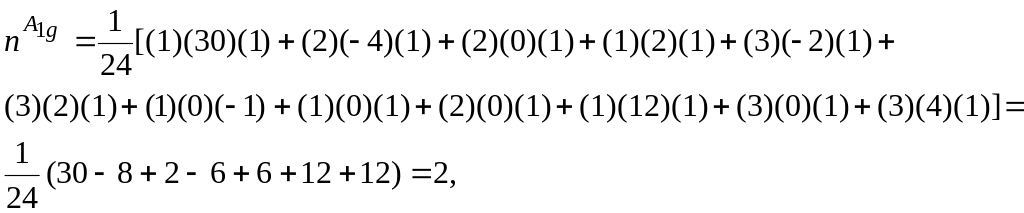 ...
... ... ... ... ... ... ... ... ... .... ... ... ... ... ...
... ... ... ... ... ... ...
...
... ... ... ... ... ... ... ... ... .... ... ... ... ... ...
... ... ... ... ... ... ...
...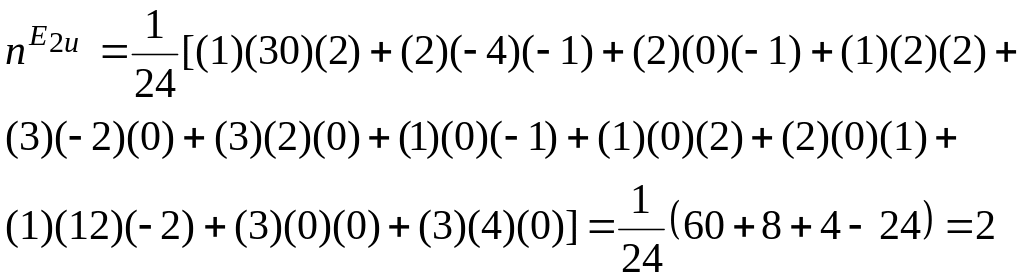
В результате все тридцать колебаний молекулы бензола распределяются между следующими типами симметрии:
Гv = 2A1g + A2g + 2B2g + E1 g + 4E2g + A2u + 2B1u + 2B2u + 3E1u + 2E2u.
знание только симметрии молекулы позволяет сравнительно простым расчетом определить число колебаний того или иного типа симметрии.
Аналогичное распределение колебаний по типам симметрии можно получить, решив колебательную задачу для молекулы на ЭВМ, однако это потребовало бы намного больших усилий и затрат времени. Для сравнения расчетных значений частот колебаний молекулы бензола с экспериментальными (см. табл. 4.11).
Таблица 4.11
