
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
4.2. Колебания многоатомной молекулы в классическом случае
Для описания движений атомов в молекуле в классической теории пользуются представлением смещения атомов в молекуле, при которых силы, возвращающие атомы в состояние равновесия, пропорциональны величинам смещений и направлены в сторону равновесного положения. Согласно законам механики, система в этом случае совершает гармонические колебания.
В качестве величин, определяющих смещение атомов в молекуле от равновесных положений, вводят n независимых параметров (колебательных координат) q1, q2 ,,... , qn, характеризующих изменения межъядерных расстояний и валентных углов по отношению к состоянию равновесия, т. е. q1 = r1 – r1e, q2 = r2 – r2e, ...qn – qne, где re означает равновесное положение данного атома; значок n пробегает все колебательные степени свободы молекулы.
Кинетическая Т и потенциальная V энергии молекулы при малых колебаниях выражаются через колебательные координаты следующим образом
![]() ,
(4.1)
,
(4.1)
![]() ,
(4.2)
,
(4.2)
где
![]() и
и![]() – скорости движения атомов; qi
и qk
величины смещений iго
и k-го
атомов из положения равновесия; Aik
– величина,
зависящая от масс колеблющихся атомов
и их расположения в пространстве
(кинематические коэффициенты); Kik
– квазиупругая постоянная, возникающая
при изменении положения i-го
и k-го
–
атомов; значки
i
и k
независимо принимают значения от единицы
до n
(число колебательных степеней свободы).
Величины Аik
являются симметричными по индексам,
так как они служат коэффициентами перед
численно равными величинами qiqk
и qkqi
– скорости движения атомов; qi
и qk
величины смещений iго
и k-го
атомов из положения равновесия; Aik
– величина,
зависящая от масс колеблющихся атомов
и их расположения в пространстве
(кинематические коэффициенты); Kik
– квазиупругая постоянная, возникающая
при изменении положения i-го
и k-го
–
атомов; значки
i
и k
независимо принимают значения от единицы
до n
(число колебательных степеней свободы).
Величины Аik
являются симметричными по индексам,
так как они служат коэффициентами перед
численно равными величинами qiqk
и qkqi
Для небольших смещений из положения равновесия потенциальную энергнию V можно разложить в степенной ряд по степеням свободы qi
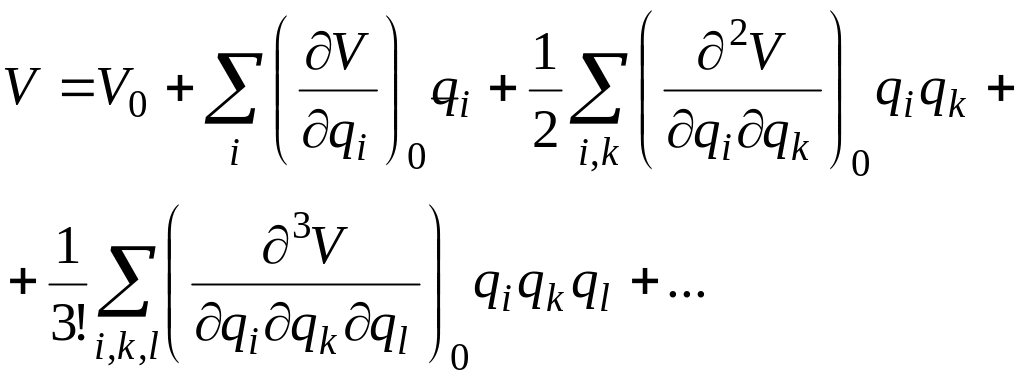 (4.3)
(4.3)
Можно
выбрать систему координат так, чтобы
равновесное значение потенциальной
энергии V0
равнялось нулю. тогда
формула (4.3) значительно упростится.
Кроме того, в состоянии равновесия все
qi
и
![]() ,
где fi
– квазиупругая сила, действующая на
i-ю
связь.
,
где fi
– квазиупругая сила, действующая на
i-ю
связь.
Для достаточно малых амплитуд колебаний можно пренебречь высшими членами разложения, в которые входят q в третьей, четвертой и высших степенях. После этого получим:
![]() ,
(4. 4)
,
(4. 4)
что
совпадает с формулой
(4.2), если
принять
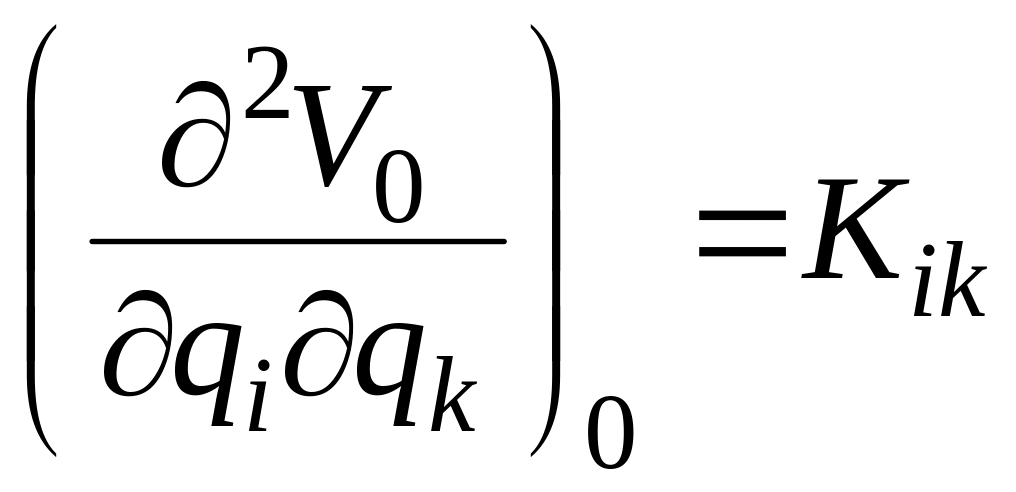 (индексы i
и k
не равны друг другу и пробегают значения
от i,
k
= 1 до п).
(индексы i
и k
не равны друг другу и пробегают значения
от i,
k
= 1 до п).
Уравнения движения Ньютона для многоатомной молекулы удобно записать в такой форме, в которую бы входили значения кинетической и потенциальной энергий. В этом случае необходимо записать функцию Лагранжа для молекулы, совершающей малые колебания, в виде
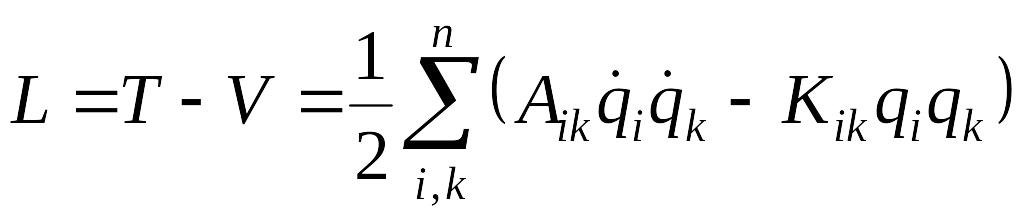 ,
(4.5)
,
(4.5)
а затем записать уравнения движения в форме Ньютона, т. е.
![]()
или
![]() ,
(4.6)
,
(4.6)
так как Т – функция только скоростей, а V – функция только координат. Подставив в (4. 6) значения кинетической и потенциальной энергии (4.1) и (4.2), получим следующее выражение:
![]() .
(4.7)
.
(4.7)
Формула (4.7) представляет собой систему n (i, = l, 2, ..., n) линейных однородных дифференциальных уравнений с постоянными коэффициентами. Эта система в развернутом виде может быть записана следующим образом:
![]()
Соотношение (4.7) представляет собой систему n совместных дифференциальных уравнений второго порядка. Одно из возможных решений этой системы в гармоническом приближении ищем в виде
![]() ,
(4.9)
,
(4.9)
где q0k амплитуда k-го колебания; – угловая частота; – начальная фаза. Примем для простоты начальную фазу = 0. Тогда подстановка равенства (4.9) в систему дифференциальных уравнений (4.8) позволяет получить систему алгебраических уравнений вида
![]() .
(4.10)
.
(4.10)
Это система однородных линейных алгебраических уравнений относительно n неизвестных амплитуд колебаний qk0. В развернутом виде эту систему можно записать следующим образом
![]() ,
,
![]() ,
(4.11)
,
(4.11)
... ... ... ... ... ... ... ... ... ... ,
![]() .
.
Условием разрешимости системы (4.11) является равенство нулю определителя, составленного из коэффициентов при неизвестных амплитудах, т. е.
![]() . (4.12)
. (4.12)
В развернутом виде этот определитель будет выглядеть так:
![]()
Уравнение
(4.12)
называется характеристическим. Оно в
общем случае имеет n
различных вещественных положительных
корней
![]() (
= l,
2, ..., n).
Величины
,
определяемые из этого уравнения,
называются собственными частотами
колебаний молекулы. Только для этих
значений
в определителе
(4.11) получают
ненулевые значения
(
= l,
2, ..., n).
Величины
,
определяемые из этого уравнения,
называются собственными частотами
колебаний молекулы. Только для этих
значений
в определителе
(4.11) получают
ненулевые значения
![]() .
Определив одно из значений
,
обращающих детерминант
(4.12) в нуль,
можно найти коэффициенты в уравнениях
(4.11) перед
неизвестными
.
Это позволит получить решения системы
(4.10) в виде
.
Определив одно из значений
,
обращающих детерминант
(4.12) в нуль,
можно найти коэффициенты в уравнениях
(4.11) перед
неизвестными
.
Это позволит получить решения системы
(4.10) в виде
![]() ,
где индекс
указывает на соответствие с данным
значением
,
где индекс
указывает на соответствие с данным
значением
![]() .
Однако система уравнений
(4.10) не
определяет однозначно
,
а только их отношения. Если принять
значение одной из амплитуд колебаний
за единицу (например,
.
Однако система уравнений
(4.10) не
определяет однозначно
,
а только их отношения. Если принять
значение одной из амплитуд колебаний
за единицу (например,
![]() ),
то мы получим набор значений амплитуд
),
то мы получим набор значений амплитуд
![]() ,
,
![]() и т. д. в условных единицах. Каждый
корень определителя (4.12) соответствует
набору амплитуд
и, следовательно,
решению
(4.10) исходных
уравнений движения.
и т. д. в условных единицах. Каждый
корень определителя (4.12) соответствует
набору амплитуд
и, следовательно,
решению
(4.10) исходных
уравнений движения.
Если все частоты найдены из корней определителя (4.12) (в предположении, что коэффициенты Аik и Кik известны), то из (2.10) можно рассчитать все коэффициенты (амплитуды колебаний).
Исследуем
характер полученных решений. Из уравнения
(4.9) следует,
что каждый атом колеблется около своего
положения равновесия по закону простого
гармонического движения с амплитудой
![]() ,
частотой k
и фазой .Частота
и фаза, соответствующая данному решению
векового уравнения, одинаковы для каждой
координаты. Амплитуды смещений всех
атомов, вообще говоря, различны. Мы
видели, что каждому значению
векового
определителя
(4.12)
соответствует свой набор амплитуд qik0,
характеризующий форму колебания.
,
частотой k
и фазой .Частота
и фаза, соответствующая данному решению
векового уравнения, одинаковы для каждой
координаты. Амплитуды смещений всех
атомов, вообще говоря, различны. Мы
видели, что каждому значению
векового
определителя
(4.12)
соответствует свой набор амплитуд qik0,
характеризующий форму колебания.
Поскольку фаза и частота одинаковы, то все атомы достигают положения максимальных смещений в одно и то же время, и все атомы в одно и то же время проходят свои равновесные положения. Колебание, имеющее указанные характеристики, называется нормальным, а частота этого колебания – нормальной или фундаментальной.
Рассмотренные случаи решения системы уравнений (4.8) представляют собой частные решения. В общем случае изменение во времени каждой координаты qk представляет собой совокупность одновременно происходящих гармонических колебаний с частотами ω1, ω2,... ωk...
Изложенное выше справедливо в том случае, когда все частоты ωk, допускаемые решением определителя (4.12), различны. Однако иногда, когда две или три частоты при решении уравнения (4.12) совпадают. В этом случае говорят о дважды или трижды вырожденном нормальном колебании. Картина колебаний атомов в молекуле при этом усложняется. Например, известно, что при сложении двух колебаний одинаковой частоты, но различных амплитуд и фаз результирующее движение может представлять собой возвратно-поступательное движение по прямой, по эллипсу, или движение по окружности.
