
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
3.5. Колебательные спектры двухатомных молекул с изотопным замещением
Как мы видели в 2.2, положение колебательных полос в ИК-спектрах молекул зависит от приведенной массы молекулы. Если один из атомов в молекуле заменить ее изотопом, то это почти не повлияет на ее электронную оболочку и, следовательно, на межатомные расстояния и квазиупругую постоянную k, но существенно изменит приведенную массу .
Так как положение колебательных полос обратно пропорционально приведенной массе , то при более тяжелой изотопной молекуле положение полос будет сдвигаться влево в частотной шкале, а величина сдвига будет определяться различием в приведенных массах. например, для водорода Н2 и D2 это различие максимально, так как приведенные массы различаются в 2 раза. для других более тяжелых молекул это различие невелико.
Рассмотрим изменение колебательных частот для молекул, содержащих атом водорода Н, который может быть заменен атомом дейтерия D, имеющим вдвое большую массу. Указанная процедура в химии называется дейтерированием, которое приводит к довольно значительному изменению частот колебаний. Например, возьмем отношение частот колебаний Н2 и D2
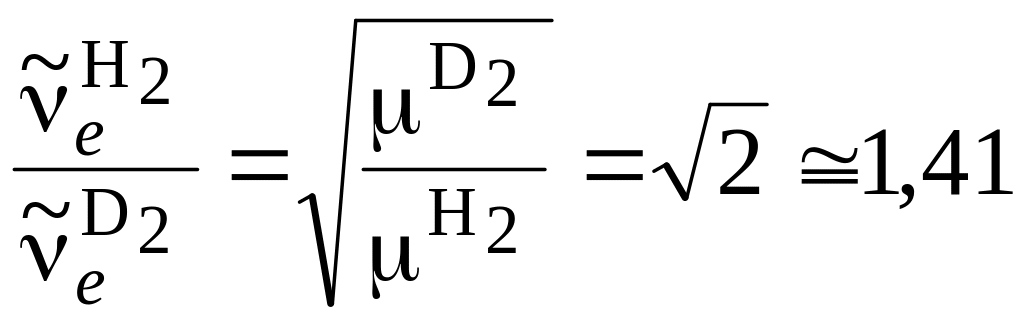 ,
( 3.55)
,
( 3.55)
т.
е. частота колебаний молекулы водорода
в
![]() раз больше частоты колебаний молекулы
дейтерия. Действительно, сравнение
частот колебаний этих молекул, приведенных
в табл. 3.1 показывает, что их отношение
равно 1,41, что совпадает с (3.55). Если
сравнить различие частот колебаний в
молекуле
раз больше частоты колебаний молекулы
дейтерия. Действительно, сравнение
частот колебаний этих молекул, приведенных
в табл. 3.1 показывает, что их отношение
равно 1,41, что совпадает с (3.55). Если
сравнить различие частот колебаний в
молекуле
![]() и
и
![]() ,
то оно будет
небольшим, так как отношение частот
колебаний близко к единице:
,
то оно будет
небольшим, так как отношение частот
колебаний близко к единице:
![]() .
(3.56)
.
(3.56)
При
частоте колебаний
![]() ,
равной 560 см–1,
это различие составит 16 см–1,
а разница в частотах для водорода (
,
равной 560 см–1,
это различие составит 16 см–1,
а разница в частотах для водорода (![]() 4401 см–1)
и дейтерия (
4401 см–1)
и дейтерия (![]() 3118
см–1)
составляет 1283 см–1.
3118
см–1)
составляет 1283 см–1.
Рассмотрим
в общем случае более подробно отношение
изотопических частот .
обозначим
массы атомов в изотопически незамещенной
молекуле через m1
и m2
, а в
изотопически замещенной – через
![]() и
и
![]() .
тогда
выражение
.
тогда
выражение
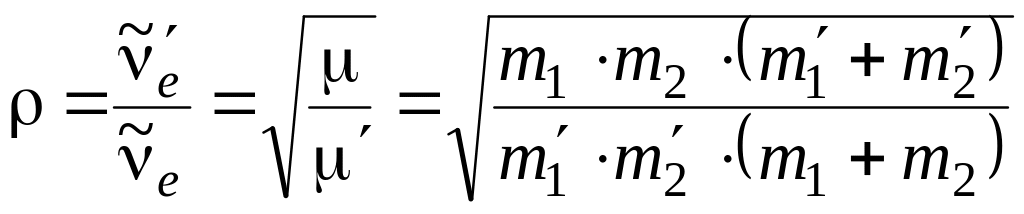 .
(3.57)
.
(3.57)
в случае изотопического замещения лишь одного из атомов (например, m2 = m'2) сводится к формуле:
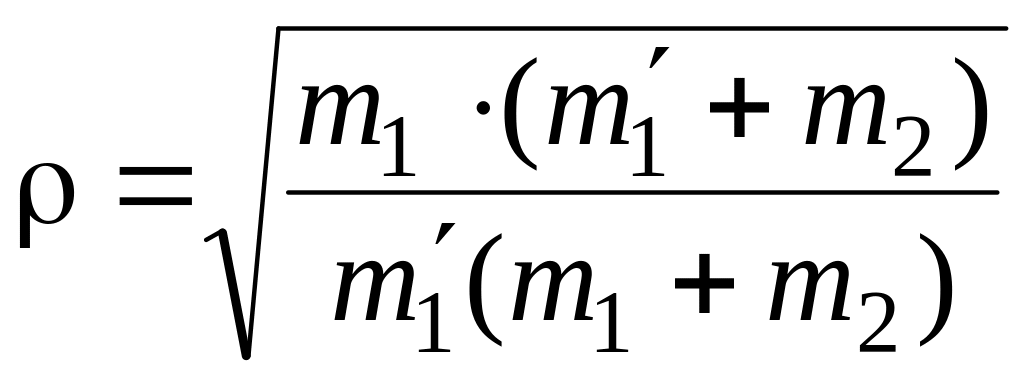 .
(3.58)
.
(3.58)
При дейтерировании двухатомной молекулы соотношение (3.58) можно переписать следующим образом:
![]() ,
(3.59)
,
(3.59)
где
m2
– масса
атома, отличного от водорода. Когда эта
масса достаточно велика, т. е. m2
>> m1
, то величина
будет стремиться к своему предельному
значению
![]() Этот результат физически понятен, так
как при большой массе m2
практически
колеблется только атом водорода (m1).
Этот результат физически понятен, так
как при большой массе m2
практически
колеблется только атом водорода (m1).
Для
случая, когда массы изотопов будут мало
отличаться друг от друга (например, (![]() и
и
![]() ),
изменение частот колебаний будет
невелико, т. е.
будет мало
отличаться от единицы. Пусть m1
= m2
и m'1
= m'2
, но m'2
=m1
+
,
где
есть разность в изотопических массах,
на основании (3.57) получим
),
изменение частот колебаний будет
невелико, т. е.
будет мало
отличаться от единицы. Пусть m1
= m2
и m'1
= m'2
, но m'2
=m1
+
,
где
есть разность в изотопических массах,
на основании (3.57) получим
![]() ,
(3.60)
,
(3.60)
т.
е. относительное изменение частот
порядка
![]() .
Для указанных молекул это отличие равно
0,057. Необходимо при этом отметить, что
различие в частотах колебаний изотопных
молекул в обертонах выше, чем у основных
тонов, и это различие тем больше, чем
выше порядок обертона.
.
Для указанных молекул это отличие равно
0,057. Необходимо при этом отметить, что
различие в частотах колебаний изотопных
молекул в обертонах выше, чем у основных
тонов, и это различие тем больше, чем
выше порядок обертона.
Метод изотопических замещений оказывается очень полезным при рассмотрении колебаний многоатомных молекул, так как позволяет относить полученные в ИК-спектре полосы к колебаниям соответствующих групп атомов в сложной молекуле.
В заключение необходимо отметить, что изотопическое замещение одного из атомов в двухатомной молекуле может приводить к появлению полос в ИК-спектре поглощения для молекул, не обладающих дипольным моментом и относящихся к симметрии Dh . Если молекула состоит из разных изотопов (например, HD и Сl37 Cl35), то колебание у этой молекулы происходит несимметричным образом и возникает переменный дипольный момент, обуславливающий поглощение ИК радиации. Симметрия молекулы при этом нарушается колебаниями, которые не являются полносимметричными. Только при одинаковых ядрах двухатомная молекула при колебаниях сохраняет симметрию Dh, при этом указанная молекула не будет поглощать или испускать ИК-радиацию. Чем больше различие в массах колеблющихся атомов, тем больше асимметрия колебаний, тем интенсивнее соответствующая полоса в ИК-спектре.
Эффект изотопного замещения в колебательных спектрах дает чувствительный и довольно точный метод обнаружения изотопов и измерения их относительных количеств путем измерения интенсивностей линий.
