
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
Интерпретация колебательного спектра бензола
Номер колебания |
Форма колебания |
Симмет-рия |
Расчет, см–1 |
Эксперимент, жидкость |
|||
ИК, см–1,инт, Iотн. |
КР, см–1, инт. Iотн |
||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
(С–С) æ(ССС) |
E2u |
405 |
(405) |
оч.сл. |
405 |
0 |
|
(ССС) |
E2g |
607 |
|
|
607 |
130 |
|
(С–H) |
A2 u |
671 |
676 |
оч.с. |
|
|
|
(С–H) æ (С–H) |
B2g |
703 |
|
|
690 |
0 |
|
(С–H) |
E1g |
849 |
|
|
850 |
34 |
|
(С–H) æ (СCC) |
E2u |
970 |
(970) |
оч.сл. |
|
|
|
(С–H) æ (СCC) |
B2 g |
985 |
|
|
984 |
3 |
|
Q(CC) |
A1g |
992 |
|
|
992 |
1200 |
Продолжение табл. 4.11
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
(ССС) |
B1u |
1010 |
(1010) |
оч.сл. |
|
|
|
(CCH) Q(CC) |
E1u |
1037 |
1037 |
оч.с. |
|
|
|
(CCH) Q(CC) |
B2u |
1146 |
|
|
|
|
|
(CCH) Q(CC) |
E2g |
1178 |
|
|
1178 |
120 |
|
(CCH) Q(CC) |
B2u |
1310 |
|
|
|
|
|
(CCH) Q(CC) |
A2g |
1326 |
|
|
1326 |
0 |
|
(CCH) Q(CC) |
E1u
|
1485
|
1485
|
оч.с. |
|
|
|
(CCH) Q(CC) |
E2g |
1596 |
|
|
1606 1586 |
50 85 |
|
q(C–H) |
E2g |
3047 |
|
|
3047 |
260 |
|
q(C–H) |
B1u |
3060 |
|
|
|
|
|
q(C–H) |
A1g |
3062 |
|
|
3062 |
630 |
|
q(C–H) |
E1u |
3080 |
3054 3085 |
с. с. |
|
|
Примечание: обозначение частот колебаний произведено по вильсону:
q – изменение длин связей С–Н; (С–Н) – угол поворота связи С–Н относительно плоскости молекулы; (ССН) – изменение угла ССН; (ССС) – изменение угла ССС; æ(ССС) – изменение угла ССС относительно плоскости молекулы; Q(CC) – изменение длины связи;
Как следует из табл. 4.11, экспериментально полученные частоты хорошо согласуются с расчетными как по числовым значениям, так и по поляризации (симметрии).
4.13. Примеры ИК спектров поглощения
отдельных молекул и ионов
На рис. 4.17 приведен инфракрасный спектр поглощения тонкой пленки жидкости бензола. Как видим, спектр бензола занимает область частот от 400 до 3500 см–1.
Наиболее интенсивные полосы относятся к типам колебаний A2u и E1u, как следует из общего расчета, таких типов колебаний всего четыре: три дважды вырожденных E1u и один тип A2u. Согласно внимание на табл. 4.8, для указанных типов колебаний происходит изменение дипольного момента. Известно, чтобы молекула поглощала ИК-радиацию, необходимо при этом изменение дипольного момента. Если этого не происходит, то молекула не поглощает ИК-радиацию. Следовательно, в молекуле бензола будут активны в ИК-спектре колебания типов A2u и E1u, а таких колебаний (если не учитывать снятие вырождения) только четыре. Значит, четыре полосы в ИК спектре будут наиболее интенсивны. Далее отметим некоторые особенности ИК-спектра (рис. 4.17). Кроме интенсивных полос поглощения в ИК спектре наблюдаются малоинтенсивные полосы. Их отнесение необходимо искать в комбинациях различных колебаний, возможных для данной молекулы. Два из составных типов колебаний обозначены на рисунке. Это комбинации Е2u и В2g, E1g и E2u. Так как, согласно групповым законам составные колебания будут наблюдаться в виде слабых полос, если прямое произведение типов симметрии колебаний (Е2u ·В2g) будет содержать тип симметрии E1u. Проверка по групповым законам приводит к следующим выражениям:
В2g ·E1u = E1u; E1g· E2u = В1u · В2u · E1u,
т. е. в каждом случае мы имеем разрешенный по правилам отбора тип симметрии E1u. Такие составные тоны могут наблюдаться в ИК спектре.
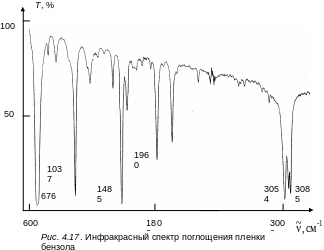
В области 3000 см–1 вместо двух и даже одной полосы типа E1u наблюдаются три полосы. Причиной этого является взаимодействие колебаний основных типов с их обертонами или составными тонами. Если взаимодействуют колебания одинаковой симметрии (Ферми-резонанс), то это приводит к расщеплению частот колебаний, что наблюдается в спектре. Ряд очень слабых полос могут принадлежать некоторым другим составным тонам (предоставляем проверить симметрию читателям) и небольшим примесям других ароматических молекул, присутствующих в жидком бензоле.
Рассмотрим ИК-спектры поглощения иона NO3– точечной группы симметрии D3h. В свободном состоянии он имеет конфигурацию плоского треугольника с атомами кислорода в вершинах и длинами связей N–O, равными 0,121 нм. Шесть его нормальных колебаний распределены между следующими типами симметрии
![]() ,
(4.90)
,
(4.90)
и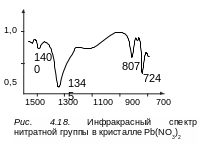 з
которых в ИК-спектре активны только
колебания типов
з
которых в ИК-спектре активны только
колебания типов
![]() и
E',
по-этому ИК-спектр нитратной группы и
характеризуется тремя полосами (рис.
4.18). Частоты, принадлежащие свободной
нитратной группе NO3–,
проявляются в
ИК-спектрах
нитратов
щелочных металлов и считаются характерными
для соединений с ионными связями
нитратной группы с атомами металла. При
включении одного или двух атомов
кислорода нитратной группы в ковалентную
связь с атомами металла симметрия ее
понижается до С2.
При этом снимается вырождение уровней
энергии и все шесть нормальных колебаний
становятся активными в ИК-спектре. На
рис. 4.19 приведены формы колебаний
нитратной группы симметрии С2,
а в табл. 4.12 – частоты и симметрия
колебаний свободного иона нитратной
группы и бидентатно координированного.
Как видно из табл. 4.12, при бидентатной
координации иона нитратной группы
вырождение снимается с частот
и
и все шесть колебаний становятся
активными в ИК спектре.
и
E',
по-этому ИК-спектр нитратной группы и
характеризуется тремя полосами (рис.
4.18). Частоты, принадлежащие свободной
нитратной группе NO3–,
проявляются в
ИК-спектрах
нитратов
щелочных металлов и считаются характерными
для соединений с ионными связями
нитратной группы с атомами металла. При
включении одного или двух атомов
кислорода нитратной группы в ковалентную
связь с атомами металла симметрия ее
понижается до С2.
При этом снимается вырождение уровней
энергии и все шесть нормальных колебаний
становятся активными в ИК-спектре. На
рис. 4.19 приведены формы колебаний
нитратной группы симметрии С2,
а в табл. 4.12 – частоты и симметрия
колебаний свободного иона нитратной
группы и бидентатно координированного.
Как видно из табл. 4.12, при бидентатной
координации иона нитратной группы
вырождение снимается с частот
и
и все шесть колебаний становятся
активными в ИК спектре.
Таблица 4.12
