
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
6.6.1 Бензол
Простейшей
ароматической молекулой является
молекула бензола С6Н6.
При рассмотрении ее молекулярных
орбиталей (см. п. 6.2.3) мы пришли к выводу,
что нижней заполненной молекулярной
орбиталью является орбиталь симметрии
![]() .
При поглощении кванта света электрон
переходит из занятой молекулярной
орбитали типа
на свободную симметрии
.
При поглощении кванта света электрон
переходит из занятой молекулярной
орбитали типа
на свободную симметрии
![]() ,
т. е. симметрия результирующего состояния
есть
,
т. е. симметрия результирующего состояния
есть
![]() .
.
Таким образом, первое электронное возбужденное состояние дает три состояния, которые соответствуют случайному вырождению. Учет межэлектронного отталкивания приводит к трем отдельным состояниям, которые располагаются в следующем порядке: B2u, B1u, E1u Действительно, сопоставление с экспериментом показывает,что в ультрафиолетовой области спектра бензол имеет три полосы поглощения, причем две из них обладают колебательной структурой со сравнительно малой силой осциллятора (запрещенные переходы 260 и 200 нм) и одна характеризуется высокой силой осциллятора при 180 нм, равной единице. Общая схема электронных переходов показана на рис. 6.18.
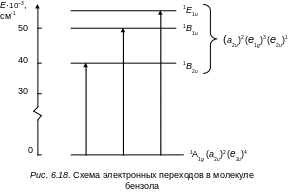 Первый
длинноволновый переход соответствует
электронному переходу типа
,
который для точечной группы симметрии
D6h
молекулы бензола запрещен по симметрии.
Разрешается он при учете взаимодействий
электронного и колебательного движения
(эффект Герцберга
– Теллера, см.
6.42). Колебание e2g
вследствие вибронного взаимодействия
смешивает состояния
и
Первый
длинноволновый переход соответствует
электронному переходу типа
,
который для точечной группы симметрии
D6h
молекулы бензола запрещен по симметрии.
Разрешается он при учете взаимодействий
электронного и колебательного движения
(эффект Герцберга
– Теллера, см.
6.42). Колебание e2g
вследствие вибронного взаимодействия
смешивает состояния
и
![]() .
Действительно, если рассмотреть прямое
произведение типа симметрии электронного
состояния
.
Действительно, если рассмотреть прямое
произведение типа симметрии электронного
состояния
![]() на колебательное состояние
на колебательное состояние
![]() ,
то получится тип симметрии вибронного
состояния
,
которое хорошо взаимодействует с
разрешенным состоянием
в силу одинаковой симметрии.
,
то получится тип симметрии вибронного
состояния
,
которое хорошо взаимодействует с
разрешенным состоянием
в силу одинаковой симметрии.
В молекуле бензола
имеется четыре колебания типа
![]() (см. табл. 6.1).
(см. табл. 6.1).
Таблица 6.1
Колебательные
частоты (см–1) молекулы бензола
в парах.
Нижнее электронное состояние
![]() и верхнее
и верхнее
![]()
Обозначение частот |
Симметрия |
Состояния |
|
|
|
||
1 |
a1g |
993 |
923 * |
2 |
a1g |
3073 |
3130 |
3 |
a2g |
1350 |
|
4 |
b2g |
707 |
365 |
5 |
b2g |
990 |
745 |
6 |
e2g |
608 |
521* |
7 |
e2g |
3056 |
3077 |
8 |
e2g |
1599 |
|
9 |
e2g |
1178 |
1148 |
10 |
e1g |
846 |
581 |
11 |
a2u |
674 |
516 |
12 |
b1u |
1010 |
|
13 |
b1u |
305 |
|
14 |
b2u |
1309 |
1570 |
15 |
b2u |
1146 |
1048 |
16 |
e1g |
399 |
237 |
17 |
e1g |
967 |
718 |
18 |
e1u |
1037 |
919 |
19 |
e1u |
1482 |
|
20 |
e1u |
3064 |
|
* – обозначены
наиболее интенсивные вибронные переходы
в спектре электронного поглощения (![]() ).
).
Нумерация частот
приведена по Вильсону. Два штриха у
частоты обозначает нижнее электронное
состояние. Самые интенсивные в спектре
поглощения полосы соответствуют
переходам,
включающим однократное колебание
![]() с
последующей комбинацией его с
полносимметричным колебанием
с
последующей комбинацией его с
полносимметричным колебанием
![]() (дыхательное
колебание кольца). В качестве примера
на рис.6.19 приведен спектр поглощения
бензола, растворенного в жидком криптоне
(T
= 150 К, длинноволновая область).
(дыхательное
колебание кольца). В качестве примера
на рис.6.19 приведен спектр поглощения
бензола, растворенного в жидком криптоне
(T
= 150 К, длинноволновая область).
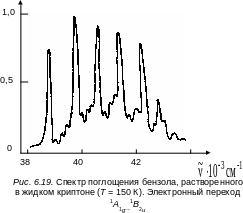
![]()
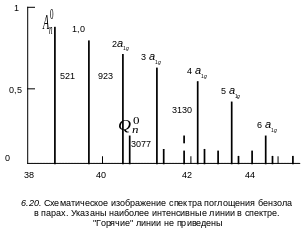
Почти 95 % всей интенсивности сосредоточено именно в вибронных компонентах указанных колебаний. Около 5 % спектра поглощения приходится на другие комбинации частот типа симметрии e2g. На рис. 6.20 приведено схематическое изображение спектра поглощения бензола в парах.
Кроме того, в
спектре поглощения паров ряд наблюдается
горячих переходов с включением колебаний
![]() ,
,
![]() и
и
![]() в нижнем электронном состоянии. На рис.
6.20 горячие полосы не указаны, чтобы не
загромождать рисунок. Отмечены только
наиболее интенсивные серии и несколько
слабых. В литературе условились обозначать
серии следующим образом: серия
в нижнем электронном состоянии. На рис.
6.20 горячие полосы не указаны, чтобы не
загромождать рисунок. Отмечены только
наиболее интенсивные серии и несколько
слабых. В литературе условились обозначать
серии следующим образом: серия
![]() ,
серия
,
серия
![]() ,
серия
,
серия
![]() (горячая серия), а также отдельная серия
(горячая серия), а также отдельная серия
![]()
Обозначения следует читать следующим образом: цифра обозначает номер колебания по Вильсону; верхний индекс – значение колебательного квантового числа в верхнем электронном состоянии; нижний индекс – то же самое для нижнего состояния.
Например,
![]() – означает колебание '6
и комбинация с ним колебания '1
в верхнем со стоянии (правда, оно может
комбинировать n
раз). Частоты этой серии определяются
как
– означает колебание '6
и комбинация с ним колебания '1
в верхнем со стоянии (правда, оно может
комбинировать n
раз). Частоты этой серии определяются
как
![]() .
В спектре поглощения мы наблюдаем
прогрессии по частоте
.
В спектре поглощения мы наблюдаем
прогрессии по частоте
![]() до семи квантов с уменьшающейся частотой
от 923см–1
до 917см–1.
колебание
''2
(3056см–1,
тип e2g)
также появляется по механизму Герцберга
– Теллера и дает повторы
с колебанием
''1
(993см–1,
тип
до семи квантов с уменьшающейся частотой
от 923см–1
до 917см–1.
колебание
''2
(3056см–1,
тип e2g)
также появляется по механизму Герцберга
– Теллера и дает повторы
с колебанием
''1
(993см–1,
тип
![]() )
до четырех квантов, т. е. соответствующие
линии в спектре будут записываться так:
)
до четырех квантов, т. е. соответствующие
линии в спектре будут записываться так:
![]() ,
где
m =
1, 2, ..., 4.
,
где
m =
1, 2, ..., 4.
Частота
e2g,
равная 1178см–1
проявляется в комбинации с частотой
'6 (525
см–1),
а затем в комбинации с полносимметричным
колебанием (923 см–1).
В газовой фазе переход 0–0 запрещен,
однако в растворе бензола в криптоне
он очень слабо разрешен. Общий вид
спектра поглощения бензола в жидком
криптоне очень похож на спектр поглощения
в
газовой фазе и для наглядности он
приведен на рис. 6.19 (![]() ).На
схеме рис. 6.20 многие серии полос
представлены условно.
).На
схеме рис. 6.20 многие серии полос
представлены условно.
В табл 6.1 приведены частоты колебаний, зарегистрированные в нижнем и верхнем электронных состояниях. Как следует из таблицы, некоторые частоты испытывают заметные изменения своих значений, особенно в сторону уменьшения. Правда, существует несколько колебаний, которые увеличивают свои частоты при возбуждении молекулы. Таким образом, в электронном спектре поглощения всегда выделяются две-три частоты колебаний, которые в общем формируют весь электронно-колебательный спектр молекулы. Их интенсивность в спектре определяется спецификой электронно-колебательного взаимодействия. Это положение относится и к другим ароматическим молекулам.
6.6.2 Нафталин
Молекула нафталина
С10Н8
содержит два бензольных кольца и
относится к точечной группе симметрии
D2h.
Если провести аналогию между спектром
поглощения паров нафталина (рис. 6. 21) и
бензола, то следует заметить, что чисто
электронный переход в спектре нафталина
значительно смещен в красную сторону
по сравнению со спектром бензола (![]() ).
Экспериментальные
данные по поляризации
показывают,
что первый электронный переход в молекуле
нафталина относится к типу B3u
и разрешен
по симметрии. Однако экспериментально
измеренная сила осциллятора этого
перехода
).
Экспериментальные
данные по поляризации
показывают,
что первый электронный переход в молекуле
нафталина относится к типу B3u
и разрешен
по симметрии. Однако экспериментально
измеренная сила осциллятора этого
перехода
![]() почти в 50 раз меньше перехода в следующее
электронное состояние
и на три порядка меньше в третье
возбужденное состояние
почти в 50 раз меньше перехода в следующее
электронное состояние
и на три порядка меньше в третье
возбужденное состояние
![]() .
Квантовомеханический расчет силы
осциллятора первого синглет-синглетного
перехода
.
Квантовомеханический расчет силы
осциллятора первого синглет-синглетного
перехода
![]() в -
электронном приближении дает нулевой
результат, что можно объяснить «случайной»
симметрией волновых функций.
в -
электронном приближении дает нулевой
результат, что можно объяснить «случайной»
симметрией волновых функций.
Поэтому можно предположить, что общая структура спектра поглощения будет подобна структуре спектра молекулы бензола. На рис. 6.21 приведена схема спектра поглощения паров нафталина.
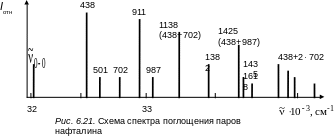
При сравнении спектров поглощения паров бензола и нафталина можно установить, что наиболее интенсивные вибронные переходы в молекуле нафталина начинаются из двух несимметричных колебаний типа b1g и включают частоты 438 и 911 см–1 (см. рис. 6.21 и табл. 6.2). Колебания, которые смешивают оба состояния ( и ), должны относиться к типу симметрии b1g.
Таблица 6.2
Колебательные частоты (см–1) в спектрах поглощения и флуоресценции паров нафталина
Флуоресценция
|
Поглощение
|
Обозначения частот и симметрия колебаний |
506 |
438 |
17 (b1g) |
511 |
501 |
9 (ag) |
763 |
702 |
8 (ag) |
936 |
911 |
16 (b1g) |
1025 |
987 |
7 (ag) |
|
1138 |
6 (ag) или 17+28 (b1g) |
1380 |
1382 |
5 (ag) |
1450 |
1425 |
17+7 (b1g) |
|
1435 |
4 (ag) |
1639 |
1619 |
12 (b1g) |
|
1849 |
17+28 (b1g) |
1886 |
1883 |
17+13 |
Действительно,
согласно теории групп вибронный переход,
соответствующий колебанию типа b1g,
будет иметь симметрию B2u,
т. е.
![]() ,
поэтому он будет хорошо взаимодействовать
с электроном перехода той же симметрии
и заимствовать из него свою интенсивность.
,
поэтому он будет хорошо взаимодействовать
с электроном перехода той же симметрии
и заимствовать из него свою интенсивность.
В спектре наблюдаются
наиболее интенсивные переходы с
включением двух колебаний типа b1g
(438 и 911см–1),
которые и дают существенный вклад в
общую интенсивность спектра поглощения,
поэтому часть вибронных линий почти не
уменьшает свою интенсивность при
приближении к частоте второго чисто
электронного перехода (![]() ).
Поляризация этих переходов отличается
от поляризации чисто электронного
перехода (
).
Поляризация этих переходов отличается
от поляризации чисто электронного
перехода (![]() )
и его повторений с частотами
полносимметричных колебаний. Таких
колебаний в ближней области спектра
поглощения можно обнаружить до четырех
(501, 702, 987 и 1382 см–1).
)
и его повторений с частотами
полносимметричных колебаний. Таких
колебаний в ближней области спектра
поглощения можно обнаружить до четырех
(501, 702, 987 и 1382 см–1).
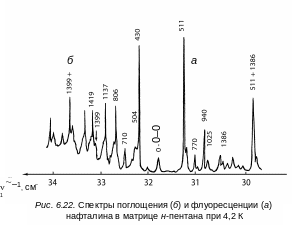
В спектроскопии полагают, что первый чисто электронный переход проявляется в спектре поглощения за счет эффекта Герцберга – Теллера. А так как в спектре поглощения чисто электронный переход все-таки наблюдается, хотя и с малой интенсивностью, то, согласно принципу Франка – Кондона, в комбинации с ним можно обнаружить указанные выше колебания полносимметричного типа, которые в спектрах поглощения и флуоресценции будут давать серии линий (секвенции, т. е. повторы по частоте одного или нескольких активных полносимметричных колебаний). На рис. 6.22 в качестве иллюстрации приведены начальные участки спектров поглощения и флуоресценции нафталина в матрице n-пентана при 4,2 К. Линия 0–0-перехода совмещена.
Из рис. 6.22 видно, что сохраняется зеркальная симметрия спектров и наиболее активно проявляются в обоих спектрах одни и те же колебания. В спектре флуоресценции хорошо заметно начало повтора структуры спектра на частоте полносимметричного колебания (1380 см–1.)
6.6.3 Антрацен
Молекула антрацена
С![]() Н
Н![]() содержит три бензольных кольца и, подобно
бензолу и нафталину имеет плоское
строение и относится к точечной группе
симметрии D
содержит три бензольных кольца и, подобно
бензолу и нафталину имеет плоское
строение и относится к точечной группе
симметрии D![]() .Чисто
электронный переход в молекуле разрешен
и имеет заметную силу осциллятора
порядка
.Чисто
электронный переход в молекуле разрешен
и имеет заметную силу осциллятора
порядка
![]() .
Согласно принципу Франка-Кондона в
электронном спектре поглощения
преимущественно будут проявляться
полносимметричные колебания молекулы,
взаимодействующие с чисто электронным
переходом. Действительно, для молекулы
антрацена можно выделить таких два
колебания с частотами
.
Согласно принципу Франка-Кондона в
электронном спектре поглощения
преимущественно будут проявляться
полносимметричные колебания молекулы,
взаимодействующие с чисто электронным
переходом. Действительно, для молекулы
антрацена можно выделить таких два
колебания с частотами
![]() 400
см–1
(деформационное колебание, приводящее
к изменению скелета молекулы) и 1400 см–1,
возбуждение которого сопровождается
изменением размеров короткой оси
молекулы. Отметим при этом, что вдоль
этой же оси поляризован рассматриваемый
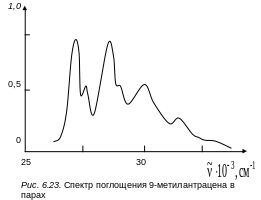
электронный переход. На рис. 6.23 приведен
пример поглощения 9-метилантрацена в
парах при сравнительно высокой
температуре.
400
см–1
(деформационное колебание, приводящее
к изменению скелета молекулы) и 1400 см–1,
возбуждение которого сопровождается
изменением размеров короткой оси
молекулы. Отметим при этом, что вдоль
этой же оси поляризован рассматриваемый
электронный переход. На рис. 6.23 приведен
пример поглощения 9-метилантрацена в
парах при сравнительно высокой
температуре.
Из рисунка можно четко выделить два колебания – низкочастотное, дающее перегиб в области первой полосы, и высокочастотное, которое ответственно за расширение спектра в коротковолновую сторону. Последнее колебание дает повторы, которых можно наблюдать до пяти. Конечно, изучая тонкоструктурные спектры молекулы, можно обнаружить и ряд других, достаточно слабых колебаний, присутствующих в спектре поглощения 1506, 1585, 1640 см‑1. На рис. 6.24 приведен спектр возбуждения (поглощения) молекулы антрацена, охлажденного в сверхзвуковой струе. В спектре заметны как низкочастотные так и высокочастотные колебания. Особо следует отметить основную несущую частоту 1380 см–1(ag), которая в спектре дает повторы до пяти квантов. Отметим, что низкочастотное колебание 387 см–1, заметно в спектре только двумя квантами.
В табл 6.3 приведены значения и симметрия частот молекулы антрацена, наблюдаемых в низкотемпературных тонкоструктурных спектрах.
Таблица 6.3.
Колебательные частоты (в см–1) в спектрах поглощения и флуоресценции молекулы антрацена
-
Поглощение, пары
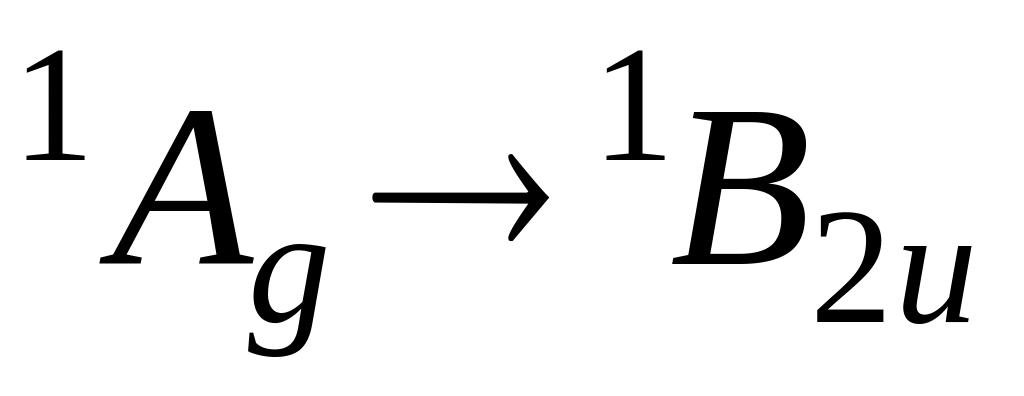
Флуоресценция, пары

Поглощение в матрице
Расчет
Отнесение колебаний
387
393
390
396
12, аg
541
625
601
11, аg
889
919
930
24, b3g
1014
1012
1030
1027
9, аg
1168
1169
1170
1165
8, аg
1290
1266
1265
1261
7, аg
1380
1409
1405
1403
6, аg
1488
1480
5, аg
1554
1568
1565
1561
16, b1g
1645
1655
1634
15, b1g
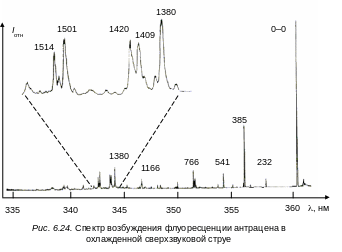
Анализ спектров показывает, что только две частоты полносимметричных колебаний типа ag 390 и 1400 см–1 определяют всю структуру спектра как поглощения, так и флуоресценции. Первую частоту можно проследить до двух, а вторую до пяти квантов. Они и определяют все секвенции (повторы) в спектрах (см. рис. 6.23).
6.7. Спектроскопия молекул в конденсированной среде
