
- •Глава 1. Общие вопросы спектроскопии молекул
- •1.1. Единицы измерения энергии и длины волны различных видов излучения
- •Переводные множители единиц измерения энергии
- •Длины волн, частоты и энергии различных диапазонов
- •1.2. Ширина уровней энергии и спектральных линий
- •1.3. Распределение молекул по уровням энергии
- •1.4. Вероятности оптических переходов
- •1.5. Квантовомеханический расчет вероятностей переходов
- •1.6. Правила отбора для различных типов излучения и поглощения
- •1.7 Поглощение света классическим электрическим осциллятором
- •Глава 2. Вращательные спектры молекул
- •2.1. Вращение двухатомной молекулы. Классический случай
- •2.2. Квантовомеханический случай
- •Значения вращательной энергии Евр двухатомной молекулы в зависимости от j
- •Вращательные постоянные , межъядерные расстояния re
- •2.3. Вращательные спектры многоатомных молекул
- •2.3.1. Деление молекул на сферические, симметричные и асимметричные волчки
- •2.3.2. Вращательные уровни энергии сферического волчка.
- •2.3.3. Вращательные уровни энергии и спектры молекул типа симметричного волчка
- •2.3.4. Уровни энергии и спектры молекул типа асимметричного волчка
- •Значения энергии вращательных уровней молекулы н2о, см–1
- •2.4. Применения вращательных спектров молекул
- •Вращательные постоянные (в см–1), межатомные расстояния и дипольные
- •Вращательные постоянные и структурные параметры некоторых
- •Глава 3.
- •3.1.Образование двухатомной молекулы. Представление о ее потенциальной кривой.
- •3.2. Колебания двухатомной молекулы как гармонического осциллятора
- •3.2.1. Механическая модель двухатомной молекулы
- •3.2.2. Квантовомеханический случай
- •3.3. Колебания двухатомной молекулы как ангармонического осциллятора
- •3.3.1. Аппроксимация зависимости потенциальной энергии от межьядерного расстояния в реальной молекуле (кривая Морзе)
- •3.3.2 Уровни энергии, правила отбора и спектры двухатомной молекулы как ангармонического осциллятора
- •3.4. Определение энергии диссоциации двухатомной молекулы
- •3.4.1. Аналитический метод
- •3.4.2. Метод графической экстраполяции (метод Берджа – Шпонер)
- •3.5. Колебательные спектры двухатомных молекул с изотопным замещением
- •3.6. Колебательно-вращательные спектры двухатомных молекул
- •3.6.1. Общая характеристика колебательно-вращательных
- •3.6.2 Колебательно-вращательные спектры. Ик-поглощения
- •3.6.3. Колебательно-вращательные спектры кр
- •3.6.4. Интенсивности линий вращательной структуры
- •Глава 4 колебательные спектры многоатомных молекул
- •4.1. Колебательные степени свободы многоатомной молекулы
- •4.2. Колебания многоатомной молекулы в классическом случае
- •4.3. Нормальные координаты и колебания.
- •4.4. Малые колебания в квантовой механике
- •4. 5. Классификация нормальных колебаний по форме
- •4.6. Симметрия молекул
- •4.6.1. Группа. Определение и основные свойства
- •4.6.2. Элементы и операции симметрии
- •4.6.3. Точечные группы симметрии и их элементы
- •Группы симметрии молекул
- •4.7. Примеры применения групповых законов к конкретным молекулам
- •Одно из возможных представлений группы с3
- •4.8. Представления группы симметрии. Линейные преобразования координат, соответствующие операциям симметрии
- •4.9. Выбор колебательных координат для характеристики колебательного движения атомов в молекулах
- •4.10. Анализ симметрии колебаний с помощью теории групп
- •4.11. Типы симметрии колебаний молекул
- •Типы симметрии колебаний и характеры представлений точечной группы симметрии d6h
- •4.12. Порядок нахождения числа колебаний различных типов симметрии
- •Характеры приводимых представлений молекулы воды точечной группы симметрии с.
- •Характеры приводимых представлений молекулы бензола точечной группы симметрии d6h
- •Интерпретация колебательного спектра бензола
- •Частоты и симметрия колебаний свободной и бидентатно-координированной нитратной группы
- •4.14. Спектры комбинационного рассеяния многоатомных молекул
- •4.15. Правила отбора в колебательных спектрах
- •Результирующая симметрия для сочетаний вырожденных состояний точечной группы симметрии d6h
- •4.16. Характеристические частоты колебаний молекулы
- •Характеристические частоты колебаний отдельных функциональных групп
- •Глава 5
- •5.1. Колебательная структура электронного спектра двухатомной молекулы
- •5.2.Относительная интенсивность полос в электронно-колебательном спектре двухатомной молекулы. Принцип Франка – Кондона
- •5.2.2. Квантовомеханический принцип Франка – Кондона
- •5.3. Химическая связь в двухатомной молекуле
- •5.3.1. Общие сведения о двухатомной молекуле
- •5.3.2. Основы метода молекулярных орбиталей (мо)
- •5.4. Типы химических связей в двухатомных молекулах. Σ- и π-связи
- •5.5. Систематика электронных состояний в двухатомной молекуле
- •5.6. Молекулярные электронные оболочки в двухатомной молекуле
- •5.7. Вращательная структура электронно-колебательных полос
- •5.8. Взаимодействие электронного и вращательного движений
- •5.9. Правила отбора в электронно-колебательно-вращательных спектрах двухатомных молекул
- •Глава 6 Электронные спектры многоатомных молекул
- •6.1. Электронные состояния и химические связи в многоатомных молекулах
- •6.1.1 Характеристика электронных состояний в многоатомных молекулах
- •6.2.2. Молекулярные орбитали молекулы формальдегида н2со
- •6.2.3. Молекула бензола с6н6
- •6.4. Некоторые вопросы теории электронно-колебательных спектров многоатомных молекул
- •6.4.1.Адиабатическое приближение
- •. Учет электронно-колебательного взаимодействия. Эффект Герцберга – Теллера
- •6.6. Электронные спектры поглощения ароматических соединений в газовой фазе
- •6.6.1 Бензол
- •6.7.1. Растворы. Ван-дер-ваальсово взаимодействие
- •Молекулярные постоянные и величины межмолекулярных взаимодействий в различных средах
- •6.7.2 Модель Онзагера
- •Реактивное поле, рассчитанное в модели Онзагера, равно
- •6.8. Электронные спектры поглощения растворов бензола и его производных
- •6.8.1. Общие замечания
- •6.8.2 Спектры растворов бензола и его производных с алкильными заместителями
- •6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
- •6.9. Электронные спектры молекул в твердотельных матрицах. Эффект Шпольского
- •6.10. Электронные спектры поглощения молекулярных кристаллов
- •6.10.1.Общая характеристика молекулярного кристалла
- •6.10.2. Возникновение экситонных состояний в кристаллах. Давыдовское расщепление
- •6.10.3. Электронные спектры поглощения кристаллов бензола, нафталина и антрацена
- •Литература
6.8.3. Спектры поглощения производных бензола с заместителями, содержащими неподеленные пары электронов
При наличии в молекуле бензола заместителей, содержащих неподеленные пары электронов, в длинноволновой области проявляются полосы, соответствующие n-π* преходам, т. е. переходам электрона из квазиатомного (свободного) состояния на разрыхляющую орбиталь π*-состояния кольца. Эта схема переходов широко используется в химии и физике для указания того, как ведут себя валентные и невалентные электроны в молекулах при оптическом возбуждении. Энергетические уровни внешних электронов строятся следующим образом. В наиболее низких состояниях размещаются электроны, которые участвуют в σ-связях, затем выше располагаются электроны, задействованные в π-связях, и только потом располагаются электроны, не участвующие в химических связях (н-электроны). Общая энергетическая картина расположения орбиталей приведена на рис. 6.29. Несвязывающие или разрыхляющие орбитали, обозначенные звездочкой расположены выше, причем π*-разрыхляющая орбиталь расположена ниже, чем σ*-разрыхляющая.
Наиболее длинноволновые переходы указаны стрелкой n→π* и соответствуют переходам неподеленной пары электрона из n-состояния на разрыхляющую π*-орбиталь кольца. После этого следуют переходы π→π*, обладающие значительно большей интенсивностью, чем n→π* переходы. В более коротковолновой области проявятся и другие, указанные стрелками на рис. 6.29 переходы.
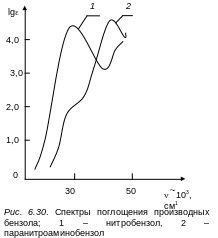
Рассмотрим спектры поглощения бензола типа XC6H5, где X-акцепторный или донорный заместитель, а также спектры бензола типа XC6H4Y с двумя заместителями, где X-донорный (D), а Y-акцепторный (А) заместители. Например, в спектре поглощения нитробензола C6H5NO2 в длинноволновой области наблюдается на фоне интенсивного поглощения перегиб (см. рис. 30, 1), который приписывается переходу n→π* неподеленной пары электронов азота на π*-разрыхляющую орбиталь кольца. При введении в n-положение молекулы бензола второй донорной группы, скажем NH2, мы получим молекулу н-нитроаминобензола, спектр которой существенно изменяется. В длинноволновой области возникает интенсивная полоса поглощения, которая интерпретируется как полоса переноса заряда от донорной группы NH2 к акцепторной NO2 через посредство сопряженной системы π-электронов кольца (рис. 6.30, 2). Природа заместителей X и Y существенно влияет на возможность проявления полос внутримолекулярного переноса заряда у дизамещенных бензола.
К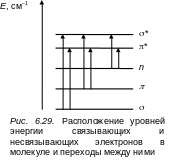 ак
видно на рис. 6.30, 2,
лишь при наличии в молекуле XC6H4Y
одновременно сильных D
и A
групп проявляются полосы внутримолекулярного
переноса заряда в заметно более
длинноволновой, чем у монозамещенных,
области (νлин 20200 ÷ 36300 см–1).
ак
видно на рис. 6.30, 2,
лишь при наличии в молекуле XC6H4Y
одновременно сильных D
и A
групп проявляются полосы внутримолекулярного
переноса заряда в заметно более
длинноволновой, чем у монозамещенных,
области (νлин 20200 ÷ 36300 см–1).
Такого
рода полоса отсутствует у дизамещенных
бензола при слабых D
(алкилы,
галогены) или слабых A
(–CH=CH2,
–C![]() CH)
заместителях. Однако введение заместителей
с сильной электроноакцепторной группой
(например, у таких соединений как
паранитроаминобензол) способствует
возникновению сильной полосы
внутримолекулярного переноса заряда
в длинноволновой области спектра.
CH)
заместителях. Однако введение заместителей
с сильной электроноакцепторной группой
(например, у таких соединений как
паранитроаминобензол) способствует
возникновению сильной полосы
внутримолекулярного переноса заряда
в длинноволновой области спектра.
Значение энергии максимума полосы Emax подчиняется зависимости
![]() ,
,
где
![]() –
потенциал ионизации донора,
–
потенциал ионизации донора,
![]() –
сродство к электрону А,
–
сродство к электрону А,
![]() – кулоновское взаимодействие между A
и D.
– кулоновское взаимодействие между A
и D.
У некоторых дизамещенных бензола состава DC6H4A наблюдается лишь одна полоса внутримолекулярного переноса заряда, тождественная с таковой у соответствующего C6H5A, а роль донорного заместителя сводится только к возмущению уровней π-электронной системы бензольного кольца. Очевидно, что это возможно лишь при слабых донорных заместителях, таких как алкины и галогены. В этом случае проявляется лишь одна полоса внутримолекулярного переноса заряда почти в той же области, что и у монозамещенного C6H5A. При сравнительно сильных заместителях D и A в длинноволновой области относительно полосы C6H5A проявляется достаточно интенсивная полоса внутримолекулярного переноса заряда.
Отнесение ее к полосе внутримолекулярного переноса заряда следует из того факта, что она более резко реагирует на внешние и внутренние возмущения молекулы.
Иногда у дизамещенных бензола обнаруживаются две полосы внутримолекулярного переноса заряда, одна из них соответствует полосе поглощения C6H5A, а вторая – DC6H4A. Указанные данные подтверждаются и результатами расчета изменения заряда Δq на атомах в различных возбужденных состояниях. Действительно, увеличение заряда на акцепторе в молекуле DC6H4A связана преимущественно с убылью его на доноре D. Наоборот, в молекуле C6H5A возрастание заряда на акцепторе связано с переносом его из бензольного кольца.
Введение в дизамещение бензола типа DC6H4A с сильными D и A третьего слабого заместителя (т.е. со слабым D'') не вызывает изменения числа полос и их характеристик. С усилением донорных свойств третьего заместителя D' могут наблюдаться в длинноволновой области уже три полосы. При этом характеристики всех полос внутримолекулярного переноса заряда подвергаются аналогичным изменениям как у ди- и монозамещённых бензола при действии на них растворителя и других реакционно способных реагентов.
Таким образом, у бензола и его замещённых в области 200–400 нм возможны полосы поглощения, связанные с электронными переходами в рамках определённой функциональной группы (n→π* или n→σ* переходы, связанные с переходами несвязывающих n-электронов на разрыхляющие π*- и σ*-орбитали кольца). Возможны переходы, связанные с переносом электронной плотности с одной функциональной группы (D) на другую (А) – полосы внутримолекулярного переноса заряда.
Полосы такого рода наблюдаются у ди- и более замещённых бензола и лишь у соединений, содержащих одновременно группы А и D, причём группы с низкой вакантной орбиталью у А и низким потенциалом ионизации n-электронов у D. Эти полосы обусловлены переходами электронов с верхней занятой орбитали группы D на разрыхляющую орбиталь группы А через сопряжённую систему электронов кольца. Справедливость этого заключения следует из отсутствия этих полос при связывании n-электронов донорной группы или при введении заместителя (углеродного радикала) между группой и кольцом.
