
- •Міністерство освіти і науки України Харківський національний університет імені в. Н. Каразіна Теоретичні основи та способи розв’язання задач з аналітичної хімії
- •Вступне слово
- •Основні позначення
- •1. Величини, що визначають склад
- •1.1. Хімічний склад
- •Розв’язок. Масова концентрація дорівнює
- •1.2. Стехіометричні розрахунки за рівнянням реакції
- •1.3. Вправи
- •2. Закон дії мас. Алгебра хімічних реакцій
- •2.1. Загальні співвідношення
- •2.2. Активності та рівноважні концентрації
- •Позначення констант рівноваг
- •2.3. Лінійні комбінації реакцій
- •2.4. У який бік зміщено рівновагу реакції?
- •2.5. Як записувати реакції у лабораторних журналах?
- •2.6. Вправи
- •3. Концентраційно-логарифмічні діаграми (клд)
- •3.1. Клд для гетерогенних систем
- •3.2. Графіки логарифмів розчинності
- •3.3. Вправи із гетерогенних систем
- •3.4. Умови переважання в гомогенних системах
- •3.5. Ускладнення у визначенні областей переважання
- •3.6. Клд для систем із одноядерними комплексами
- •3.7. Зміна ядерності реагентів
- •3.8. Вправи із гомогенних систем
- •4. Баланс компонентів
- •4.1. Загальні принципи
- •4.2. Підстановка рівнянь здм у рівняння балансу
- •4.3. Одноядерні продукти
- •4.4. Фази постійного складу
- •4.5. Вправи Гомогенні системи
- •5. Розрахунки за балансом компонентів
- •5.1. Буферні розчини
- •5.2. Стехіометричні співвідношення концентрацій
- •Кислотно-основні рівноваги
- •5.3. Ієрархія макро- та мікрокомпонентів
- •5.4. Гетерогенні системи
- •5.5. Кількісний вимір буферних властивостей
- •5.6. Вправи Буферні розчини
- •Стехіометричне співвідношення концентрацій
- •Гетерогенні системи
- •Буферні властивості
- •Системи із комплексами
- •6. Розрахунки за балансом реакції
- •6.1. Умови балансу
- •6.2. Прості розрахунки
- •Добуваючи квадратний корінь з обох частин, маємо
- •6.3. Методи розрахунків
- •6.4. Вправи
- •7. Умовні константи рівноваги
- •7.1. Класи реагентів
- •7.2. Умовні константи рівноваги
- •7.3. Умовні константи в розрахунках рівноваг
- •7.4. Графіки залежностей часток та їх логарифмів
- •7.5. Графіки логарифмів умовних констант
- •Параметри графіка залежності
- •7.6. Вправи
- •8. Декілька фаз змінного складу
- •8.1. Розподіл речовини між фазами
- •Відношення об’ємів порцій фаз дорівнює
- •Тангенси кутів нахилу асимптот для логарифма умовної константи екстракції оксинату плюмбуму від pH, приклад 8.4
- •8.2. Іонний обмін
- •8.3. Вправи
- •9. Утворення певної рівноважної концентрації, розчинності або ступеня екстракції
- •9.1. Метод балансу компонентів
- •На кроці 5 (непотрібному для уточнення клд) використовуємо
- •9.2. Метод балансу реакцій
- •9.3. Концентрація реагенту, що забезпечує задані умови для іншої речовини
- •9.4. Відокремлення компонентів Графічний розв’язок цієї проблеми показано на прикладі 3.3. Тут розгляньмо типові розрахункові методи.
- •9.5. Вибір величини умовної константи
- •9.6. Вправи
- •Варіанти завдання для вправи 9.1
- •10. Визначення компонентів. Гравіметрія
- •10.1. Стехіометричні співвідношення у гравіметрії
- •10.2. Розрахунок результату аналізу
- •10.3. Похибки у гравіметрії
- •10.4. Вправи
- •11. Титриметрія: стехіометричні розрахунки
- •11.1. Загальні відомості про титриметрію
- •11.2. Результат кислотно-основного титрування
- •Аліквотне відношення, {Vк/Vп}, безрозмірне, бо величини Vк та Vп виражено у однакових одиницях.
- •Виводячи формулу, маємо (у процентах)
- •11.3. Визначення концентрації розчину титранту за титруванням зразкової речовини
- •Для еквівалентів коефіцієнти вживаємо неявно,
- •Стехіометричний множник 2 приховуємо, застосовуючи еквівалент, (1/2)h2c2o4, або (1/2)h2c2o4·2h2o.
- •11.4. Оцінка наважок та аліквот
- •Бюретці відповідає оптимальна витрата титранту 20 мл, отже nst(oh‑) 2·10‑3 моль, n(н2с4н4о4) nst(oh‑) / 2 1·10‑3 моль.
- •11.5. Окреме визначення декількох аналітів
- •За двома рівняннями,
- •11.6. Зворотне титрування
- •Титруванню надлишку реагенту відповідає реакція
- •Дія 4. Масова частка CaCo3(s) у мінералі дорівнює
- •11.7. Визначення продукту, в який перетворено аналіт
- •Бо при зворотному титруванні здобутий po43‑ знову переходить у hpo42‑. Надлишок реагенту титруємо за реакцією
- •Дія 5. Масова частка p2o5 у мінералі дорівнює
- •11.8. Окисно-відновне титрування
- •11.9. Комплексометричне титрування
- •Дія 4. Масова частка kAl(so4)2 12 h2o у технічному галуні ‑
- •11.10. Вправи
- •Окисно-відновне титрування
- •Комплексонометричне титрування
- •12. Титриметрія: розбіжність точок –стехіометрії та кінцевої
- •12.1. Загальні уявлення
- •12.2. Дослідження титрування безпосередньо за клд
- •12.3. Різні методи титрування
- •12.4. Класи та умовні константи у титруванні
- •12.5. Вибір умов титрування за графіками залежностей логарифмів умовних констант
- •Параметри асимптот для прикладу 12.10
- •Із здм реакції
- •Параметри асимптот графіків (приклад 12.11)
- •Параметри асимптот графіків (приклад 12.12)
- •12.6. Вправи
- •Кислотно-основне титрування
- •Окисно-відновне титрування
- •Комплексонометричне титрування
- •Теоретичні проблеми титрування
- •Цитована література
- •Відповіді до вправ
- •61077, М.Харків, пл. Свободи, 4 Харківський національний університет ім. В.Н. Каразіна, Організаційно-видавничий відділ нмц
Відношення об’ємів порцій фаз дорівнює
w = 20 мл / (1 л 1000 мл/л) = 0,020.
Використовуємо умовну константу, розраховану для рН = 5 у прикладі 8.3, K’D(HOxin| H+) = 250. Згідно (8.8), концентрація після n-ї екстракції дорівнює
[HOxin| H+]n = [HOxin| H+]0 / (1 + K’D(HOxin| H+) w)n.
За умовою, [HOxin| H+]n cmin. Підставляючи числа, маємо
lg [HOxin| H+]n = lg [HOxin| H+]0 – n lg (1 + K’D(HOxin| H+) w) lg (cmin), lg (1.10‑3) ‑ n lg (1 + 250 0,020) lg (110‑8),
n [lg (1.10‑3) ‑ lg (110‑8)] / lg (1 + 250 0,020) =
= [(‑3) – (‑8)] / lg (1 + 5) = 5 / 0,778 = 6,4.
Оскільки число послідовних екстракцій має бути цілим, воно щонайменше дорівнює n = 7.
Приклад 8.5. Залежність логарифма умовної константи екстракції оксихінолінату плюмбуму від pH (розчинник ‑ CHCl3).
Розв’язок. Іон 8-оксихіноліну утворює комплекси із багатьма іонами металів. Їх використовують для відокремлення відповідних компонентів або у тверді фази, або в екстракти. Для екстракції плюмбуму(ІІ) маємо
Pb2+ + 2
![]() + 2 H+, lg Kex = ‑ 8,0.
+ 2 H+, lg Kex = ‑ 8,0.
Для залежності логарифма умовної константи,
lg K’ex( | H+) = lg Kex + lg r(Pb2+| H+) + 2 lg r( | H+) + 2 pH,
графік будуємо за алгоритмом із розділу 7.5. Оскільки { | H+} = { }, член – lg r( | H+) = 0 й тому опущений у формулі.
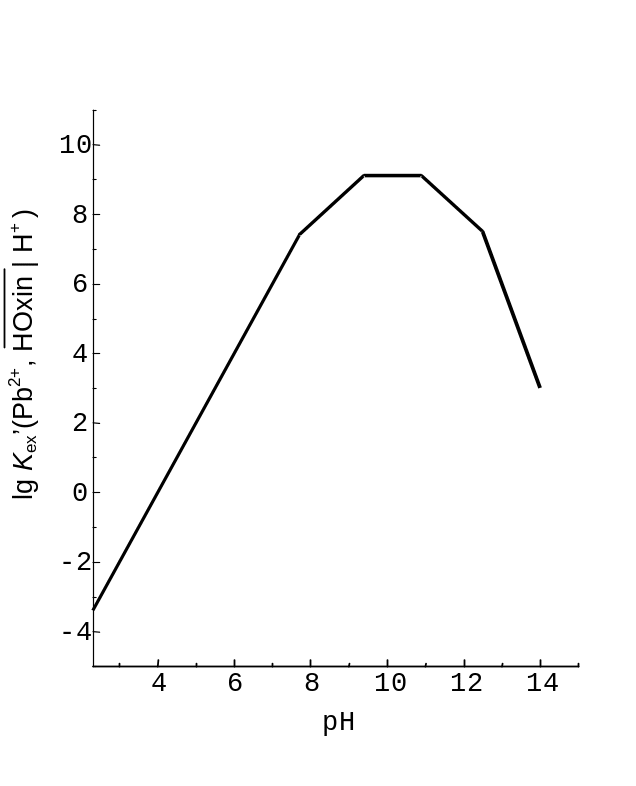
Рис. 8.4. Залежність логарифма умовної константи екстракції оксинату свинцю від рН (двофазна система CHCl3 - H2O).
Крок 1 – границі областей переважання представників класів. Логарифми констант ЗДМ для реакцій, що відповідають гідроксокомплексам, дорівнюють: lg *K1 = ‑ 7,7, lg *K2 = ‑ 9,4, lg *K3 = ‑ 10,9. Ці величини із зворотним знаком є pH границь областей переважання. Константи для класу { | H+} наведено у прикладі 8.3. Розгляньмо перетворення
+ i H+ Hi+1Oxini+, i = ‑ 1, 0, 1.
При i = 0 це розподіл HOxin, lg K0 = ‑ 2,66. Із лінійних комбінацій обчислюємо lg K‑1 = ‑ 12,47, lg K1 = 2,25.
Концентрацію класу відносимо до об’єму водяного розчину. Оскільки K0 є малою, нехтуємо [HOxin] у воді порівняно із [ ]. На границях областей переважання pH дорівнюють (‑ lg K‑1) та lg K1.
Кроки 2-4 аналогічні розглянутим у розділі 7.5. Числові дані наведено в табл. 8.1. Ордината горизонтального відрізка дорівнює логарифмові константи реакції між переважаючими представниками класів,
1 |
Pb2++2 |
+ 2 H+ |
‑8,0 |
1 |
Pb(OH)2 + 2 H+ |
Pb2+ + 2 H2O |
17,1 |
Pb(OH)2 +2 |
+ 2 H2O |
9,1 |
|
Крок 5. Праворуч та ліворуч від горизонтального відрізка ламаної проведімо відрізки, нахили й границі яких наведені у табл. 8.1. Не проведені на рис. 8.4 спряження (крок 6) лежали б на lg 2 0,3 нижче за зломи наближеного графіка. Спряження при pH = 2,3 та pH = 12,5, відповідні lg r( | H+), лежать на 2 lg 2 0,6 нижче за точки злому, бо у реакції при коефіцієнт (‑ 2).
Таблиця 8.1
Тангенси кутів нахилу асимптот для логарифма умовної константи екстракції оксинату плюмбуму від pH, приклад 8.4
р |
tg ψ(Pb2+) |
2 tgψ (HOxin) |
‑2 tgψ (H+) |
tg ψ |
Ордината кінця інтервалу |
|
Від |
До |
|||||
… |
2,3 |
0 |
2 |
2 |
4 |
-3,4 |
2,3 |
7,7 |
0 |
0 |
2 |
2 |
7,4 |
7,7 |
9,4 |
-1 |
0 |
2 |
1 |
9,1 |
9,4 |
10,9 |
-2 |
0 |
2 |
0 |
9,1 |
10,9 |
12,5 |
-3 |
0 |
2 |
-1 |
7,5 |
12,5 |
… |
-3 |
-2 |
2 |
-3 |
3,0 (pH = 14) |
Приклад 8.6. Екстракція Br2 із водяного розчину c(KBr) = = 0,010 моль/л у фазу тетрахлориду карбону, CCl4, при t(Br2) = = 0,10 моль/л, V = 1,00 л, = 100 мл.
Розв’язок. Реакції у системі –
Br2 ![]() lg KD = 1,25; Br‑ + Br2 Br3‑, lg = 1,44.
lg KD = 1,25; Br‑ + Br2 Br3‑, lg = 1,44.
У класі {Br2| w}, при w = (0,100 л) / (1,00 л) = 0,10,
r(Br2| w) = 1 / (1 + KD w) = 1 / (1 + 101,25·0,10) = 1 / 2,778, lg r(Br2| w) = ‑0,444, lg ’( | w) = lg + lg r(Br2| w) = 1,44 ‑ 0,444 = 0,996.
Переважаючий компонент – це {Br2| w}, бо [Br2| w] перевищує [Br2] чи [ #]. Замість розв’язку для реакцій
Br2 + Br‑ Br3‑ та Br2 ,
що потребував би ітеративного уточнення, досить однієї реакції,
{Br2| w} |
+ Br‑ |
Br3‑ |
lg ’( |w) = 0,996 |
|
c |
0,10 |
0,010 |
0 |
|
[ ] |
0,10‑x |
0,010‑x |
x. |
|
Із повного квадратного рівняння одержимо:
x = [Br3‑] = 4,8510‑3 4,910‑3 моль/л, [Br‑] 5,110‑3 моль/л,
[Br2| w] = 0,09515 моль/л, [Br2] = [Br2| w] r(Br2) 0,034 моль/л,
а далі, на кроці 3 алгоритму,
[ #] = [Br2| w] r( #) = 0,0609 0,061 моль/л,
[Br2] = [ #] / w 0,61 моль/л.
