
- •Міністерство освіти і науки України Харківський національний університет імені в. Н. Каразіна Теоретичні основи та способи розв’язання задач з аналітичної хімії
- •Вступне слово
- •Основні позначення
- •1. Величини, що визначають склад
- •1.1. Хімічний склад
- •Розв’язок. Масова концентрація дорівнює
- •1.2. Стехіометричні розрахунки за рівнянням реакції
- •1.3. Вправи
- •2. Закон дії мас. Алгебра хімічних реакцій
- •2.1. Загальні співвідношення
- •2.2. Активності та рівноважні концентрації
- •Позначення констант рівноваг
- •2.3. Лінійні комбінації реакцій
- •2.4. У який бік зміщено рівновагу реакції?
- •2.5. Як записувати реакції у лабораторних журналах?
- •2.6. Вправи
- •3. Концентраційно-логарифмічні діаграми (клд)
- •3.1. Клд для гетерогенних систем
- •3.2. Графіки логарифмів розчинності
- •3.3. Вправи із гетерогенних систем
- •3.4. Умови переважання в гомогенних системах
- •3.5. Ускладнення у визначенні областей переважання
- •3.6. Клд для систем із одноядерними комплексами
- •3.7. Зміна ядерності реагентів
- •3.8. Вправи із гомогенних систем
- •4. Баланс компонентів
- •4.1. Загальні принципи
- •4.2. Підстановка рівнянь здм у рівняння балансу
- •4.3. Одноядерні продукти
- •4.4. Фази постійного складу
- •4.5. Вправи Гомогенні системи
- •5. Розрахунки за балансом компонентів
- •5.1. Буферні розчини
- •5.2. Стехіометричні співвідношення концентрацій
- •Кислотно-основні рівноваги
- •5.3. Ієрархія макро- та мікрокомпонентів
- •5.4. Гетерогенні системи
- •5.5. Кількісний вимір буферних властивостей
- •5.6. Вправи Буферні розчини
- •Стехіометричне співвідношення концентрацій
- •Гетерогенні системи
- •Буферні властивості
- •Системи із комплексами
- •6. Розрахунки за балансом реакції
- •6.1. Умови балансу
- •6.2. Прості розрахунки
- •Добуваючи квадратний корінь з обох частин, маємо
- •6.3. Методи розрахунків
- •6.4. Вправи
- •7. Умовні константи рівноваги
- •7.1. Класи реагентів
- •7.2. Умовні константи рівноваги
- •7.3. Умовні константи в розрахунках рівноваг
- •7.4. Графіки залежностей часток та їх логарифмів
- •7.5. Графіки логарифмів умовних констант
- •Параметри графіка залежності
- •7.6. Вправи
- •8. Декілька фаз змінного складу
- •8.1. Розподіл речовини між фазами
- •Відношення об’ємів порцій фаз дорівнює
- •Тангенси кутів нахилу асимптот для логарифма умовної константи екстракції оксинату плюмбуму від pH, приклад 8.4
- •8.2. Іонний обмін
- •8.3. Вправи
- •9. Утворення певної рівноважної концентрації, розчинності або ступеня екстракції
- •9.1. Метод балансу компонентів
- •На кроці 5 (непотрібному для уточнення клд) використовуємо
- •9.2. Метод балансу реакцій
- •9.3. Концентрація реагенту, що забезпечує задані умови для іншої речовини
- •9.4. Відокремлення компонентів Графічний розв’язок цієї проблеми показано на прикладі 3.3. Тут розгляньмо типові розрахункові методи.
- •9.5. Вибір величини умовної константи
- •9.6. Вправи
- •Варіанти завдання для вправи 9.1
- •10. Визначення компонентів. Гравіметрія
- •10.1. Стехіометричні співвідношення у гравіметрії
- •10.2. Розрахунок результату аналізу
- •10.3. Похибки у гравіметрії
- •10.4. Вправи
- •11. Титриметрія: стехіометричні розрахунки
- •11.1. Загальні відомості про титриметрію
- •11.2. Результат кислотно-основного титрування
- •Аліквотне відношення, {Vк/Vп}, безрозмірне, бо величини Vк та Vп виражено у однакових одиницях.
- •Виводячи формулу, маємо (у процентах)
- •11.3. Визначення концентрації розчину титранту за титруванням зразкової речовини
- •Для еквівалентів коефіцієнти вживаємо неявно,
- •Стехіометричний множник 2 приховуємо, застосовуючи еквівалент, (1/2)h2c2o4, або (1/2)h2c2o4·2h2o.
- •11.4. Оцінка наважок та аліквот
- •Бюретці відповідає оптимальна витрата титранту 20 мл, отже nst(oh‑) 2·10‑3 моль, n(н2с4н4о4) nst(oh‑) / 2 1·10‑3 моль.
- •11.5. Окреме визначення декількох аналітів
- •За двома рівняннями,
- •11.6. Зворотне титрування
- •Титруванню надлишку реагенту відповідає реакція
- •Дія 4. Масова частка CaCo3(s) у мінералі дорівнює
- •11.7. Визначення продукту, в який перетворено аналіт
- •Бо при зворотному титруванні здобутий po43‑ знову переходить у hpo42‑. Надлишок реагенту титруємо за реакцією
- •Дія 5. Масова частка p2o5 у мінералі дорівнює
- •11.8. Окисно-відновне титрування
- •11.9. Комплексометричне титрування
- •Дія 4. Масова частка kAl(so4)2 12 h2o у технічному галуні ‑
- •11.10. Вправи
- •Окисно-відновне титрування
- •Комплексонометричне титрування
- •12. Титриметрія: розбіжність точок –стехіометрії та кінцевої
- •12.1. Загальні уявлення
- •12.2. Дослідження титрування безпосередньо за клд
- •12.3. Різні методи титрування
- •12.4. Класи та умовні константи у титруванні
- •12.5. Вибір умов титрування за графіками залежностей логарифмів умовних констант
- •Параметри асимптот для прикладу 12.10
- •Із здм реакції
- •Параметри асимптот графіків (приклад 12.11)
- •Параметри асимптот графіків (приклад 12.12)
- •12.6. Вправи
- •Кислотно-основне титрування
- •Окисно-відновне титрування
- •Комплексонометричне титрування
- •Теоретичні проблеми титрування
- •Цитована література
- •Відповіді до вправ
- •61077, М.Харків, пл. Свободи, 4 Харківський національний університет ім. В.Н. Каразіна, Організаційно-видавничий відділ нмц
7.4. Графіки залежностей часток та їх логарифмів
Графіки часток.У середині області переважання частинки MLi маємо [MLi] [MLi| L], r(MLi| L) 1, й графік r(MLi| L) є близьким до горизонтальної асимптоти. Зовні області [MLi] << [MLi| L], r(MLi| L) 0. В околі границі області переважання помітна різниця r(MLi| L) від 1 та 0.
Якщо вихід тільки двох сортів частинок є істотним, то графіки є однотипними, їх можна будувати за шаблоном, не повторюючи розрахунків, і графіки є симетричними відносно точки r(MLi| L) = 0,5.
Приклад 7.11. Залежність часток r(Ac‑| H+) та r(HAc| H+) від pH.
Розв’язок. Позначмо h = [H+], K = KHc. Тоді
r(Ac‑| H+) = 1 / (1 + K h) = 1 / {1 + 10(lg K‑pH)}, r(HAc| H+) = K h / (1 + K h) = 10(lg K‑pH) / {1 + 10(lg K‑pH)}.
Асимптоти графіків, r(HiAc| H+) 1 (для переважаючої частинки) й r(HiAc| H+) 0 (для непереважаючої). Графіки будуємо за обчисленими значеннями функцій в околі їх точки перетину, pH = lg KH (рис. 7.1).
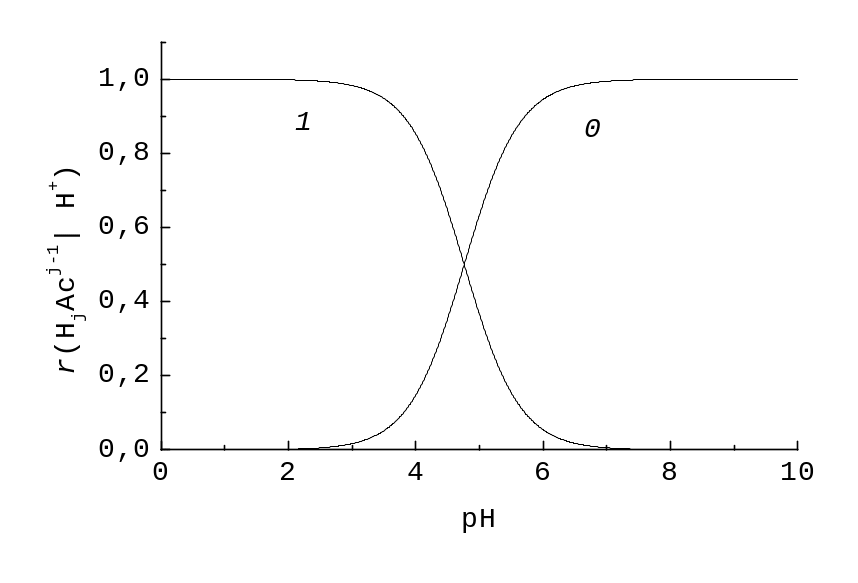
Рис. 7.1. Залежність часток r(HjAc j‑1| H+) у класі {Ac ‑| H+} від pH. Індекси біля кривих відповідають j.
Приклад 7.12. Залежність часток у класі {C2O42‑| H+} від pH.
Розв’язок. Функції (із lg H1 = 4,27 та lg H2 = 5,52),
r(C2O42‑| H+) = 1 / (1 + H1 h + H2 h2), r(HC2O4‑| H+) = = H1 h / (1 + H1 h + H2 h2), r(H2C2O4| H+) = H2 h2 / (1 + H1 h + H2 h2).
Їх графіки нагадують рис. 7.1 зі зміною положення кривих відносно шкали абсцис. На рис. 7.2b подано графіки сум часток,
![]() r(MLk| L) =
k [L]k /
k [L]k,
r(MLk| L) =
k [L]k /
k [L]k,
де часткам r(MLk| L) відповідають відрізки, на які лінії графіка поділяють вертикальну пряму. При pH = H2 / 2 = 2,76 обчислюємо:
r(C2O42‑| H+) = r(H2C2O4| H+) = 0,029, r(HC2O4‑| H+) = 0,972.
Враховуючи у знаменниках лише найбільші доданки, ми б одержали 0,030 та 0,970, що у масштабі графіків не відрізняються від точних значень, і можна перенести криві з рис. 7.1 на 7.2a, змінивши абсциси. На рис. 7.2b наведено графіки сум часток.
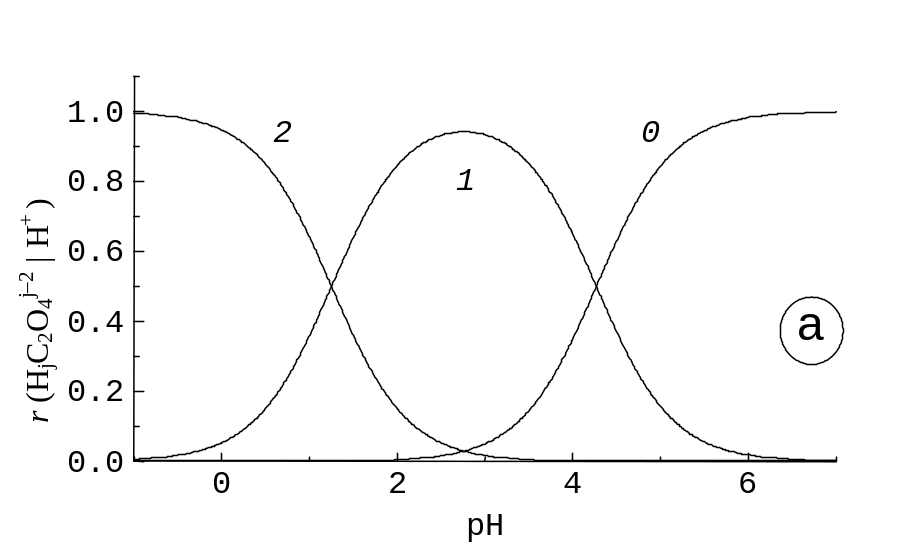
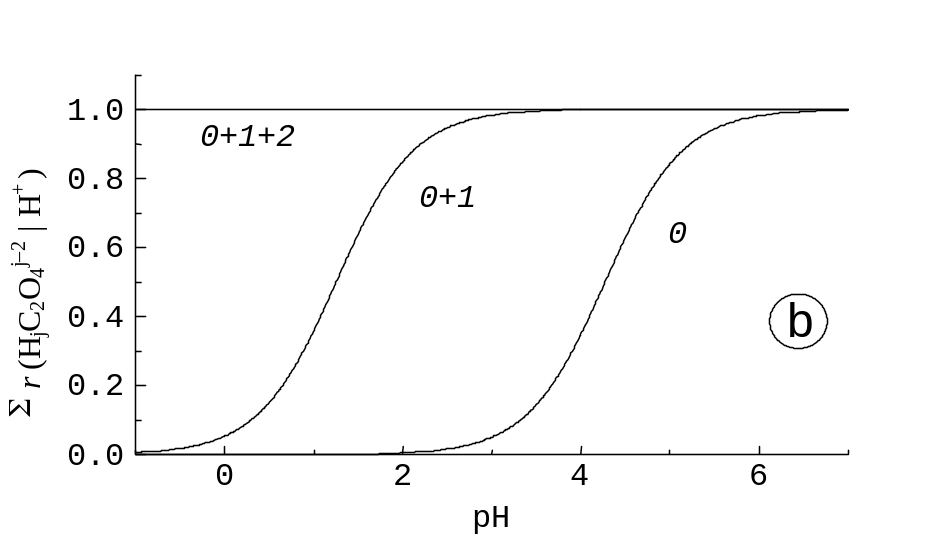 Рис.
7.2. Залежність від pH у класі {C2O42‑| H+}:
(a) часток r(HjC2O4j‑2|
H+),
індекси j
біля кривих, (b) сум часток
r(HjC2O4j‑2| H+);
індекси, біля кривих, сполучені знаком
+, відповідають тим j,
що увійшли в суми.
Рис.
7.2. Залежність від pH у класі {C2O42‑| H+}:
(a) часток r(HjC2O4j‑2|
H+),
індекси j
біля кривих, (b) сум часток
r(HjC2O4j‑2| H+);
індекси, біля кривих, сполучені знаком
+, відповідають тим j,
що увійшли в суми.
Таблиця 7.2
Залежність часток rn = r(Ag(NH3)n+), n = 0, 1, 2, від pNH3. l = [NH3],lg K1 = 3,31, lg K2 = 3,91, (lg 2) / 2 = 3,61
pNH3 |
1 l |
2 l2 |
1 + 1 l +2 l2 |
r0 |
r1 |
r2 |
2,5 |
6,46 |
166 |
173 |
0,006 |
0,037 |
0,957 |
3,0 |
2,04 |
16,6 |
19,6 |
0,051 |
0,104 |
0,845 |
3,31 |
1,00 |
3,98 |
5,98 |
0,167 |
0,167 |
0,67 |
3,61 |
0,50 |
1,00 |
2,50 |
0,40 |
0,20 |
0,40 |
3,91 |
0,25 |
0,25 |
1,50 |
0,67 |
0,167 |
0,167 |
4,5 |
0,065 |
0,017 |
1,08 |
0,925 |
0,060 |
0,015 |
Приклад 7.13. Залежність часток представників класу {Ag+| NH3} від pNH3.
Розв’язок. Біля границі областей переважання Ag+ та Ag(NH3)2+ вихід усіх форм є сумірним. Розрахунок часток у околі ТС (при lg 1 = 3,31, lg 2 = 7,22) подано у табл. 7.2.
За його результатами побудовано рис. 7.3.
 Рис.7.3.
Залежність від pNH3
часток r(Ag(NH3)j+|NH3)
представників класу {Ag+| NH3}.Індекси
біля кривих відповідають j.
Рис.7.3.
Залежність від pNH3
часток r(Ag(NH3)j+|NH3)
представників класу {Ag+| NH3}.Індекси
біля кривих відповідають j.
Графіки логарифмів часток. На графіках r(MLi| L) не видно відносних змін часток в областях, де ці частки є близькими до 0. Цього недоліку позбавлені графіки логарифмів часток, lg r(MLi| L) = lg [MLi] – lg [M| L], що відрізняються від графіків КЛД зміщенням за віссю ординат на –lg [M| L], ТС тут лягають на вісь абсцис (рис. 7.4 та 7.5).
Алгоритм побудови графіків логарифмів часток відрізняється від алгоритму для КЛД ординатами ТС:
1. Обчислити значення головної змінної, pL, на границях областей переважання комплексів.
2. Почати наближений графік lg r(MLk| L) із горизонтального відрізка на осі абсцис (pL), кінці якого на границях області переважання MLi. Якщо MLi ніде не переважає, то графік почати із точки на границі областей переважання комплексів, найближчих за складом до MLk.
3. Продовжити графік неперервною ламаною у область переважання інших комплексів, MLi. Тангенс кута нахилу відрізка ламаної дорівнює (i ‑ k), різниці індексів при L для частинки MLi, що переважає у відповідній області, та MLk. Кінець відрізка – на границях областей переважання.
4. Якщо потрібно уточнити графіки, то замінити зломи плавними спряженнями, що відхиляються від злому за ординатою на = ‑lg j, де j – число сортів частинок, концентрації яких майже однакові у відповідній ТС.
Приклад 7.14. Залежність логарифма частки іона етилендіамінтетраацетату, Y4‑, від pH.
Розв’язок. Для кислотно-основних перетворень іона Y4‑: lg KH1 = 10,17, lg KH2 = 6,11, lg KH3 = 2,68, lg KH4 = 2,0, lg KH5 = 1,5.
Як і КЛД, наближений графік lg r(Y4‑| H+) є ламаною (рис. 7.5). Його починаємо з правої гілки (максимуму), що збігається із віссю абсцис. Лівіше за ТС, при pH < lg KH1, переходимо в похилу із тангенсом кута нахилу 1, тут переважає HY3‑. Лівіше за наступну ТС, при pH < lg KH2, тангенс дорівнює 2, і т. д. Точки злому (табл. 7.3, останній стовпчик – ординати кінця інтервалів) з’єднуємо відрізками прямих.
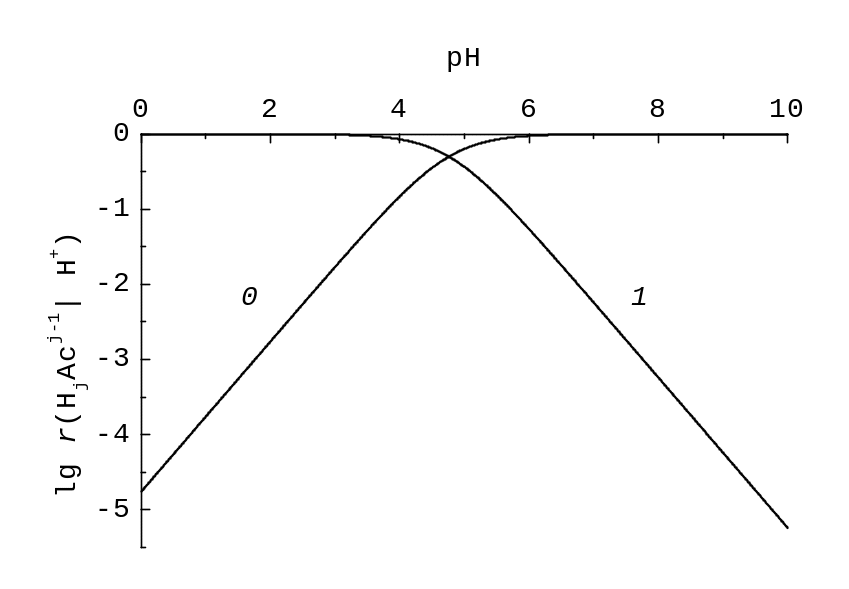 Рис.
7.4. Залежність логарифмів часток
lg r(Ac‑| H+)
та lg r (HAc| H+)
у класі {Ac‑| H+}
від pH. Цифри біля кривих – індекси j
у формулі HjAcj‑1.
Рис.
7.4. Залежність логарифмів часток
lg r(Ac‑| H+)
та lg r (HAc| H+)
у класі {Ac‑| H+}
від pH. Цифри біля кривих – індекси j
у формулі HjAcj‑1.
