
- •Міністерство освіти і науки України Харківський національний університет імені в. Н. Каразіна Теоретичні основи та способи розв’язання задач з аналітичної хімії
- •Вступне слово
- •Основні позначення
- •1. Величини, що визначають склад
- •1.1. Хімічний склад
- •Розв’язок. Масова концентрація дорівнює
- •1.2. Стехіометричні розрахунки за рівнянням реакції
- •1.3. Вправи
- •2. Закон дії мас. Алгебра хімічних реакцій
- •2.1. Загальні співвідношення
- •2.2. Активності та рівноважні концентрації
- •Позначення констант рівноваг
- •2.3. Лінійні комбінації реакцій
- •2.4. У який бік зміщено рівновагу реакції?
- •2.5. Як записувати реакції у лабораторних журналах?
- •2.6. Вправи
- •3. Концентраційно-логарифмічні діаграми (клд)
- •3.1. Клд для гетерогенних систем
- •3.2. Графіки логарифмів розчинності
- •3.3. Вправи із гетерогенних систем
- •3.4. Умови переважання в гомогенних системах
- •3.5. Ускладнення у визначенні областей переважання
- •3.6. Клд для систем із одноядерними комплексами
- •3.7. Зміна ядерності реагентів
- •3.8. Вправи із гомогенних систем
- •4. Баланс компонентів
- •4.1. Загальні принципи
- •4.2. Підстановка рівнянь здм у рівняння балансу
- •4.3. Одноядерні продукти
- •4.4. Фази постійного складу
- •4.5. Вправи Гомогенні системи
- •5. Розрахунки за балансом компонентів
- •5.1. Буферні розчини
- •5.2. Стехіометричні співвідношення концентрацій
- •Кислотно-основні рівноваги
- •5.3. Ієрархія макро- та мікрокомпонентів
- •5.4. Гетерогенні системи
- •5.5. Кількісний вимір буферних властивостей
- •5.6. Вправи Буферні розчини
- •Стехіометричне співвідношення концентрацій
- •Гетерогенні системи
- •Буферні властивості
- •Системи із комплексами
- •6. Розрахунки за балансом реакції
- •6.1. Умови балансу
- •6.2. Прості розрахунки
- •Добуваючи квадратний корінь з обох частин, маємо
- •6.3. Методи розрахунків
- •6.4. Вправи
- •7. Умовні константи рівноваги
- •7.1. Класи реагентів
- •7.2. Умовні константи рівноваги
- •7.3. Умовні константи в розрахунках рівноваг
- •7.4. Графіки залежностей часток та їх логарифмів
- •7.5. Графіки логарифмів умовних констант
- •Параметри графіка залежності
- •7.6. Вправи
- •8. Декілька фаз змінного складу
- •8.1. Розподіл речовини між фазами
- •Відношення об’ємів порцій фаз дорівнює
- •Тангенси кутів нахилу асимптот для логарифма умовної константи екстракції оксинату плюмбуму від pH, приклад 8.4
- •8.2. Іонний обмін
- •8.3. Вправи
- •9. Утворення певної рівноважної концентрації, розчинності або ступеня екстракції
- •9.1. Метод балансу компонентів
- •На кроці 5 (непотрібному для уточнення клд) використовуємо
- •9.2. Метод балансу реакцій
- •9.3. Концентрація реагенту, що забезпечує задані умови для іншої речовини
- •9.4. Відокремлення компонентів Графічний розв’язок цієї проблеми показано на прикладі 3.3. Тут розгляньмо типові розрахункові методи.
- •9.5. Вибір величини умовної константи
- •9.6. Вправи
- •Варіанти завдання для вправи 9.1
- •10. Визначення компонентів. Гравіметрія
- •10.1. Стехіометричні співвідношення у гравіметрії
- •10.2. Розрахунок результату аналізу
- •10.3. Похибки у гравіметрії
- •10.4. Вправи
- •11. Титриметрія: стехіометричні розрахунки
- •11.1. Загальні відомості про титриметрію
- •11.2. Результат кислотно-основного титрування
- •Аліквотне відношення, {Vк/Vп}, безрозмірне, бо величини Vк та Vп виражено у однакових одиницях.
- •Виводячи формулу, маємо (у процентах)
- •11.3. Визначення концентрації розчину титранту за титруванням зразкової речовини
- •Для еквівалентів коефіцієнти вживаємо неявно,
- •Стехіометричний множник 2 приховуємо, застосовуючи еквівалент, (1/2)h2c2o4, або (1/2)h2c2o4·2h2o.
- •11.4. Оцінка наважок та аліквот
- •Бюретці відповідає оптимальна витрата титранту 20 мл, отже nst(oh‑) 2·10‑3 моль, n(н2с4н4о4) nst(oh‑) / 2 1·10‑3 моль.
- •11.5. Окреме визначення декількох аналітів
- •За двома рівняннями,
- •11.6. Зворотне титрування
- •Титруванню надлишку реагенту відповідає реакція
- •Дія 4. Масова частка CaCo3(s) у мінералі дорівнює
- •11.7. Визначення продукту, в який перетворено аналіт
- •Бо при зворотному титруванні здобутий po43‑ знову переходить у hpo42‑. Надлишок реагенту титруємо за реакцією
- •Дія 5. Масова частка p2o5 у мінералі дорівнює
- •11.8. Окисно-відновне титрування
- •11.9. Комплексометричне титрування
- •Дія 4. Масова частка kAl(so4)2 12 h2o у технічному галуні ‑
- •11.10. Вправи
- •Окисно-відновне титрування
- •Комплексонометричне титрування
- •12. Титриметрія: розбіжність точок –стехіометрії та кінцевої
- •12.1. Загальні уявлення
- •12.2. Дослідження титрування безпосередньо за клд
- •12.3. Різні методи титрування
- •12.4. Класи та умовні константи у титруванні
- •12.5. Вибір умов титрування за графіками залежностей логарифмів умовних констант
- •Параметри асимптот для прикладу 12.10
- •Із здм реакції
- •Параметри асимптот графіків (приклад 12.11)
- •Параметри асимптот графіків (приклад 12.12)
- •12.6. Вправи
- •Кислотно-основне титрування
- •Окисно-відновне титрування
- •Комплексонометричне титрування
- •Теоретичні проблеми титрування
- •Цитована література
- •Відповіді до вправ
- •61077, М.Харків, пл. Свободи, 4 Харківський національний університет ім. В.Н. Каразіна, Організаційно-видавничий відділ нмц
3.7. Зміна ядерності реагентів
Розгляньмо реакцію
q Q + X r R, (3.10)
де стехіометричні коефіцієнти q r. Якщо реакція пройде повністю праворуч, увесь реагент Q перейде у R, а якщо ліворуч, то R у Q. Ядерність змінюється, й висота горизонтальних відрізків lg [Q] та lg [R] різна. Запобігаючи цьому, функції пов’язуємо із рівноважними концентраціями еквівалентів qQ та rR, що в реакції втрачають або приєднують одну частинку X. Ці величини пропорційні концентраціям реагентів,
[qQ] = (1 / q) [Q], [rR] = (1 / r) [R]. (3.11a)
Графіки логарифмів рівноважних концентрацій еквівалентів,
lg [qQ] = lg [Q] ‑ lg q, lg [rR] = lg [R] – lg r, (3.11b)
йдуть паралельно до графіків lg [Q] та lg [R]. Нехтуючи одним із доданків у виразі загальної концентрації еквівалента,
t = t(qQ) = (1 / q) t(Q) = [qQ] + [rR], (3.12)
маємо наближений графік логарифма другого доданка – відрізок горизонтальної прямої із ординатою lg t. Відрізки графіків lg [qQ] та lg [rR] уже на однаковій висоті, графік зручний та звичний.
Приклад 3.10. КЛД для t(S2O32‑) = t = 0,050 моль/л, головна змінна pe.
Розв’язок. Тут X – електрон e‑,
S4O62‑ + 2 e‑ 2 S2O32‑, Eo = 0,08 В, lg K = 2 Eo / k = 3,0,
q = 1/2, r = 1. У системах із зміною ядерності ТС не збігається ні з lg K, ні з (1/2) lg K. Обчислімо головну змінну в точці системи, peТС. З лівого боку від ТС [S2O32‑] t = 0,050 моль/л, а з правого, після граничного зсуву за схемою
2 S2O32‑ |
‑ 2 e‑ S4O62‑, |
|||
c |
0,050 |
– |
0 |
|
clim |
‑2 xlim |
– |
xlim |
xlim = 0,059 / 2 = 0,025, |
clim |
0 |
– |
0,025 |
|
маємо удвічі меншу молярну концентрацію, [S4O62‑] t / 2 = = 0,025 моль/л.
Підставмо ці значення у ЗДМ,
[S2O32‑]2 / {[S4O62‑] aе2} = K,
peТС = (1/2) lg K + (1/2) lg (t/2) ‑ lg t = 1,5 – 0,15 +(1/2) lg (t/2) =
= 1,35 ‑ (1/2) lg t = 2,0.
Ця абсциса залежить від t. Графік її як функції lg t проведено на рис. 3.7 пунктиром. У нашій системі ординатою є
lg t = ‑1,3.
Графік lg [S2O32‑] почнімо горизонтальним променем лівіше за ТС. Його продовжуємо правіше за ТС променем із тангенсом кута нахилу (‑1). Визначмо нахил, не посилаючись на крок 4 алгоритму. Згідно із ЗДМ реакції для однієї не переважаючої S2O32‑,
(1/2) S4O62‑ + e‑ S2O32‑,
тангенс дорівнює коефіцієнтові при електроні із оберненим знаком.
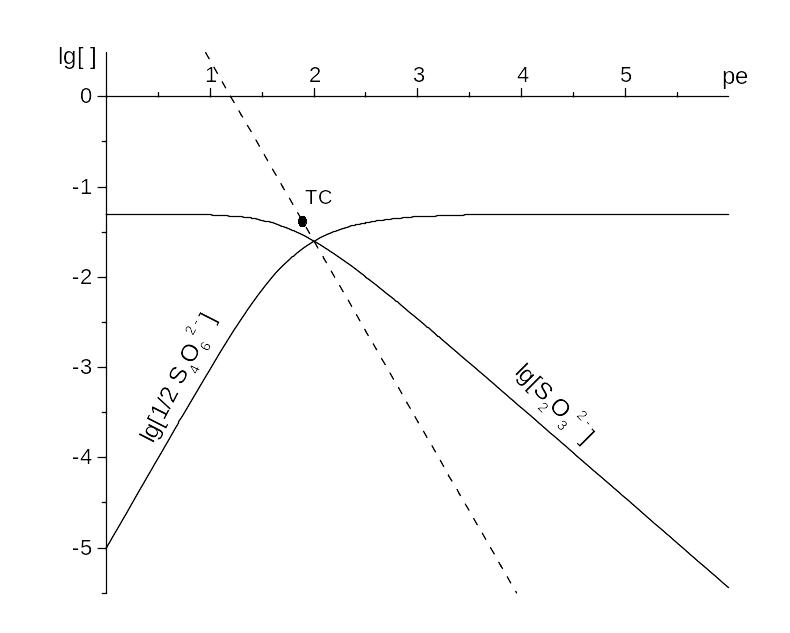
Рис. 3.7. КЛД для системи S2O32‑ – S4O62‑, головна змінна ре. Геометричне місце точок системи відзначено пунктиром.
Графік lg [(1/2) S4O62‑] почнімо горизонтальним променем правіше за ТС. Його продовжимо променем із тангенсом кута нахилу 2, згідно із коефіцієнтом при електроні у реакції, де продуктом є одна частинка S4O62‑,
2 S2O32‑ ‑ 2 е‑ S4O62‑.
Уточнюючи КЛД, спряження ламаних перетинаємо на 0,3 нижче за ТС, при lg [ ] = lg (t / 2). У системі, де змінюється ядерність, точка перетину лежить не під ТС, а на пунктирній прямій. Абсциса точки перетину відповідає формулі, аналогічній формулі для peТС, із підстановкою замість t величини [(1/2) S4O62‑] = [S2O32‑] = t / 2 = 0,025 моль/л,
pe = 1,35 ‑ (1/2) lg (t / 2) = 2,15.
Спряження на графіках. Для реакції (3.10)
pXТС = lg K + q lg q - r lg r + (q - r) lg t. (3.13)
Абсцисі точки перетину відповідатиме pX, у розрахунку якого lg t замінено на lg (t / j), де j описане у кроці 5 загального алгоритму. Точка перетину графіків зміщується за абсцисою на (q ‑ r) lg j. Підраховуючи pXТС за ЗДМ для конкретної реакції, як у прикладі 3.10, важче помилитися, ніж за загальною формулою (ще розберіться, чому відповідають абстрактні символи!).
