
- •Шкільний курс хімії та методика його викладання
- •Визначення номерів завдань самостійної роботи (інваріантна складова)
- •Зміст дисципліни
- •Модульна програма дисципліни модуль 1
- •Лабораторні заняття
- •Модуль 2
- •Лабораторні заняття
- •Модуль 3
- •Лабораторні заняття
- •Модуль 4
- •Лабораторні заняття
- •Модуль 5
- •Лабораторні заняття
- •Модуль 6
- •Лабораторні заняття
- •Матеріали для самостійної роботи
- •VII. Розв’язування розрахункових задач з хімії класифікація хімічних задач
- •Загальні правила розв’язування задач
- •Взаємозв’язок фізичних величин у хімії
- •Навчання учнів розв’язуванню задач
- •Способи розв’язання задач
- •Синтетичний шлях
- •Відомі величини
- •Аналітичний шлях
- •Тема 2. Концепція і стандарт шкільної хімічної освіти у 12-річній школі
- •Матеріали для самостійної роботи
- •Ключові групи компетентностей
- •Концепція загальної середньої освіти (12-річна школа)
- •Концепція загальної середньої освіти (12-річна школа) Вступ
- •I. Мета, завдання і засади діяльності школи
- •II. Структура 12-річної школи
- •III. Зміст загальної середньої освіти
- •IV. Навчально-виховний процес
- •V. Середня загальноосвітня школа в системі безперервної освіти
- •VI. Управління загальноосвітньою школою
- •VII. Підготовка вчителя і його професійне вдосконалення
- •Державний стандарт базової і повної середньої освіти
- •Загальна частина
- •Базовий навчальний план
- •Характеристика освітніх галузей
- •5. Освітня галузь «Природознавство»
- •Основна школа
- •Старша школа
- •Загальноприроднича компонента освітньої галузі
- •Додаток 1
- •Типовий навчальний план загальноосвітніх навчальних закладів з українською мовою навчання (основна школа у структурі 12-річної)
- •Додаток 5
- •Таблиця розподілу годин на навчальні предмети за рівнями змісту
- •Додаток 6
- •Типовий навчальний план загальноосвітніх навчальних закладів з українською мовою навчання (старша школа (без профільна) у структурі 12-річної)
- •Додаток 7
- •Додаток 8
- •Додаток 9
- •Додаток 10
- •Додаток 11
- •Додаток 12
- •Додаток 13
- •Додаток 14
- •Додаток 18
- •Додаток 22
- •Типовий навчальний план вечірньої (змінної) загальноосвітньої школи
- •Додаток 23
- •Типовий навчальний план вечірньої (змінної) загальноосвітньої школи
- •Додаток 24
- •Типовий навчальний план-схема спеціалізованих шкіл, гімназій, ліцеїв, колегіумів, класів з поглибленим вивченням окремих предметів
- •Концепція хімічної освіти 12-річної школи
- •Програми, підручники та посібники, рекомендовані Міністерством освіти і науки України для загальноосвітніх навчальних закладів у 2006-2007 н.Р.
- •Тема 3. Структура і зміст шкільної хімічної освіти
- •Матеріали для самостійної роботи
- •Тема 4. Методи навчання хімії.
- •Матеріали для самостійної роботи
- •Робота в малих групах
- •Результати роботи в малих групах
- •Лабораторні заняття Заняття 1
- •Правила з техніки безпеки при роботах в хімічній лабораторії Загальні положення
- •Вимоги безпеки перед початком роботи
- •Вимоги безпеки після закінчення роботи
- •Вимоги безпеки в екстремальних ситуаціях
- •Заняття 2
- •Заняття 3
- •Модуль 2
- •Матеріали для самостійної роботи
- •Матеріали для самостійної роботи Засоби навчання
- •Засоби дистанційного навчання
- •Матеріали для самостійної роботи
- •Типи і структура уроків з хімії
- •Уроки засвоєння нових знань
- •Уроки-лекції
- •Уроки з використанням ігрових прийомів
- •Інтегровані (бінарні) уроки
- •Уроки узагальнення і систематизації знань
- •Уроки-семінари
- •Уроки-конференції
- •Урок «Мозкова атака»
- •Урок-аукціон
- •Біт-урок
- •Урок “круглий стіл”
- •Уроки контролю і корекції знань, умінь і навичок
- •Урок-гра
- •Урок-вікторина
- •Урок–конкурс
- •Урок–захист
- •Урок–квк (Клуб веселих та кмітливих)
- •Громадський огляд знань
- •Урок-залік
- •Урок удосконалення знань і вмінь
- •Урок перевірки знань і умінь
- •III. Вимоги до сучасного уроку
- •IV. Планування навчальної роботи та підготовка вчителя до уроку.
- •Лекційно-семінарська система навчання хімії
- •Сучасні освітні технології
- •Шкала переведення рейтингової оцінки в 5-бальну
- •Особливості методики:
- •Позакласна та позашкільна робота з хімії
- •Екскурсії
- •Позакласна робота з хімії
- •Хімічний вечір
- •Тиждень (декада, місячник) хімії
- •Хімічна олімпіада
- •Удосконалення класно-урочної системи
- •Нестандартні уроки
- •Матеріали для самостійної роботи
- •Хід уроку Ми продовжуємо вивчати властивості солей-електролітів. Давайте пригадаємо:
- •Компоненти солі повторення
- •Демонстрація
- •Демонстрація
- •Значення гідролізу.
- •Хід уроку:
- •1. Питання до класу:
- •II. Повторення матеріал
- •IV. Вивчення нового матеріалу:
- •V. Закріплення.
- •Урок-екскурсія
- •Хід уроку:
- •K Ca Se
- •У гостях у кислот
- •Хід уроку:
- •Лабораторні заняття Заняття 4
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 5
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Алгоритм
- •Модуль 3
- •Матеріали для самостійної роботи
- •Номенклатура неорганічних сполук
- •Хімічні сполуки
- •Катіони
- •Бінарні сполуки Оксигену (оксиди)
- •Основи, амфотерні гідроксиди
- •Кислоти
- •Солі та солеподібні сполуки
- •Координаційні сполуки
- •Органічні сполуки Алкани
- •Карбонові кислоти
- •Аміни і гетероциклічні сполуки
- •Лабораторні заняття Заняття 6
- •Семінарська частина
- •Практична частина
- •Аналіз уроку
- •Прийоми роботи учителя та учнів
- •Розподіл часу за етапами уроку і видами діяльності
- •Прийоми розвитку пізнавальних здібностей учнів
- •Характеристика особливостей даного уроку
- •Дотримання основних вимог до уроку і його результативність:
- •Самоаналіз уроку
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 7
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Визначте за хімічною формулою:
- •Заняття 8
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 4
- •Лабораторні заняття Заняття 9
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 10
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 11
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 5 Лекційний курс
- •Лабораторні заняття Заняття 12
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 13
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 6
- •Лабораторні заняття Заняття 14
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 15
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 16
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 7 (Проект) завдання №1
- •Завдання №2
- •Завдання №3
- •Завдання №4
- •Завдання №5
- •Завдання №6
- •Завдання №7
- •Завдання №8
- •Завдання №9
- •Завдання №10
- •Завдання №11
- •Завдання №12
- •Завдання №13
- •Завдання №14
- •Завдання №15
- •Завдання №16
- •Завдання №17
- •Завдання №18
- •Завдання №19
- •Завдання №20
- •Завдання №21
- •Завдання №22
- •Завдання №23
- •Завдання №24
- •Завдання №25
- •Завдання №26
- •Завдання №27
- •Завдання №28
- •Завдання №29
- •Завдання №30
- •Рекомендована література
Координаційні сполуки
При написанні формул комплексів символ центрального атома (комплексоутворювача) вказують першим, за ним спочатку йонні, а потім нейтральні ліганди в алфавітному порядку. Комплексну частину обмежують квадратними дужками. Назву комплексів починають з лігандів, які перелічують за алфавітом, потім вказують центральний атом.
[Fe(CN)6]3- – гексаціаноферат(ІІІ)
Катіонні та нейтральні комплекси не одержують у назвах спеціальних закінчень, назви аніонних мають суфікс –ат, що додається до кореня назви центрального атома. У разі необхідності вказують ступінь окиснення центрального атома або заряд його йона.
Назви катіонних та нейтральних лігандів не відрізняються від назв відповідних катіонів та молекул (за деяким винятком). Назви аніонних лігандів утворюють додаванням до назви аніонів закінчення –о.
SO42- - сульфато-
N3- - нітридо-
N3- - азидо-
Для деяких поширених аніонних лігандів поряд із систематичними можна використовувати традиційні назви:
|
Формула |
Аніон |
Ліганд |
|
F- |
флуорид |
флуоро- |
|
Cl- |
хлорид |
хлоро- |
|
Br- |
бромід |
бромо- |
|
J- |
йодид |
йодо- |
|
O2- |
оксид |
оксо- |
|
H- |
гідрид |
гідридо- |
|
OH- |
гідроксид |
гідроксо- |
|
O22- |
пероксид |
пероксо- |
|
S2- |
сульфід |
тіо- |
|
CN- |
ціанід |
ціано- |
Назва лігандів вважається одним цілим і перелічується в алфавітному порядку.
K3[Al(OH)6] – калій гексагідроксоалюмінат
K4[Fe(CN)6] – калій гексаціаноферат(ІІ)
Назви нейтральних лігандів використовуються без змін та беруться в дужки. Лише координовані вода, амоніак, нітроген(ІІ) оксид та карбон(ІІ) оксид мають свої специфічні традиційні назви: аква, амін, нітрозил, карбоніл, які входять до назви комплексу без дужок:
[Ag(NH3)2]Cl – диамінаргентум(І) хлорид
[CrOH(H2O)2(NH3)3]J2 – діакватриамінгідроксохром(ІІІ) іодид.
Для підкреслення способу координаціїї лігандів атоми (групи атомів), через які вона здійснюється, вказують після назви лігандів через дефіс за допомогою символів елементів:
K2[Hg(SCN)4] – калій тетра(тіоціанато-S)меркурат(ІІ)
K2[V(NCS)6] – калій гекса(тіоціанато-N)ванадат(IV)
Органічні сполуки Алкани
С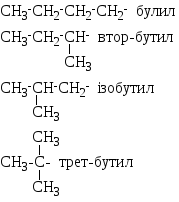 Н3-СН2-СН2-
пропіл
Н3-СН2-СН2-
пропіл
СН3-СН-СН3 – ізопропіл

Головний ланцюг – найдовший
Головний ланцюг – якнайбільше найпростіших відгалуджень
Нумерація – а) замісники отримують найменші локанти; б) порядок нумерації визначається алфавітним порядком замісників
Правила побудови назви
Головний ланцюг – назва алкану
Відгалуження – в алфавітному порядку з відповідним локантом і, якщо треба, множними префіксами (ди-, три-,...)
При визначенні алфавітного порядку множні префікси не враховуються
Локанти розділяють між собою комами, а від словесних частин назви відокремлюють дефісом
Алкени
Вибір головного ланцюга і його нумерація – наявністю подвійних зв’язків. Локант подвійного зв’язку позначають перед коренем назви.
СН2= або –СН2 – метилен
СН2=СН – етеніл (вініл)
СН2=СН – СН2 – 2-пропеніл (аліл)
СН3 – СН = СН – 1-пропеніл
Суфікс –ен замінюється на –еніл, при цьому атом вуглецю з вільною валентністю завжди одержує номер 1.
Алкіни
-ан на –ин (після л, м, н, п пишемо –ін, а після голосних –їн).
![]()
1,5-гексадієн-3-ін
радикал - -ініл
НСС – етиніл
![]()
1,3-гексадієн-5-ін 4-пентен-2-ініл
Ароматичні вуглеводні
С6Н6 – бензен
С6Н5 – феніл
С6Н4 – фенілен (орто-, мета-, пара-)
Т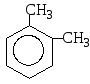 радиційні
назви зберігаються:
радиційні
назви зберігаються:
о-ксилен (м-, п-)

стирен
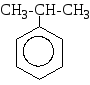
кумен
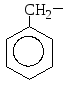
бензил
Галогенопохідні
Флуор-, хлор-, бром-, іод-
Нумерація – в алфавітному порядку

2-бром-3-метилбутан
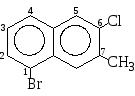
1-бром-7-метил-6-хлорнафтален
Спирти
-ол
-діол
-триол
При виборі головного ланцюга та його нумерації перевага надається гідроксигрупі.

2-метил-5-хлор-2,4-гександіол

5-метил-3,5-гептадієн-2-ол
Феноли

Фенол 2-метилфенол (о-крезол)
Альдегіди і кетони
Суфікс –аль до назви вуглеводню з найдовшим ланцюгом, включаючи альдегідну групу.
Для кетонів – нумерація з кінця, до якого ближче кетонна група і суфікс –он, а також локант, що вказує місце карбонільної групи. Карбонільна група вважається старшою за гідроксигрупу, тому при наявності у молекулі їх обох, гідроксигрупа вказується префіксом (гідрокси-), а альдегідна – суфіксом –аль, а кетогрупа суфіксом –он, чи префіксом –оксо-.
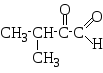
3-метил-2-оксобутаналь
![]()
2-гідрокси-6-хлор-4-гептанон
