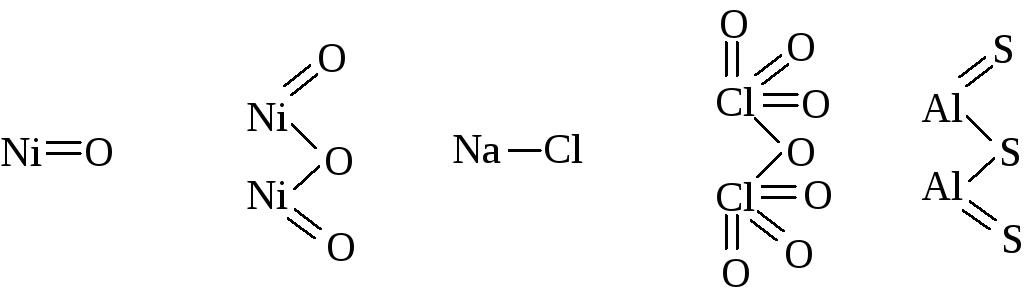- •Шкільний курс хімії та методика його викладання
- •Визначення номерів завдань самостійної роботи (інваріантна складова)
- •Зміст дисципліни
- •Модульна програма дисципліни модуль 1
- •Лабораторні заняття
- •Модуль 2
- •Лабораторні заняття
- •Модуль 3
- •Лабораторні заняття
- •Модуль 4
- •Лабораторні заняття
- •Модуль 5
- •Лабораторні заняття
- •Модуль 6
- •Лабораторні заняття
- •Матеріали для самостійної роботи
- •VII. Розв’язування розрахункових задач з хімії класифікація хімічних задач
- •Загальні правила розв’язування задач
- •Взаємозв’язок фізичних величин у хімії
- •Навчання учнів розв’язуванню задач
- •Способи розв’язання задач
- •Синтетичний шлях
- •Відомі величини
- •Аналітичний шлях
- •Тема 2. Концепція і стандарт шкільної хімічної освіти у 12-річній школі
- •Матеріали для самостійної роботи
- •Ключові групи компетентностей
- •Концепція загальної середньої освіти (12-річна школа)
- •Концепція загальної середньої освіти (12-річна школа) Вступ
- •I. Мета, завдання і засади діяльності школи
- •II. Структура 12-річної школи
- •III. Зміст загальної середньої освіти
- •IV. Навчально-виховний процес
- •V. Середня загальноосвітня школа в системі безперервної освіти
- •VI. Управління загальноосвітньою школою
- •VII. Підготовка вчителя і його професійне вдосконалення
- •Державний стандарт базової і повної середньої освіти
- •Загальна частина
- •Базовий навчальний план
- •Характеристика освітніх галузей
- •5. Освітня галузь «Природознавство»
- •Основна школа
- •Старша школа
- •Загальноприроднича компонента освітньої галузі
- •Додаток 1
- •Типовий навчальний план загальноосвітніх навчальних закладів з українською мовою навчання (основна школа у структурі 12-річної)
- •Додаток 5
- •Таблиця розподілу годин на навчальні предмети за рівнями змісту
- •Додаток 6
- •Типовий навчальний план загальноосвітніх навчальних закладів з українською мовою навчання (старша школа (без профільна) у структурі 12-річної)
- •Додаток 7
- •Додаток 8
- •Додаток 9
- •Додаток 10
- •Додаток 11
- •Додаток 12
- •Додаток 13
- •Додаток 14
- •Додаток 18
- •Додаток 22
- •Типовий навчальний план вечірньої (змінної) загальноосвітньої школи
- •Додаток 23
- •Типовий навчальний план вечірньої (змінної) загальноосвітньої школи
- •Додаток 24
- •Типовий навчальний план-схема спеціалізованих шкіл, гімназій, ліцеїв, колегіумів, класів з поглибленим вивченням окремих предметів
- •Концепція хімічної освіти 12-річної школи
- •Програми, підручники та посібники, рекомендовані Міністерством освіти і науки України для загальноосвітніх навчальних закладів у 2006-2007 н.Р.
- •Тема 3. Структура і зміст шкільної хімічної освіти
- •Матеріали для самостійної роботи
- •Тема 4. Методи навчання хімії.
- •Матеріали для самостійної роботи
- •Робота в малих групах
- •Результати роботи в малих групах
- •Лабораторні заняття Заняття 1
- •Правила з техніки безпеки при роботах в хімічній лабораторії Загальні положення
- •Вимоги безпеки перед початком роботи
- •Вимоги безпеки після закінчення роботи
- •Вимоги безпеки в екстремальних ситуаціях
- •Заняття 2
- •Заняття 3
- •Модуль 2
- •Матеріали для самостійної роботи
- •Матеріали для самостійної роботи Засоби навчання
- •Засоби дистанційного навчання
- •Матеріали для самостійної роботи
- •Типи і структура уроків з хімії
- •Уроки засвоєння нових знань
- •Уроки-лекції
- •Уроки з використанням ігрових прийомів
- •Інтегровані (бінарні) уроки
- •Уроки узагальнення і систематизації знань
- •Уроки-семінари
- •Уроки-конференції
- •Урок «Мозкова атака»
- •Урок-аукціон
- •Біт-урок
- •Урок “круглий стіл”
- •Уроки контролю і корекції знань, умінь і навичок
- •Урок-гра
- •Урок-вікторина
- •Урок–конкурс
- •Урок–захист
- •Урок–квк (Клуб веселих та кмітливих)
- •Громадський огляд знань
- •Урок-залік
- •Урок удосконалення знань і вмінь
- •Урок перевірки знань і умінь
- •III. Вимоги до сучасного уроку
- •IV. Планування навчальної роботи та підготовка вчителя до уроку.
- •Лекційно-семінарська система навчання хімії
- •Сучасні освітні технології
- •Шкала переведення рейтингової оцінки в 5-бальну
- •Особливості методики:
- •Позакласна та позашкільна робота з хімії
- •Екскурсії
- •Позакласна робота з хімії
- •Хімічний вечір
- •Тиждень (декада, місячник) хімії
- •Хімічна олімпіада
- •Удосконалення класно-урочної системи
- •Нестандартні уроки
- •Матеріали для самостійної роботи
- •Хід уроку Ми продовжуємо вивчати властивості солей-електролітів. Давайте пригадаємо:
- •Компоненти солі повторення
- •Демонстрація
- •Демонстрація
- •Значення гідролізу.
- •Хід уроку:
- •1. Питання до класу:
- •II. Повторення матеріал
- •IV. Вивчення нового матеріалу:
- •V. Закріплення.
- •Урок-екскурсія
- •Хід уроку:
- •K Ca Se
- •У гостях у кислот
- •Хід уроку:
- •Лабораторні заняття Заняття 4
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 5
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Алгоритм
- •Модуль 3
- •Матеріали для самостійної роботи
- •Номенклатура неорганічних сполук
- •Хімічні сполуки
- •Катіони
- •Бінарні сполуки Оксигену (оксиди)
- •Основи, амфотерні гідроксиди
- •Кислоти
- •Солі та солеподібні сполуки
- •Координаційні сполуки
- •Органічні сполуки Алкани
- •Карбонові кислоти
- •Аміни і гетероциклічні сполуки
- •Лабораторні заняття Заняття 6
- •Семінарська частина
- •Практична частина
- •Аналіз уроку
- •Прийоми роботи учителя та учнів
- •Розподіл часу за етапами уроку і видами діяльності
- •Прийоми розвитку пізнавальних здібностей учнів
- •Характеристика особливостей даного уроку
- •Дотримання основних вимог до уроку і його результативність:
- •Самоаналіз уроку
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 7
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Визначте за хімічною формулою:
- •Заняття 8
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 4
- •Лабораторні заняття Заняття 9
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 10
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 11
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 5 Лекційний курс
- •Лабораторні заняття Заняття 12
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 13
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 6
- •Лабораторні заняття Заняття 14
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 15
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 16
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 7 (Проект) завдання №1
- •Завдання №2
- •Завдання №3
- •Завдання №4
- •Завдання №5
- •Завдання №6
- •Завдання №7
- •Завдання №8
- •Завдання №9
- •Завдання №10
- •Завдання №11
- •Завдання №12
- •Завдання №13
- •Завдання №14
- •Завдання №15
- •Завдання №16
- •Завдання №17
- •Завдання №18
- •Завдання №19
- •Завдання №20
- •Завдання №21
- •Завдання №22
- •Завдання №23
- •Завдання №24
- •Завдання №25
- •Завдання №26
- •Завдання №27
- •Завдання №28
- •Завдання №29
- •Завдання №30
- •Рекомендована література
Хід уроку:
1. Питання до класу:
1 .Діти, яку тему ми розглянули з вами на попередньому уроці?
2.Що означає хімічна формула?
3.Що можна обчислити за хімічною формулою?
До дошки йдуть З учні (робота з картками)
№ 1.СuО а). Обчислити масові співвідношення
№ 2 SO2 б) Mr
№ 3 MgSO4 в) W елементів (у %).
За столом робота з картками (4 учні).
II. Повторення матеріал
Що ж вивчає хімія?
Що таке тіла? Приклади.
Що таке речовина?
Що називається фізичним явищем? Приклади.
Що називається хімічним явищем? Приклади.
Як ми називаємо хімічне явище?
З чого складаються речовини?
А з чого складаються молекули?
Що ми називаємо молекулою?
Що ми називаємо атомом?
ІІІ. Перевіряємо відповіді учнів, що працювали біля дошки та на картках.
Якщо відповідь неповна, учні задають додатково запитання, потім оцінюють відповіді.
IV. Вивчення нового матеріалу:
Валентність атомів елементів
До цього часу ви користувалися готовими формулами.
А як же складаються хімічні формули? Хімічну формулу виводять на основі даних про якісний і кількісний склад речовин. Встановлено, що в будь-якій порції води на 1 м.ч. Н припадає 8 м.ч. О. Через те, що найменшою кількістю атомів О в молекулі води може бути 1 атом, тобто 16 м.ч. (Аг(О) = 16), Н в ній міститься 2 атоми (Аг(Н) = 1). Отже, на 2 атоми Н припадає 1 атом О.
|
Н О 1:8 2:16 Н2О |
Такий спосіб використовують тоді, коли формулу даної речовини виводять вперше.
|
Речовин дуже багато і заучувати їх формули важко, і вивчати хімію було б важко. Виявляється, що можна судити про склад речовини і написати її формулу, знаючи закономірності сполучення атомів. Для цього треба ознайомитися з новою властивістю атомів – валентністю.
Розглянемо склад кількох речовин:
НСl Н2O NН3 СН4
Що ж таке валентність? Властивість атомів одного хімічною елемента сполучатися з певною кількістю атомів іншого елемента.
За одиницю валентності прийнято валентність атома Н. Атом Н не може приєднати більше одного атома іншого елемента.
![]()
У молекулі будь-якої сполуки загальна сума одиниць валентностей атомів одного елемента дорівнює загальній сумі одиниць валентностей атомів іншого елемента.
Чому дорівнює валентність атома іншого елемента, якщо валентність Н – І?
НВr SiН4 РН3 Н2S
Демонстрація моделей.
Запишемо графічні формули:
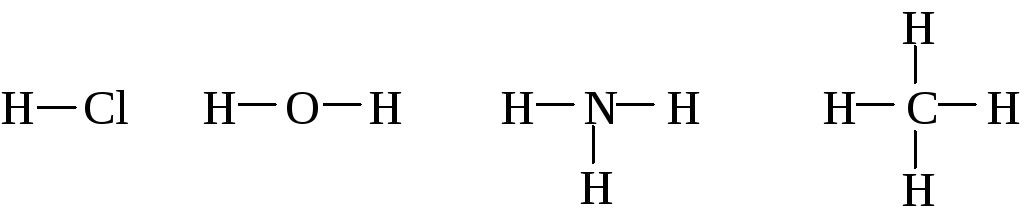
прості речовини Н2, О2
графічні формули Н–Н, O=O
Рисочка означає зв’язки між атомами – звідси видно, які атоми сполучені один з одним, а які ні.
Розглянемо ряд бінарних сполук елементів з киснем.
![]()

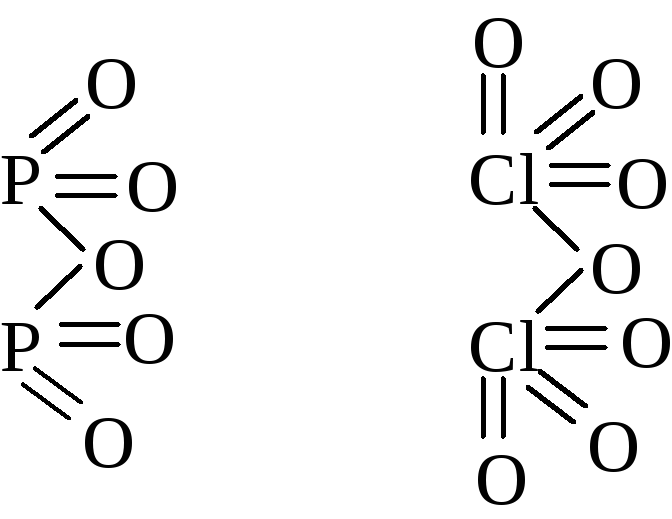
а) Визначити валентність атомів іншого елемента, знаючи, що валентність Оксигену – ІІ.
б) У яких випадках індекс одного елемента в бінарній сполуці є валентністю іншого елемента?
в) У яких випадках обов’язково знаходити найменше спільне кратне при виведенні хімічної формули?
Елементи із сталою валентністю
І – Nа, К, Аg, Н, F.
II – О, Мg, Са, Zn, Сd, Ва, Sг.
III – А1, В.
V – Ві.
Елементи із змішаною валентністю
|
Cu – 1 i 2 Hg – 1 i 2 |
Fe – 2 i 3 Ni – 2 i 3 Co – 2 i 3 Cr – 2 i 3 |
C – 2 i 4 Si – 2 i 4 Sn – 2 i 4 Pb – 2 i 4 Pt – 2 i 4 |
Au – 1 i 3 P – 3 (H, Me), 3, 5 (O) As – 3 (H), 3, 5 (O) N – 3 (H, Me), 1,2,3,4 (O) S – 2 (H, Me), 4, 6 (O) Mn – 2, 3, 4, 6, 7 (O), 2, 4 з ін. Cl, Br, I – 1 (H, Me), 7 (O) |
Назва речовин:
![]()
![]()
![]()
![]()
Складання формул за валентністю
Знаючи валентність, можна виводити формули бінарних сполук:
![]()
Учні самостійно записують в зошит формули з послідуючою перевіркою через графопроектор:
![]()