
- •Шкільний курс хімії та методика його викладання
- •Визначення номерів завдань самостійної роботи (інваріантна складова)
- •Зміст дисципліни
- •Модульна програма дисципліни модуль 1
- •Лабораторні заняття
- •Модуль 2
- •Лабораторні заняття
- •Модуль 3
- •Лабораторні заняття
- •Модуль 4
- •Лабораторні заняття
- •Модуль 5
- •Лабораторні заняття
- •Модуль 6
- •Лабораторні заняття
- •Матеріали для самостійної роботи
- •VII. Розв’язування розрахункових задач з хімії класифікація хімічних задач
- •Загальні правила розв’язування задач
- •Взаємозв’язок фізичних величин у хімії
- •Навчання учнів розв’язуванню задач
- •Способи розв’язання задач
- •Синтетичний шлях
- •Відомі величини
- •Аналітичний шлях
- •Тема 2. Концепція і стандарт шкільної хімічної освіти у 12-річній школі
- •Матеріали для самостійної роботи
- •Ключові групи компетентностей
- •Концепція загальної середньої освіти (12-річна школа)
- •Концепція загальної середньої освіти (12-річна школа) Вступ
- •I. Мета, завдання і засади діяльності школи
- •II. Структура 12-річної школи
- •III. Зміст загальної середньої освіти
- •IV. Навчально-виховний процес
- •V. Середня загальноосвітня школа в системі безперервної освіти
- •VI. Управління загальноосвітньою школою
- •VII. Підготовка вчителя і його професійне вдосконалення
- •Державний стандарт базової і повної середньої освіти
- •Загальна частина
- •Базовий навчальний план
- •Характеристика освітніх галузей
- •5. Освітня галузь «Природознавство»
- •Основна школа
- •Старша школа
- •Загальноприроднича компонента освітньої галузі
- •Додаток 1
- •Типовий навчальний план загальноосвітніх навчальних закладів з українською мовою навчання (основна школа у структурі 12-річної)
- •Додаток 5
- •Таблиця розподілу годин на навчальні предмети за рівнями змісту
- •Додаток 6
- •Типовий навчальний план загальноосвітніх навчальних закладів з українською мовою навчання (старша школа (без профільна) у структурі 12-річної)
- •Додаток 7
- •Додаток 8
- •Додаток 9
- •Додаток 10
- •Додаток 11
- •Додаток 12
- •Додаток 13
- •Додаток 14
- •Додаток 18
- •Додаток 22
- •Типовий навчальний план вечірньої (змінної) загальноосвітньої школи
- •Додаток 23
- •Типовий навчальний план вечірньої (змінної) загальноосвітньої школи
- •Додаток 24
- •Типовий навчальний план-схема спеціалізованих шкіл, гімназій, ліцеїв, колегіумів, класів з поглибленим вивченням окремих предметів
- •Концепція хімічної освіти 12-річної школи
- •Програми, підручники та посібники, рекомендовані Міністерством освіти і науки України для загальноосвітніх навчальних закладів у 2006-2007 н.Р.
- •Тема 3. Структура і зміст шкільної хімічної освіти
- •Матеріали для самостійної роботи
- •Тема 4. Методи навчання хімії.
- •Матеріали для самостійної роботи
- •Робота в малих групах
- •Результати роботи в малих групах
- •Лабораторні заняття Заняття 1
- •Правила з техніки безпеки при роботах в хімічній лабораторії Загальні положення
- •Вимоги безпеки перед початком роботи
- •Вимоги безпеки після закінчення роботи
- •Вимоги безпеки в екстремальних ситуаціях
- •Заняття 2
- •Заняття 3
- •Модуль 2
- •Матеріали для самостійної роботи
- •Матеріали для самостійної роботи Засоби навчання
- •Засоби дистанційного навчання
- •Матеріали для самостійної роботи
- •Типи і структура уроків з хімії
- •Уроки засвоєння нових знань
- •Уроки-лекції
- •Уроки з використанням ігрових прийомів
- •Інтегровані (бінарні) уроки
- •Уроки узагальнення і систематизації знань
- •Уроки-семінари
- •Уроки-конференції
- •Урок «Мозкова атака»
- •Урок-аукціон
- •Біт-урок
- •Урок “круглий стіл”
- •Уроки контролю і корекції знань, умінь і навичок
- •Урок-гра
- •Урок-вікторина
- •Урок–конкурс
- •Урок–захист
- •Урок–квк (Клуб веселих та кмітливих)
- •Громадський огляд знань
- •Урок-залік
- •Урок удосконалення знань і вмінь
- •Урок перевірки знань і умінь
- •III. Вимоги до сучасного уроку
- •IV. Планування навчальної роботи та підготовка вчителя до уроку.
- •Лекційно-семінарська система навчання хімії
- •Сучасні освітні технології
- •Шкала переведення рейтингової оцінки в 5-бальну
- •Особливості методики:
- •Позакласна та позашкільна робота з хімії
- •Екскурсії
- •Позакласна робота з хімії
- •Хімічний вечір
- •Тиждень (декада, місячник) хімії
- •Хімічна олімпіада
- •Удосконалення класно-урочної системи
- •Нестандартні уроки
- •Матеріали для самостійної роботи
- •Хід уроку Ми продовжуємо вивчати властивості солей-електролітів. Давайте пригадаємо:
- •Компоненти солі повторення
- •Демонстрація
- •Демонстрація
- •Значення гідролізу.
- •Хід уроку:
- •1. Питання до класу:
- •II. Повторення матеріал
- •IV. Вивчення нового матеріалу:
- •V. Закріплення.
- •Урок-екскурсія
- •Хід уроку:
- •K Ca Se
- •У гостях у кислот
- •Хід уроку:
- •Лабораторні заняття Заняття 4
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 5
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Алгоритм
- •Модуль 3
- •Матеріали для самостійної роботи
- •Номенклатура неорганічних сполук
- •Хімічні сполуки
- •Катіони
- •Бінарні сполуки Оксигену (оксиди)
- •Основи, амфотерні гідроксиди
- •Кислоти
- •Солі та солеподібні сполуки
- •Координаційні сполуки
- •Органічні сполуки Алкани
- •Карбонові кислоти
- •Аміни і гетероциклічні сполуки
- •Лабораторні заняття Заняття 6
- •Семінарська частина
- •Практична частина
- •Аналіз уроку
- •Прийоми роботи учителя та учнів
- •Розподіл часу за етапами уроку і видами діяльності
- •Прийоми розвитку пізнавальних здібностей учнів
- •Характеристика особливостей даного уроку
- •Дотримання основних вимог до уроку і його результативність:
- •Самоаналіз уроку
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 7
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Визначте за хімічною формулою:
- •Заняття 8
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 4
- •Лабораторні заняття Заняття 9
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 10
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 11
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 5 Лекційний курс
- •Лабораторні заняття Заняття 12
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 13
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 6
- •Лабораторні заняття Заняття 14
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 15
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Заняття 16
- •Семінарська частина
- •Практична частина
- •Лабораторна частина
- •Завдання для самостійної роботи
- •Модуль 7 (Проект) завдання №1
- •Завдання №2
- •Завдання №3
- •Завдання №4
- •Завдання №5
- •Завдання №6
- •Завдання №7
- •Завдання №8
- •Завдання №9
- •Завдання №10
- •Завдання №11
- •Завдання №12
- •Завдання №13
- •Завдання №14
- •Завдання №15
- •Завдання №16
- •Завдання №17
- •Завдання №18
- •Завдання №19
- •Завдання №20
- •Завдання №21
- •Завдання №22
- •Завдання №23
- •Завдання №24
- •Завдання №25
- •Завдання №26
- •Завдання №27
- •Завдання №28
- •Завдання №29
- •Завдання №30
- •Рекомендована література
V. Закріплення.
Питання до класу:
Що таке валентність?
Проведення гри: Хто швидше виведе формулу, запише графічну формулу та, користуючись набором моделей атомів, складе структурну формулу?
Бінарні сполуки.
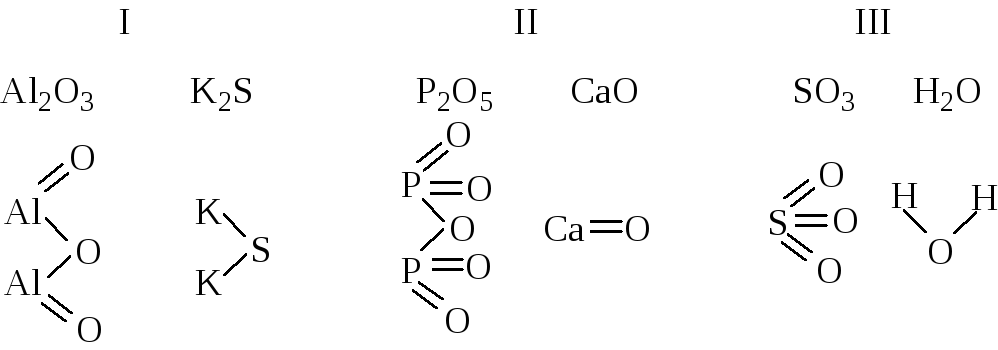
Домашнє завдання: § 11, 12.
Тема: “Хімічні властивостей солей у світлі уявлень про електролітичну дисоціацію і вчення про окислювально-відновні реакції”
Навчальна мета: Узагальнити знання учнів про хімічні властивості солей, їх класифікацію, застосування.
Виховна мета: Виховувати в учнів вміння коректно вести діалог, відстоювати свої позиції.
Розвиваюча мета: Розвивати вміння використовувати академічні знання для вирішення практичних проблем.
Тип уроку: Урок узагальнення набутих знань, умінь і навичок учнів.
Метод проведення: Семінарське заняття у вигляді гри “Поле чудес”.
Унаочнення: Залізний цвях, опущений в розчин CuSO4, NаНСО3, NаОН, НСl, ВaСІ2, Н2SО4.
ХІД УРОКУ:
І. Узагальнення знань, умінь і навичок учнів:
1. Сьогодні ми систематизуємо відомі вам знання про хімічні властивості солей, їх класифікацію. Проводимо урок у вигляді гри “Поле чудес”. Для активної участі в цьому уроці необхідна розминка. Слухайте уважно текст. Вам необхідно буде встановити, які помилки допустив Незнайка:
- Ура! – закричав Незнайка, – знайшов. - Дивіться беру фенолфталеїн і добавляю його до розчину солі Na2SO4, розчин набув малинового кольору, а тепер додам до цього розчину концентрований розчин НСl, потім трохи чистого цинкового пилу, проходить хімічна реакція. Дивіться як активно виділяється газ, він ... горить. Та це ж вуглекислий газ. Тепер цей газ пропущу через оксид міді. Ой, дивіться виділяється чиста мідь і рідина. Та це ж кислота! Як цікаво. Допоможіть мені. Знайка хімії заставляє мене написати рівняння реакції і каже, що я наробив безліч помилок. Допоможіть мені. Доведіть, що це не так. (Помилки виділені іншим шрифтом).
2. Вам дається три хвилини, щоб виправити помилки які зробив Незнайка. Запишіть вірно всі рівняння реакцій, де можливо в 3 формах, які неорганічні речовини тут використовуються?
Nа2SO4 – фенолфталеїн не змінює забарвлення;
Nа2SO4 + 2НСl = 2NаСl + Н2SО4;
Н2SО4 + Zп =ZпSO4 + H2;
H2 + CuO = H2O + Cu
3. Учитель перевіряє роботу учнів, які першими виконали і виставляє оцінки, а тепер ці 5-6 учнів перевіряють в інших і теж виставляють оцінки.
Учитель: Розминку закінчили, а тепер переходимо до гри “Поле чудес”. Починаємо І тур. На дошці закодоване слово речовина яка використовується на нашій водоочисній станції для очистки води. Дати визначення цій речовині (солі), з точки зору ТЕЛД і пояснити завдяки якій властивості вона там використовується. Написати рівняння в 3 формах (учні працюють на місцях).
Залізний купорос FеSO4·7Н2O
Учень: FеSO4 + 2NаОН = Nа2SO4 + Fе(ОН)2.
Учитель: Відповідь учнем дана правильна, переможцю вручаємо набори солодких напоїв з нашої води і пляшку мінеральної води “Семенівська”.
Учитель: Починаємо наступний тур. Перед вами лежить брусочок мила. На дошці закодована назва речовини без якої неможливо виготовити мило. Назвати цю речовину і написати рівняння реакцій всіх можливих способів одержання її.
Учень: Сода.
Nа2O+СO2 = Nа2СО3;
2NаОН + СО2 = Nа2СО3 + Н2О;
2NаОН + Н2СО3 = Nа2СО3 + Н2О;
2Nа + Н2СО3 = Nа2СО3 + Н2O;
Nа2О + Н2СОз = Nа2СО3 + Н2О.
Учитель: Ми можемо визначити другого переможця нашої незвичайної гри і вручаємо йому сувенірний набір мил.
Учитель: Починаємо третій тур. На дошці закодована назва речовини, яка найчастіше використовується в житті людини. Назвати цю сіль і визначити в ній аніон.
Учень: NаС1 – фізіологічний розчин 0,85%.
NаСl +АgNО3 = АgСl↓ + NаNO3,
Кухонна сіль.
Учитель: Яка властивість солей цим рівнянням з’ясована?
Учень: Взаємодія двох солей з утворенням нерозчинної солі.
Учитель: А тепер я запрошую розіграти суперприз. Подивіться, який красивий торт. Ви станете його володарем, якщо назвете сполуку, яка необхідна при випіканні його і напишете рівняння, що тут відбувається.
Учень: Питна сода.
NаHСО3 + CH3COOH → СН3СООNа + Н2О + СО2
Учитель: Яка властивість солей тут засовується?
Учень: Взаємодія з кислотами.
Учитель: Відповідь дана точно і правильно. Ви виграєте наш суперфінал. Приз Ваш.
- Давайте підведемо підсумок уроку. Ви ознайомилися із властивостями солей.
- Які властивості мають солі і як вони класифікуються?
Учениця: Перелічує властивості і дає класифікацію солям:
1. Середні;
2. Кислі;
3. Основні.
Учитель: Оцінки за урок.
Домашня контрольна робота:
“А” – Розрахуйте, скільки г-йонів Nа і хлору утвориться в результаті дисоціації розчину NаСl (m = 150 г) з масовою часткою солі 20%.
“В” – Яку формулу матиме речовина, що містить 65,3 % – О, 32,6% -S, 2,1% – H. Густина парів цієї сполуки за воднем – 49.
“С” – Скільки грамів H2SО4 з масовою часткою 10% потрібно для реакції з 46 г Na.
Нестандартні уроки хімії включають проведення уроків-екскурсій, подорожей, з ігровими моментами. Якщо раніше уроки дидактичних ігор вважалися несерйозними, то, зараз на ці уроки звертається досить значна увага. В ігровій ситуації діти не помічають як починають виконувати роль дорослої людини з тією чи іншою професією.
