
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
Антибиотики
50
Гликопептидные, полиэфирные и нуклеозидные антибиотики
ВВЕДЕНИЕ. Здесь мы рассмотрим следующие антибиотики: гликопептидный антибиотик ванкомицин, который активен против штаммов Staphylococсus aureus, устойчивых к действию метициллина; его аналог авопарцин, применяемый в качестве кормовой добавки; гликозид линкомицин, очень эффективно действующий против грамположительных энтеробактерий; а также монензин, который используют на птицефабриках для профилактики инфекций, вызываемых простейшими. Несмотря на то что нуклеозидные антибиотики – природные соединения, в медицине используются только продукты химического синтеза. В качестве примера нуклеозидного антибиотика здесь рассмотрен ацикловир – аналог гуанозина, применяемый для лечения вирусного менингита.
ВАНКОМИЦИН И АВОПАРЦИН. Ванкомицин, продуцентом которого является Amycolatopsis orientalis, применяется в борьбе с энтерококковыми бактериями, устойчивыми к действию пенициллина, например при септическом эндокардите. Этот антибиотик часто используется для лечения пациентов, страдающих аллергией на β-лактамные антибиотики. Ванкомицин оказывает негативное действие на почки, поэтому при лечении этим антибиотиком необходимо следить за функцией почек. Как и в случае β-ла- ктамных антибиотиков, действие ванкомицина на микроорганизмы заключается в ингибировании образования клеточной стенки бактерий в результате связывания антибиотика с UDP-мурамилпентапептидом. В штаммах, устойчивых к действию ванкомицина, реализуется путь синтеза клеточной стенки с другими промежуточными продуктами, не вступающими в реакцию с этим антибиотиком. Устойчивость к антибиотику, возможно, возникает в результате горизонтального переноса генетической информации посредством транспозонов между людьми, а также домашними животными. Авопарцин – продукт жизнедеятельности Streptomyces candidus, по структуре очень близкий к ванкомицину – в странах ЕС применяется в качестве кормовой добавки. Эксперименты на изолированных транспозонах, обеспечивающих устойчивость к ванкомицину и авопарцину, показали, что, возможно, в организме человека штаммы энтеробактерий, устойчивые к действию этих антибиотиков, возникают по такому же механизму передачи генетической информации. По этой причине в некоторых странах (например, в Дании) авопарцин был запрещен; согласно клиническим наблюдениям, случаи резистентности к ванкомицину стали реже.
ЛИНКОМИЦИН – антибиотик, образующийся в Streptomyces lincolnensis и действующий против грамположительных бактерий. Основное применение линкомицина связано с ветеринарией. Механизм действия
этого антибиотика сходен с действием хлорамфеникола: линкомицин связывается с 50S-субъединицей прокариотической рибосомы и препятствует дальнейшему росту пептидной цепи. К настоящему времени зарегистрировано множество штаммов, обладающих устойчивостью к линкомицину. В таких клетках линкомицин либо подвергается ферментативному разрушению, либо в результате метилирования происходят такие изменения рРНК, что линкомицин не взаимодействует с 50S-субъединицей прокариотической рибосомы.
МОНЕНЗИН – полиэфирный антибиотик, который получают в процессе ферментации, осуществляемой
Streptomyces cinnamonensis. Путь биосинтеза монензина аналогичен синтезу поликетидных антибиотиков из ацетата, пропионата и бутирата. Молекулы монензина встраиваются в мембрану и функционируют как ионофоры: они обеспечивают поступление ионов Na+
вклетку и таким образом вызывают осмотический лизис клетки. Такой механизм объясняет чрезвычайно широкий круг организмов, для которых действие монензина является токсичным: к ним относятся не только бактерии и грибы, но и простейшие, например
Eimeria sp. и Toxoplasma sp., вызывающие заболевания на птицефермах. Из-за высокой токсичности монензин не используется в медицине, однако находит широкое применение в качестве кормовой добавки при разведении кур и крупного рогатого скота. На долю монензина и его структурного аналога салиномицина приходится до 80% объема мирового рынка антибиотиков. Производство монензина превышает 3000 т/год, а рыночный оборот составляет 200 млн долл. США.
НУКЛЕОЗИДНЫЕ АНТИБИОТИКИ. Нуклеозидные антибиотики пока находят лишь ограниченное применение. Аналог цитозина, бластицидин S, образующийся
вStreptomyces griseochromogenes, используют при выращивании риса в качестве фунгицида, препятствующего возникновению мучнистой росы. Действие бластицидина S основано на ингибировании связывания аминоацил-тРНК с рибосомой. В лечении заболеваний, вызванных вирусами герпеса, таких как энцефалит, важная роль принадлежит ацикловиру – синтетическому аналогу гуанозина.
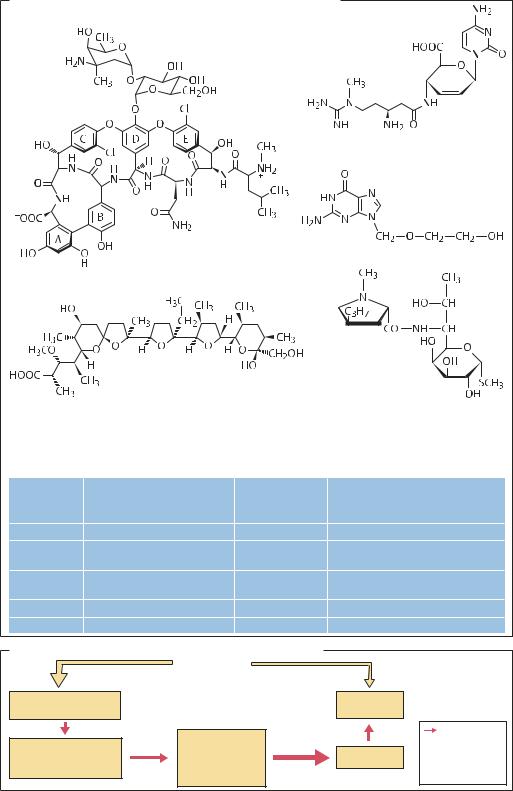
Гликопептидные, гликозидные и нуклеозидные антибиотики
a Ванкомицин |
б Бластицидин S |
в Ацикловир
д Линкомицин
г Монензин А
|
a |
б |
в |
г |
д |
|
С66Н75Сl2N9O24 |
С17Н26N8O5 |
С8Н11N5O3 |
С36Н62O11 |
С18Н34N2O6S |
MR |
1449,27 |
422,44 |
225,21 |
670,90 |
406,56 |
Код CAS |
1404-90-6 |
2079-00-7 |
59277-89-3 |
17090-79-8 |
154-21-2 |
|
|
|
|
|
|
Антибиотик |
Микроорганизмы, исполь- |
Объем мирового |
Применение |
|
зуемые при ферментации |
рынка |
|
|
|
|
|
Ванкомицин |
Amycolatopsis orientalis |
|
Медицина |
Авопарцин |
Streptomyces candidus |
|
Кормовая добавка |
Монензин |
S. cinnamonensis |
Более 3000 т в год, |
Профилактика протозойных |
|
|
200 млн долл. США |
инфекций у кур |
Бластицидин S |
S. griseochromogenes |
|
Защита растений от грибковых |
|
|
|
инфекций (фунгицид) |
Ацикловир |
Химический синтез |
|
Медицина: противовирусный препарат |
Линкомицин |
S. lincolnensis |
|
Ветеринария |
Проблема устойчивости (резистентности) к антибиотикам |
|
|
||
|
Антибиотики |
|
|
|
Корм сельскохозяйст- |
|
Клиническая |
|
|
венных животных |
|
медицина |
|
|
|
|
|
Рост числа |
|
Сельскохозяйственные |
Техническая, |
|
резистентных |
|
питьевая и водо- |
Инфекции |
штаммов |
||
и домашние животные, |
||||
проводная вода, |
микро- |
|||
отходы/сточные воды |
|
|||
орошение |
|
организмов |
||
|
|
|||
|
|
|
51 |
|
Антибиотики
52
Аминогликозидные антибиотики
ВВЕДЕНИЕ. Открытие стрептомицина, сделанное Зельманом Ваксманом в 1943 г., явилось важной вехой в изучении антибиотиков. Этот препарат был впервые успешно применен для лечения туберкулеза, вызываемого Mycobacterium tuberculosum, – одного из широко распространенных и наиболее опасных заболеваний человека. Стрептомицин, как и большинство аминогликозидных антибиотиков, оказывает различные побочные эффекты, связанные с нарушениями слуха и работы почек, поэтому в настоящее время для лечения туберкулеза используют другие антибиотики (гидразид изоникотиновой кислоты, рифампицин, а ранее часто применяли циклосерин). Молекулы аминогликозидных антибиотиков состоят из кольца аминоциклитола (например, 2-дезоксистрептамин), которое связано с другими остатками аминосахаров гликозидными связями. Аминогликозидные антибиотики, как правило, имеют широкий спектр действия, в том числе они эффективны против грамотрицательных бактерий, поэтому несмотря на относительно высокую токсичность их широко используют в медицине, например при тяжелых инфекциях. Другой областью применения аминогликозидных антибиотиков является сельское хозяйство, где они служат для защиты растений. Объем рынка аминогликозидных антибиотиков достигает 800 млн долл. США в год. В медицинских целях наиболее важное значение имеют следующие антибиотики группы аминогликозидов: гентамицин, неомицин, тобрамицин, позднее гентамицин, канамицин, полусинтетические продукты сизомицин и амикацин, а в специальных случаях – стрептомицин. Спектиномицин используют при лечении заболеваний, вызванных штаммами Neisseria gonorrhoeае, устойчивыми к пенициллину. Касугамицин применяют при выращивании риса для профилактики мучнистой росы, а гидромицин используют в ветеринарии.
БИОСИНТЕЗ. Большинство аминогликозидных антибиотиков образуются в прокариотических организмах – представителях Streptomyces и Micromonospora. Биосинтез аминогликозидных антибиотиков включает множество стадий (например, в случае стрептомицина их насчитывается 24), при этом D-глюкоза связывается с нуклеозидом, затем образуется аминоциклитольное кольцо, к которому через гликозидные связи присоединяются специфические сахара (С-разветвленные сахара, аминосахара). В синтезе стрептомицина принимают участие 33 белка, гены которых образуют крупный генный кластер размером 30–40 т.п.н. на хромосоме S. griseus. Многие из этих генов клонированы.
ПОЛУЧЕНИЕ. Для получения более высоких выходов аминогликозидных антибиотиков постоянно ведется работа по созданию новых штаммов. Так, в результа-
те многократного повторения раундов мутагенеза с последующим отбором мутантов удается повысить выход продукта, например стрептомицина: в диком штамме синтезируется нескольких миллиграммов на литр, а в штаммах-суперпродуцентах выход антибиотика превышает 10 г/л после 120 ч роста. В промышленности для выращивания культуры используют биореакторы с большим рабочим объемом. В качестве источника углерода служат глюкоза, крахмал или декстрин, а источником азота – соевая мука. Аминогликозидные антибиотики, в частности гентамицин, выделяются в среду роста, после того как рН среды доводен до 2,0. После отделения клеточной массы следует концентрирование культуральной жидкости, из которой в дальнейшем методом ионообменной хроматографии получают очищенный антибиотик.
МЕХАНИЗМ ДЕЙСТВИЯ И УСТОЙЧИВОСТЬ К АНТИБИОТИКАМ. Антимикробный эффект аминогликозидных антибиотиков объясняется тем, что их молекулы связываются с 30S-субъединицей прокариотической рибосомы и вызывают ошибки трансляции, приводящие к остановке синтеза полипептидных цепей. Некоторые антибиотики группы аминогликозидов специфически взаимодействуют с РНК интронов I группы. Недостаток аминогликозидных антибиотиков заключается в том, что микроорганизмы достаточно быстро вырабатывают механизм устойчивости к их действию. В результате ферментативного ацетилирования, фосфорилирования или аденилирования гидроксильных групп в структуре рибосомы, ее связывание с молекулами антибиотика нарушается. Ферменты, осуществляющие такие специфические модификации, закодированы в плазмиде или хромосоме микроорганизма.
ПОЛУСИНТЕТИЧЕСКИЕ АМИНОГЛИКОЗИДНЫЕ АНТИБИОТИКИ. Путем химических превращений аминокислот получают, как правило, полусинтетические аминогликозидные антибиотики (сизомицин, амикацин, тобрамицин). Несмотря на то что многие гены ферментов, участвующих в биосинтезе аминогликозидных антибиотиков, клонированы, в настоящее время синтез с использованием этих ферментов в промышленных масштабах экономически невыгоден. Это объясняется прежде всего чрезвычайно сложными механизмами регуляции активности ферментов биосинтеза.
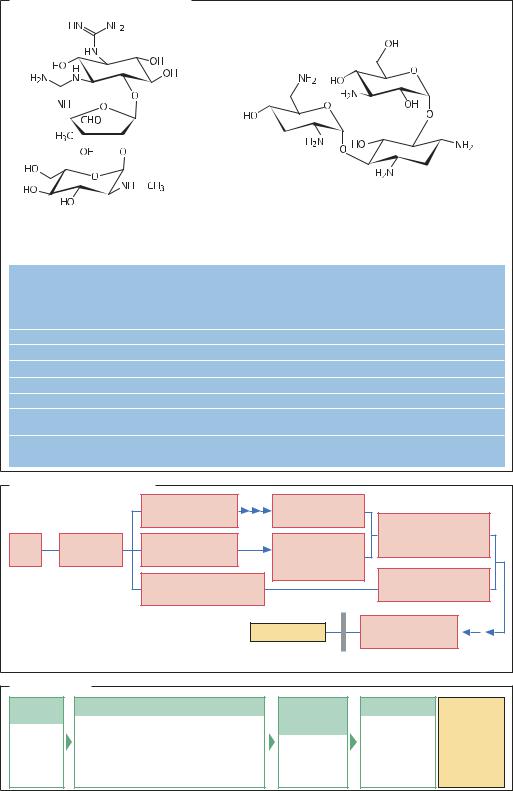
Аминогликозидные антибиотики
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Стрептомицин |
MR |
581,58 |
|
|
Тобрамицин |
MR |
467,51 |
|
||||||
|
С21Н39N7O12 |
КодCAS 57-92-1 |
|
С18Н37N5O9 |
Код CAS |
32986-56-4 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Антибиотик |
Продуцент |
|
|
Объем рынка |
Применение |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
в 2004 г. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(млн долл. США) |
|
|
|
|
Стрептомицин |
Streptomyces griseus |
|
|
Антибиотик широкого спектра действия, |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
в том числе против Mycobacterium tuberculosum |
||
Тобрамицин |
S. tenebrarius |
|
|
220 |
Антибиотик широкого спектра действия |
||||||||||
Гентамицин |
Micromonospora purpurea |
|
|
Антибиотик широкого спектра действия |
|||||||||||
Амикацин* |
S. kanamyceticus |
50 |
Антибиотик широкого спектра действия |
||||||||||||
Нетилмицин* |
M. purpurea |
|
|
|
|
Антибиотик широкого спектра действия |
|||||||||
Неомицин |
S. fradiae |
|
|
|
|
Кожные инфекции |
|||||||||
Касугамицин |
S. kasugaensis |
|
|
|
|
Используется при выращивании риса, |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
действует против мучнистой росы |
||
Валидамицин |
S. hygroscopicus |
|
|
|
|
Используется при выращивании риса |
|||||||||
* Химическое производное |
|
|
|
|||
Биосинтез стрептомицина |
|
|
|
|||
|
|
мио-Инозит- |
Стрептидин- |
|
|
|
|
|
1-фосфат |
6-фосфат |
4-О-α-L-Дигидро- |
||
|
|
|
|
|||
|
|
|
|
стрептозил-1D-стреп- |
||
Глю- |
Глюкозо- |
4-Оксо-6-дезокси- |
Тимидинфосфат- |
тидин-6-фосфат |
||
коза |
6-фосфат |
D-глюкозо-dTDP |
L-дигидро- |
|
|
|
|
|
|
стрептоза |
|
|
|
|
|
UDP-N-Метил-D-глюкоз- |
|
NDP-N-Метил- |
||
|
|
|
L-глюкозамин |
|
||
|
|
амин-6-фосфат |
|
|
||
|
|
|
|
|
||
Весь процесс синтеза стрептомицина протекает |
Стрептомицин |
Дигидрострепто- |
|
|||
с участием 33 ферментов. Их гены образуют генный |
мицин-6-фосфат |
|
||||
кластер размером 30–40 т.п.н. Большинство |
|
|
|
|||
этих генов в настоящее время клонировано. |
Цитоплазматическая мембрана |
|
||||
|
|
|
|
|||
Производство |
|
|
|
|
||
Предфер- |
|
Основная ферментация |
Отделение |
Очистка |
|
|
ментация |
Непрерывный процесс в реакторе |
клеточной |
Ионообменная |
Выход |
||
|
массы |
|||||
Инокуля- |
объемом до 150 м3, 28–30 °С в течение |
хроматография, |
продукта – |
|||
|
||||||
ция |
70–120 ч, глюкоза и декстрины, соевая |
Закисление |
перекристал- |
более 10 г/л |
||
|
мука, 1–3 г/л NaCl, микроэлементы, |
среды |
лизация |
после 120 ч |
||
|
подача кислорода с интенсивностью |
до рН 2 |
|
ферментации |
||
|
0,5–1 объем реактора в минуту |
|
|
53 |
||
|
|
|
|
|
||
