
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
Ферменты
Ферменты, расщепляющие крахмал
ВВЕДЕНИЕ. Крахмал является вторым по значимости |
α-АМИЛАЗА обнаружена во многих организмах. |
||||
полисахаридом после целлюлозы; это также один из |
Кристаллическая амилаза получена из солода, под- |
||||
самых важных компонентов питательных сред для |
желудочной железы крупного рогатого скота, а также |
||||
ферментации. Объем производства крахмала состав- |
из клеток Aspergillus oryzae и Bacillus subtilis. Опреде- |
||||
ляет 50 млн т, около 70% – из кукурузы, 20% – из |
лена кристаллическая структура α-амилазы из Bacil- |
||||
картофеля. Лишь около 20% крахмала используется |
lus amyloliquefaciens. Гены многих α-амилаз из раз- |
||||
в чистом виде, 30% подвергается химической моди- |
личных источников клонированы, и путем экспрессии |
||||
фикации, 50% гидролизуется до олигомерных поли- |
получены штаммы-суперпродуценты этого фермента. |
||||
сахаридов (декстринов) и D-глюкозы. Вместо кислот- |
По сравнению с амилазами, выделенными из клеток |
||||
ного гидролиза чаще проводят ферментативный, при |
грибов, бактериальные α-амилазы значительно бо- |
||||
котором меньше побочных процессов. |
|
лее устойчивы при высокой температуре (α-амилаза |
|||
КРАХМАЛ – это высокомолекулярное соединение |
из B. licheniformis активна при 78 °С) и щелочных ус- |
||||
(степень полимеризации 200–5000) из линейных мо- |
ловиях среды. Таким образом, добавленный в мою- |
||||
лекул амилозы (поли-α-1,4-D-глюкоза) и разветвлен- |
щее средство фермент определяет рекомендованные |
||||
ных |
цепей |
амилопектина. Псевдокристаллическая |
условия стирки. |
||
амилоза в воде образует не растворы, а гидратирован- |
β-АМИЛАЗУ можно выделять из мальтозного сиро- |
||||
ные мицеллы; при добавлении иода происходит синее |
па – побочного продукта производства пшеничного |
||||
окрашивание – качественная реакция на крахмал. |
солода, однако в промышленных целях фермент обыч- |
||||
В амилопектине линейные цепи из остатков глюкозы, |
но получают из клеток Bacillus stearothermophilus. |
||||
как |
в амилозе, приблизительно через каждые |
АМИЛАЗЫ, РАСЩЕПЛЯЮЩИЕ α-1,6-СВЯЗИ. Наибо- |
|||
20 остатков имеют характерные точки ветвления, в ко- |
лее важным представителем этой группы ферментов |
||||
торых остатки глюкозы соединены α-1,6-связями. |
является гликоамилаза из Aspergillus niger; наряду с |
||||
В зависимости от источника крахмала соотношение |
гликоамилазой используется другой фермент с ана- |
||||
амилозы и аминопектина может различаться и от это- |
логичной функцией, выделенный из Rhizopus sp. Пул- |
||||
го зависят физические и химические свойства крахма- |
луланазу получают из штаммов Klebsiella pneumoniae |
||||
ла. Крахмал не растворяется в холодной воде. При на- |
или Bacillus cereus. |
||||
гревании в крахмале рвутся водородные связи, и |
ПОЛУЧЕНИЕ. Все указанные ферменты, имеющие |
||||
растворимость крахмала немного увеличивается. Об- |
важное значение для промышленности, получают как |
||||
разование клейстера объясняется сильным повышени- |
классическим методом поверхностной ферментации, |
||||
ем вязкости раствора в результате включения воды в |
так и в биореакторах большого объема (до 120 м3). |
||||
амилопектин (желирование). В таком виде крахмал |
Ферменты выделяются клетками в среду роста, |
||||
можно подвергать химическим модификациям или |
поэтому после отделения клеточной массы культу- |
||||
ферментативному гидролизу. При охлаждении клей- |
ральная жидкость представляет собой раствор фер- |
||||
стера между молекулами амилозы вновь возникают |
ментов. Поскольку производство больших количеств |
||||
водородные связи (ретроградация). Крахмал является |
ферментов для промышленных нужд является эконо- |
||||
важным компонентом многих пищевых продуктов, на- |
мически оправданным, если цены на конечный про- |
||||
пример хлеба или пива. Традиционные технологии |
дукт невысоки, процедура очистки ферментов |
||||
крахмала постоянно совершенствуются. |
|
в достаточной мере упрощена: высокоскоростное |
|||
КРАХМАЛРАСЩЕПЛЯЮЩИЕ ФЕРМЕНТЫ. Для фер- |
центрифугирование и осаждение с последующей под- |
||||
ментативного гидролиза крахмала используются сле- |
готовкой ферментных препаратов к продаже. |
||||
дующие ферменты: α-амилаза (другое название – |
|
||||
экзоамилаза) – случайным образом гидролизует |
|
||||
внутренние α-1,4-гликозидные связи; β-амилаза |
|
||||
(другое название – эндоамилаза) – отщепляет от не- |
|
||||
восстанавливающего конца полимерной цепи мальто- |
|
||||
зу или мальтотриозу; глюкоамилаза (по-другому – γ- |
|
||||
амилаза, |
мальтаза, |
амилоглюкозидаза) |
– |
|
|
гидролизует мальтозу с образованием двух молекул D-глюкозы и расщепляет с низкой скоростью также α-1,6-гликозидные связи; пуллуланаза – селективно расщепляет 1,6-гликозидные связи боковых цепей амилопектина; изоамилазы – катализируют гидролиз α-1,6-гликозидных связей амилопектина.
86
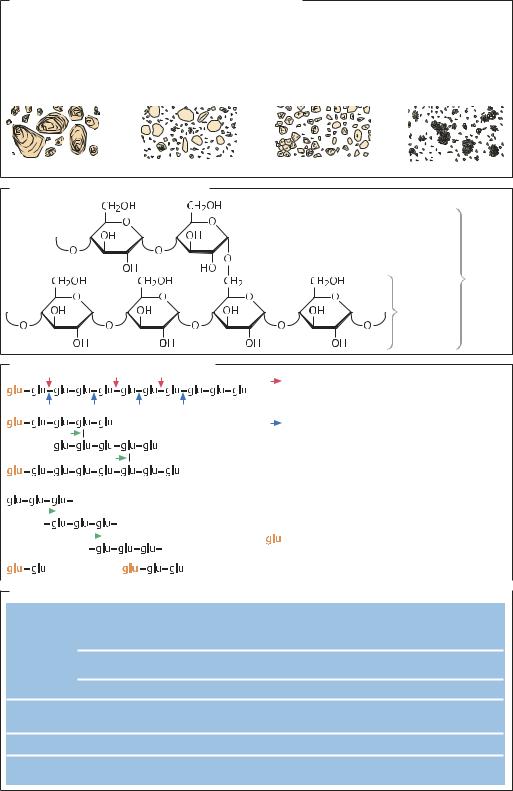
Состав и свойства крахмала из различных источников
Источник |
Амилоза, % |
Амилопектин, % |
Температура образования |
|
Способность |
||
|
|
|
|
|
клейстера, °С |
к набуханию, % |
|
Картофель |
18–23 |
77–82 |
|
56–66 |
> 1000 |
||
Пшеница |
19–25 |
75–81 |
|
52–63 |
21 |
||
Кукуруза |
21–30 |
70–79 |
|
62–72 |
24 |
||
Рис |
17–19 |
81–83 |
|
61–78 |
19 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Картофель |
Пшеница |
Кукуруза |
Рис |
Структура амилозы и амилопектина |
|
|
|
|
|
|
Амило- |
|
|
|
пектин |
|
|
|
Амилоза |
Ферментативный гидролиз крахмала |
|
|
|
|
|
α-Амилаза (1,4-α-D-глюкан-4-глюканогидролаза, |
|
|
|
ФК 3.2.1.1); расщепляет: α-1,4-связи с образова- |
|
|
Амилоза |
нием мальтоз и мальтотриоз |
|
|
β-Амилаза (1,4-α-D-глюкан-мальтогидролаза, |
||
|
|
||
|
Амилопектин |
ФК 3.2.1.2); отщепляет мальтозу с восстанавли- |
|
|
вающего конца |
|
|
|
|
|
|
 Глюкоамилаза (γ-амилаза, 1,4-α-D-глюкано- глюкогидролаза, ФК 3.2.1.41); расщепляет α-1,6-связи
Глюкоамилаза (γ-амилаза, 1,4-α-D-глюкано- глюкогидролаза, ФК 3.2.1.41); расщепляет α-1,6-связи
|
|
|
|
|
|
|
|
|
|
Смесь α-амилазы и глюкоамилазы/пуллуланазы; |
||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Пуллулан |
расщепляет амилозу и амилопектин до D-глюкозы |
||
|
|
|
|
|
|
|
|
|
|
Невосстанавливающий конец |
||
|
|
|
|
|
|
|
|
|
|
|||
|
|
Мальтоза |
Мальтотриоза |
|||||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ферменты |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||||
|
Фермент |
Источник |
Свойства |
|
Условия применения |
|||||||
|
|
|
|
|
|
|||||||
|
α-Амилаза |
Bacillus licheniformis |
Оптимальные условия 60 °С, рН 5,7, |
95–105 °С, рН 6–7, Са2+ |
||||||||
|
|
|
|
|
|
|
|
|
необходимо присутствие Ca2+ |
|
|
|
|
|
|
|
|
Aspergillus oryzae |
Оптимальные условия 50–60 °С, |
< 50 °С, рН > 3,5, Са2+ |
|||||
|
|
|
|
|
|
|
|
|
рН 5,0, необходимо присутствие Ca2+ |
|
|
|
|
|
|
|
|
Ячменный солод |
Оптимальные условия 70 °С, рН 5,5 |
< 70 °С, рН > 4,5 |
|||||
|
β-Aмилаза |
Bacillus |
Стабильна при 75 °С, рН 5,0 |
Для получения мальтозного |
||||||||
|
|
|
|
|
stearothermophilus |
|
|
сиропа |
||||
|
Пуллуланаза |
Klebsiella pneumoniae |
Оптимальные условия 70 °С, рН 5,5 |
55–65 °С, рН 3,5–5 |
||||||||
|
Глюкоамилаза |
Aspergillus niger, |
Стабильна при 70 °С, рН 5,5 |
55–65 °С, рН 3,5–5 |
||||||||
|
|
|
|
|
Rhizopus sp. |
|
|
|
|
|||
87
Ферментативное расщепление крахмала в промышленности
Ферменты |
ВВЕДЕНИЕ. Объем производства крахмала составляет |
значению DЕ, а также позволяет снизить расход |
50 млн тонн в год, почти половина его подвергается |
глюкоамилазы. Использование иммобилизованных |
|
|
ферментативному гидролизу. При этом 15% исполь- |
ферментов в этом случае неприемлемо из-за за- |
|
зуются для получения так называемой изоглюкозы |
медления диффузии в вязком растворе. Следующим |
|
(«сиропа с высоким содержанием фруктозы»), а ос- |
этапом является кристаллизация D-глюкозомоно- |
|
тальной крахмал в виде декстринов и мальтозных си- |
гидрата. В зависимости от количества глюкоамила- |
|
ропов применяется в разнообразных технологических |
зы и продолжительности осахаривания можно полу- |
|
процессах, например как компонент питательной сре- |
чать различные промежуточные продукты гидролиза |
|
ды для ферментации. В Канаде и США сырьем при по- |
крахмала: от мальтодекстрина до глюкозы и мальто- |
|
лучении крахмала служат кукуруза и пшеница. По |
зы. Глюкозные сиропы с различными значениями |
|
сравнению с объемом крахмала, выделенного из этих |
DE широко используются в кондитерской промыш- |
|
культур, объем картофельного и рисового крахмала |
ленности. Для получения мальтозных сиропов при- |
|
незначителен. Во времена Наполеона, когда завоз |
меняют α-амилазу, выделенную из Aspergillus niger. |
|
продуктов, в частности сырья для производства саха- |
Такие сиропы обладают рядом привлекательных тех- |
|
ра – сахарного тростника, в Европу был ограничен, |
нологических свойств: они не темнеют, в отличие от |
|
гидролиз крахмала под действием неорганических ки- |
многих других растворов полисахаридов, не склонны |
|
слот был основным способом получения сахара. В со- |
к кристаллизации, а также обладают повышенной |
|
временной промышленности эта технология больше не |
вязкостью. |
|
используется. |
ЦИКЛОДЕКСТРИНЫ. Под действием циклодекстрин- |
|
ФЕРМЕНТАТИВНОЕ «РАЗЖИЖЕНИЕ» КРАХМАЛА. |
трансферазы из декстринов образуются пяти-, |
|
Кукурузный и пшеничный крахмал получают при пе- |
шестиили семичленные кольца (α-, β- и γ-цикло- |
|
ремалывании зерен в сухих или влажных условиях. |
декстрины соответственно), построенные из остатков |
|
При этом образуются такие важные побочные проду- |
глюкозы. Эти вещества хорошо растворимы в воде, |
|
кты, как кукурузное масло, кукурузный (или пшенич- |
при этом размеры кольца настолько велики |
|
ный) глютен и компоненты, которые используются |
(0,5–0,75 нм), что в его полости могут разместиться |
|
для составления кормовых смесей. Крахмал, поме- |
другие молекулы, например витаминов, ароматиче- |
|
щенный в реактор объемом более 100 м3, несколько |
ских соединений или лекарственных средств. Таким |
|
минут подвергают термической обработке паром |
образом, циклодекстрины в основном обеспечивают |
|
(105–140 °С) в присутствии термостабильной бакте- |
«растворимость» нерастворимых веществ или стаби- |
|
риальной α-амилазы. При инкубации получающегося |
лизацию их взаимодействия с рецепторами. Хираль- |
|
клейстера в течение 2–3 ч при температуре 95 °С |
ный пул производных циклодекстринов используется |
|
под действием бактериальной α-амилазы крахмал на |
в качестве неподвижной фазы для хроматографиче- |
|
98% гидролизуется до мальтодекстрина (декстроз- |
ского разделения оптически активных веществ. |
|
ный эквивиалент DE 15–25) – смеси олигосахари- |
Наибольшее распространение получили β-циклодек- |
|
дов, содержащей небольшие количества моно-, ди- и |
стрины. Соответствующий фермент – циклодекст- |
|
трисахаридов. Мальтодекстрин служит субстратом |
рингликозилтрансфераза (циклодекстриназа) обна- |
|
для дальнейшего осахаривания полисахарида. Кроме |
ружен в клетках Bacillus, обитающих в нейтральных |
|
того, он используется как компонент детского или ди- |
или щелочных условиях. Промышленное получение |
|
етического питания, а также входит в состав концент- |
циклодекстринов из крахмала осуществляется в фер- |
|
ратов супов. |
ментных реакторах. |
|
ФЕРМЕНТАТИВНОЕ «ОСАХАРИВАНИЕ». Этот процесс |
|
|
ведет к образованию сиропа, содержащего глюкозу |
|
|
и мальтозу. В ферментативном осахаривании глав- |
|
|
ную роль выполняет фермент глюкоамилаза из As- |
|
|
pergillus niger. Мальтодекстин охлаждают до темпе- |
|
|
ратуры 60 °С и закисляют среду до рН 4,0. Как |
|
|
правило, непрерывный технологический процесс |
|
|
осуществляется в нескольких резервуарах, чтобы не |
|
|
допустить потери продукта из-за разбрызгивания си- |
|
|
ропа. Осахаривание (т. е. полный гидролиз) в при- |
|
|
сутствии глюкоамилазы продолжается 48–72 ч; |
|
|
продукт – глюкозный сироп с высоким декстрозным |
|
88 |
эквивалентом, DE 97–98. Добавление пуллуланазы |
|
или изоамилазы приводит к еще более высокому |
|
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
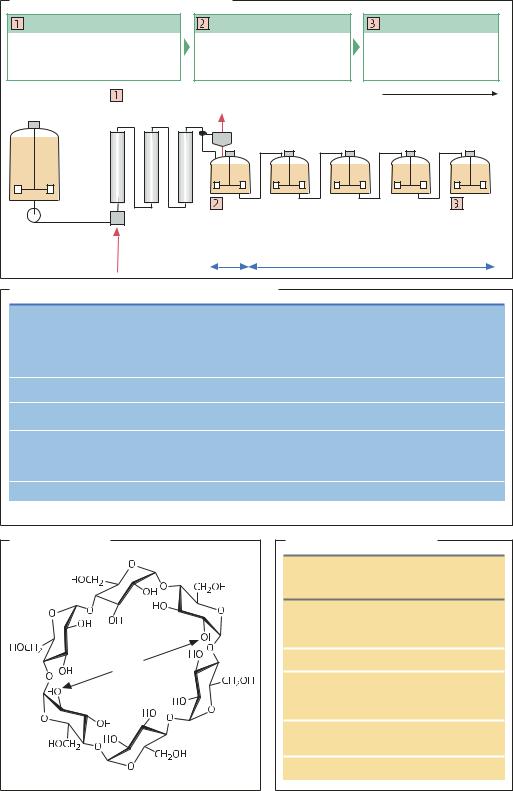
Ферментативное расщепление крахмала |
|
|
|||
Гидролиз кукурузного крахмала |
|
Мальтодекстрины DE 15–20 |
Глюкозный сироп DE 97 |
||
40% м/об, деионизованная вода, |
2–4 ч при 95 °С, |
|
рН 4,2, 60 °С, 2–3 сут., |
||
20 ppm Са2+, рН 6–6,5, 77–105 °С, |
бактериальная α-амилаза |
|
грибная глюкоамилаза |
||
0,15% бактериальной α-амилазы |
|
|
|
|
|
Крахмальное |
Крахмал набухает |
Степень гидролиза возрастает |
|||
молоко |
и превращается |
|
|
|
|
|
в клейстер |
|
Пар |
|
|
|
|
|
|
|
|
|
Варочный |
|
Мальтодекстрин |
|
Глюкозный |
Подача водяного |
аппарат |
|
|
|
сироп DE 97 |
|
|
3 ч |
|
|
|
пара, 5 мин при 105 °С, |
|
|
|
|
|
термостабильная |
|
|
при 95 °С |
2–3 сут. при 60 °С |
|
α-амилаза |
|
|
|
|
|
Продукты ферментативного гидролиза крахмала |
|
|
|||
Гидролизат |
Декстрозный |
Фермент |
Применение |
|
эквивалент, DE* |
|
|
|
|
|
|
Мальтодекстрин |
15–25 |
α-Амилаза |
В пищевой промышленности, имеет хорошее |
реологические свойства (текучесть),
|
|
|
сырье в производстве подсластителей |
|
|||
Мальтозный сироп |
40–45 |
α-Амилаза, |
Подсластитель |
|
|
|
|
|
|
β-амилаза |
|
|
|
|
|
Мальтоза |
50–55 |
α-Амилаза, |
Подсластитель |
|
|
|
|
|
|
глюкоамилаза |
|
|
|
|
|
Мальтозный сироп |
60–70 |
α-Амилаза, |
Подсластитель, сырье для ферментации |
||||
с высокой и сверх- |
|
глюкоамилаза, |
|
|
|
|
|
высокой степенью |
|
пуллуланаза |
|
|
|
|
|
осахаривания |
< 80 |
|
|
|
|
|
|
Изоглюкоза |
97 |
Глюкозоизомераза |
Подсластитель |
|
|
|
|
* Декстрозный эквивиалент оценивает степень гидролиза крахмала. |
|
|
|
|
|
||
Циклодекстрины |
|
|
Свойства циклодекстринов |
|
|||
|
|
|
Цикло- |
|
|
|
|
|
|
|
декст- |
|
|
|
|
|
|
|
рин |
|
α |
β |
γ |
|
|
|
Число |
|
|
|
|
|
|
|
остатков |
|
|
|
|
|
|
|
глюкозы |
|
6 |
7 |
8 |
|
0,52 нм |
|
MR |
|
972 |
1135 |
1297 |
|
|
|
Растворимость |
|
|
|
|
|
|
|
в воде, |
|
|
|
|
|
|
|
100 г/мл |
|
14,5 |
1,85 |
23,2 |
|
|
|
Диаметр |
|
|
|
|
|
|
|
молекулы, нм |
≥ 0,47 |
≥ 0,6 |
≥ 0,75 |
|
α-Циклодекстрин |
|
|
Код CAS |
10016-20-3 |
7585-39-9 |
17465-86-0 |
|
|
|
|
|
|
|
89 |
|
|
|
|
|
|
|
|
|
