
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
Антибиотики
40
Антибиотики: источники, применение и механизмы действия
ВВЕДЕНИЕ. Еще в 1928 г. Александр Флеминг обнару- |
для борьбы с микробными инфекциями, при этом |
|
жил явление, приведшее к открытию антибиотиков: на |
различают антибиотики с широким спектром дейст- |
|
культуре стафилококка он заметил грибковую инфек- |
вия (например, цефалоспорин и тетрациклин) и селе- |
|
цию, остановившую рост бактерий. Лишь 10 лет спу- |
ктивные антибиотики, которые действуют на опреде- |
|
стя Говарду Флори удалось изучить структуру веще- |
ленных возбудителей болезней |
(например, |
ства, вызвавшего остановку роста стафилококковых |
рифампицин активен против легочной формы тубер- |
|
бактерий – пенициллина. Успешные испытания дейст- |
кулеза, амфотерицин В – против грибковых инфек- |
|
вия пенициллина на лабораторных животных, воз- |
ций). Для терапии рака применяют так называемые |
|
можно, вскоре привели бы к его использованию и для |
«противоопухолевые» антибиотики (в |
частности, |
лечения людей, однако эти исследования, проводив- |
адриамицин) – токсичные вещества, действующие |
|
шиеся в рамках большого американо-британского |
как цитостатики. В растениеводстве в качестве пес- |
|
проекта, были прерваны Второй мировой войной. За |
тицидов также используют антибиотики (бластици- |
|
1945 г. в мире было произведено несколько кило- |
дин S и казугамицин): они эффективны в очень низ- |
|
граммов бензилпенициллина. Однако пенициллин |
ких концентрациях и практически безвредны для |
|
действует исключительно на грамположительные бак- |
теплокровных организмов. Некоторые антибиотики |
|
терии, среди которых не столь часто встречаются воз- |
применяют в качестве консервантов при изготовле- |
|
будители заболеваний человека. В 1947 г. Зельман |
нии пищевых продуктов, например пимарицин ис- |
|
Ваксман обнаружил в культуре Streptomyces |
пользуется в сыроварении для защиты от грибковой |
|
griseus антибиотик (стрептомицин), который действо- |
инфекции. Существуют так называемые «кормовые» |
|
вал на грамотрицательные бактерии. В течение пос- |
антибиотики – те, что добавляют в корм сельскохо- |
|
ледующих лет путем систематического скрининга бы- |
зяйственных животных для лучшего усвоения пищи |
|
ло выявлено множество новых антибиотиков и |
и быстрой прибавки в весе. Исключительно важной |
|
разработаны способы их промышленого получения. |
задачей представляется разработка новых антибио- |
|
В результате слишком широкого и зачастую неумест- |
тиков, которые препятствуют возникновению новых |
|
ного применения антибиотиков, как в медицинских це- |
штаммов микроорганизмов, устойчивых к ранее при- |
|
лях, так и в кормовых добавках, стали появляться но- |
менявшимся антибиотикам (в том числе монензин – |
|
вые микроорганизмы – возбудители заболеваний, |
препарат, добавляемый в корм сельскохозяйствен- |
|
обладающие устойчивостью к уже известным анти- |
ных птиц). В биохимических и молекулярных иссле- |
|
биотикам. Поэтому ведутся разработки новых анти- |
дованиях антибиотики используются как селектив- |
|
биотиков, а также осуществляются попытки строго ог- |
ные ингибиторы различных клеточных функций. |
|
раничить область применения уже существующих. |
МЕХАНИЗМ ДЕЙСТВИЯ. Антимикробное действие ан- |
|
Для поиска новых антибиотиков используют скрининг, |
тибиотиков обусловлено подавлением следующих |
|
слияние клеток продуцентов различных антибиотиков |
функций клеток микроорганизма: 1) биосинтез и |
|
и проводят поиск новых мишеней действия антибио- |
функционирование генов; 2) биосинтез клеточных |
|
тиков на основе анализа генома патогенных микроор- |
компонентов; 3) биосинтез и функционирование бел- |
|
ганизмов (gene shuffling). |
ков; 4) биосинтез и функционирование клеточной |
|
ИСТОЧНИКИ. На сегодняшний день более 8000 анти- |
мембраны; 5) биосинтез клеточной стенки. Как пра- |
|
биотиков выделены из микроорганизмов, а около |
вило, действие антибиотика является результатом |
|
4000 получены из других организмов: лишайников, |
сложной цепи его взаимодействий с клеточными |
|
растений и животных. Наиболее важным и широким |
компонентами. У микроорганизмов существует гене- |
|
классом продуцентов антибиотиков являются гри- |
тически запрограммированный механизм приспособ- |
|
бы – актиномицеты. |
ления к изменяющимся условиям среды, поэтому |
|
ПРИМЕНЕНИЕ. Промышленным способом сейчас |
создание новых антибиотиков и появление новых ре- |
|
получают около 200 антибиотиков, при этом боль- |
зистентных штаммов микроорганизмов происходят |
|
шинство препаратов являются полусинтетическими |
практически в одно и то же время. |
|
природными соединениями, т. е. биологическую ак- |
|
|
тивность которых как антибиотиков удалось проявить |
|
|
путем изменений в их молекуле, вносимых химиче- |
|
|
скими или биотехнологическими методами. Примерно две трети объема мирового рынка (32 млрд долл. США) приходится на β-лактамные антибиотики (пенициллины и цефалоспорины), объем их производства составляет более 50 000 т/г. Значительное количество антибиотиков используются в медицине

Источники антибиотиков*
Таксономи- |
Относительная |
ческая |
доля (%) |
группа |
|
Актиномицеты |
50 |
Бактерии |
10 |
Грибы |
20 |
Лишайники |
1 |
Водоросли |
2 |
Растения |
15 |
Животные |
2 |
|
|
* Из примерно 25 000 биологически активных веществ
Объем рынка некоторых антибиотиков*
Тип антибиотика |
Объем рынка |
|
(109 долл. США) |
Цефалоспорины |
9,0 |
Пенициллины/ингибиторы лактамаз |
6,9 |
Хинолон (синтетический) |
5,8 |
Макролиды |
5,7 |
Пептидные антибиотики, гликопептиды |
0,1 |
Аминогликозиды |
0,8 |
Тетрациклины |
0,9 |
Другие вещества |
2,5 |
Всего |
31,7 |
|
|
* Данные 2004 г.
Классификация антибиотиков на основе химического строения
1 |
Углеводные |
Аминогликозиды |
Стрептомицин (медицина), |
|
|
антибиотики |
|
казугамицин (фунгицид на рисовых плантациях) |
|
|
|
|
|
|
2 |
Макроциклические |
Макролидные, полиеновые |
Эритромицин (медицина), |
|
|
лактоны |
антибиотики, ансамицины |
пимарицин (сыроварение), |
|
|
|
|
рифампицин (лечение туберкулеза) |
|
|
|
|
|
|
3 |
Семейство хинона |
Тетрациклины |
Тетрациклин, хлортетрациклин (медицина, |
|
|
|
|
консервант для пищевых продуктов) |
|
|
|
Антрациклины |
Доксорубицин (противоопухолевая терапия) |
|
|
|
|
|
|
4 |
Аминокислотные |
Производные аминокислот |
Циклоспорин (трансплантация органов), |
|
|
и пептидные |
|
фосфинотрицин (растениеводство) |
|
|
антибиотики |
β-Лактамные антибиотики |
Пенициллин, цефалоспорин (медицина), |
|
|
|
Пептидные антибиотики |
бацитрацин (медицина), |
|
|
|
|
виргиниамицин (откорм скота) |
|
|
|
Хромопептиды |
Актиномицин (противоопухолевая терапия) |
|
|
|
Гликопептиды |
Блеомицин (противоопухолевая терапия), |
|
|
|
|
ванкомицин (медицина), авопарцин (скотоводство) |
|
|
|
|
|
|
5 |
N-Содержащие гетеро- |
Нуклеозидные антибиотики |
Полиоксины, бластицидин S |
|
|
циклические соединения |
(фунгицид в растениеводстве) |
||
|
|
|
|
|
6 |
О-Содержащие гетеро- |
Полиэфирные антибиотики |
Монензин (птицеводство) |
|
|
циклические соединения |
|
|
|
|
|
|
|
|
7 |
Алициклические |
Производные циклоалканов |
Циклогексимид (фунгицид) |
|
|
антибиотики |
|
|
|
8 |
Ароматические |
Производные бензола |
Хлорамфеникол (медицина), |
|
|
||||
|
антибиотики |
|
|
|
гризеофульвин (фунгицид) |
|
|
||
Мишени действия антибиотиков |
|
|
|
|
|
|
|||
|
|
Полиеновые |
Клеточная |
β-Лактамные |
Клеточная |
70S-Субъединица |
Новосинте- |
|
|
|
|
рибосомы |
|
||||||
|
Антрациклины |
антибиотики |
стенка |
антибиотики |
мембрана |
|
зированный |
|
|
|
|
|
|
|
|
|
|
белок |
|
|
|
|
|
|
|
30S |
|
|
|
|
ДНК |
Репликация |
|
|
|
Трансляция |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
50S |
|
|
|
Транскрипция |
тРНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
мРНК |
|
Аминокислоты |
|
Эритромицин |
|
||
|
|
|
|
|
Рифампицин |
Тетрациклин |
|
||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
Стрептомицин |
Хлорамфеникол |
41 |
|
|
|
|
|
|
|
|
|
|
|
Антибиотики |
Антибиотики: получение. Устойчивость к антибиотикам |
|||
СКРИНИНГ. Скрининг бактериальных штаммов с це- |
ков – продуктов вторичного обмена веществ – начи- |
|||
|
||||
|
лью выявления антимикробной активности осуществ- |
нается после того, как клетки достигли стационарной |
||
|
ляют по их влиянию на поведение контрольного |
фазы роста. Как правило, антибиотики являются вне- |
||
|
штамма. После того как на штамме выявлена анти- |
клеточными продуктами аэробного обмена веществ и |
||
|
микробная активность, антибиотик выделяют, очища- |
плохо растворяются в воде. По окончании цикла фер- |
||
|
ют и анализируют его структуру. Как правило, у ново- |
ментации клетки удаляют центрифугированием, из |
||
|
го антибиотика строение молекулы похоже на |
среды экстрагируют растворенные в ней питательные |
||
|
строение уже изученных веществ. Чтобы увеличить |
вещества (эти два этапа выделения продукта можно |
||
|
эффективность поиска штаммов-продуцентов анти- |
объединять), а затем продукт очищают перекристал- |
||
|
биотиков, разрабатывают новые методы скрининга, |
лизацией или хроматографически. Промышленные |
||
|
например с использованием биохимических или био- |
процессы получения, очистки и подготовки антибио- |
||
|
логических чипов, применяют новые химико-анали- |
тиков, которые используются в медицинских целях, |
||
|
тические методы, а также ищут возможные мишени |
ведутся под строгим контролем в полном соответст- |
||
|
для действия антибиотика (в библиотеках синтезиро- |
вии с сертифицированными правилами организации |
||
|
ванных соединений ищут вещества, действующие на |
производства и контроля качества лекарственных |
||
|
определенную функцию микроорганизма). |
средств (Good Manufacturing Practice, ISO 9000). |
||
|
УСОВЕРШЕНСТВОВАНИЕ |
ШТАММОВ. Антибиотики |
УСТОЙЧИВОСТЬ (РЕЗИСТЕНТНОСТЬ) К АНТИБИОТИ- |
|
|
являются продуктами вторичного обмена веществ |
КАМ. Микроорганизмы, обладающие устойчивостью |
||
|
у микроорганизмов и выделяются в среду роста |
к антибиотикам, весьма распространены, и это стало |
||
|
в очень небольших количествах (несколько милли- |
главной медицинской проблемой. Неуклонно растет |
||
|
граммов на литр культуральной жидкости). Поэтому, |
число штаммов Salmonella, Escherichia coli, стафило- |
||
|
если обнаруженный антибиотик представляет инте- |
кокков, стрептококков, а в последнее время и Myco- |
||
|
рес, то перед исследователем встает задача повы- |
bacterium tuberculosis (возбудитель туберкулеза), |
||
|
сить уровень его синтеза. Усовершенствование |
устойчивых к целому ряду антибиотиков. Самые важ- |
||
|
штамма заключается в многократном повторении ак- |
ные механизмы, обеспечивающие устойчивость мик- |
||
|
тов мутагенеза с последующей селекцией и обрат- |
роорганизма к действию антибиотиков, следующие: |
||
|
ным «скрещиванием». Таким образом удается повы- |
а) нарушение процесса поступления антибиотика в |
||
|
сить выход антибиотика в 103–106 раз по сравнению |
клетку или ускоренное выведение его из клетки (на- |
||
|
с диким штаммом. Методы генетической инженерии, |
пример, в результате изменения проницаемости |
||
|
например, введение дополнительных копий генов |
мембраны); б) специфические изменения структур, |
||
|
ферментов, играющих ключевую роль в синтезе |
являющихся мишенью действия антибиотика (изме- |
||
|
антибиотиков, также позволяют получать новые |
нения сайта связывания в рибосоме или молекуле |
||
|
штаммы-суперпродуценты. |
ДНК); в) генетически запрограммированные фер- |
||
|
ФЕРМЕНТАЦИЯ И ПЕРЕРАБОТКА. У большинства анти- |
ментативные реакции, обеспечивающие устойчи- |
||
|
биотиков весьма сложная структурная формула, ча- |
вость к антибиотику. Некоторые генетические дефек- |
||
|
сто с несколькими стереоцентрами, поэтому химиче- |
ты могут распространяться среди различных видов |
||
|
ский синтез редко используется для их производства. |
микроорганизмов с помощью плазмид, фагов или |
||
|
Промышленное получение антибиотиков осуществля- |
транспозонов. Таким образом, после обнаружения |
||
|
ется ферментацией в биореакторах. Питательная сре- |
нового антибиотика надо продолжить исследования, |
||
|
да содержит такие недорогие источники углерода и |
чтобы найти его аналоги на основе существующих ан- |
||
|
азота, как меласса, лактоза и соевая мука. По мере |
тибиотиков, применяемых, например, в сельском хо- |
||
|
замедления роста из-за исчерпания питательных ве- |
зяйстве для улучшения роста и профилактики забо- |
||
|
ществ клеточная культура переходит в идиофазу: |
леваний скота. Такие аналоги понадобятся для |
||
|
именно тогда синтезируются антибиотики. Большин- |
борьбы с патогенами, устойчивыми к действию суще- |
||
|
ство штаммов-продуцентов антибиотиков устойчивы к |
ствующих антибиотиков. |
||
|
своим катаболитам только в этом состоянии, поэтому |
|
||
|
для предотвращения |
самоуничтожения система |
|
|
|
должна быстро достичь идиофазы, а затем культиви- |
|
||
|
ровать микроорганизмы в этой фазе. Если в качестве |
|
||
|
продуцента антибиотиков используют грибы, или ак- |
|
||
|
тиномицеты, наряду с оптимизацией состава пита- |
|
||
|
тельной среды особое внимание уделяют концентра- |
|
||
42 |
ции кислорода, так как клетки мицелия весьма |
|
||
чувствительны к аэрации. Образование антибиоти- |
|
|||
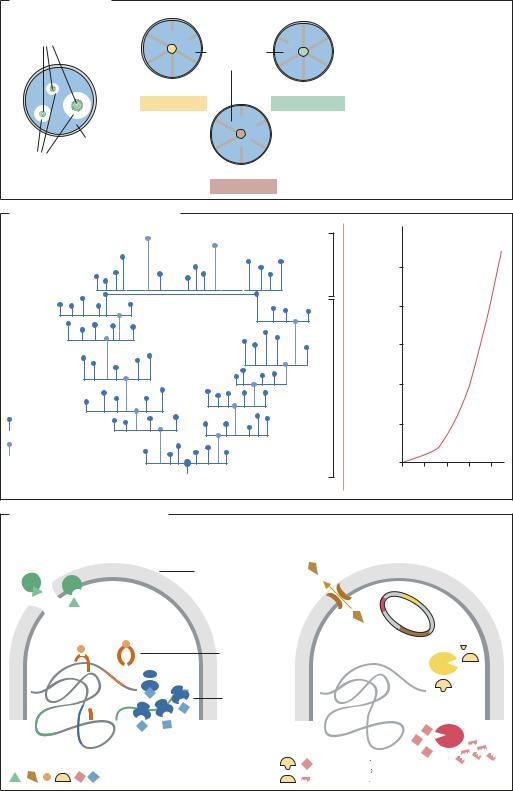
Скрининг и отбор |
|
|
|
|
|
|
Плесневые грибы, |
1 |
|
|
1 |
Пробы микроорганизмов (мазки): |
|
6 |
2 |
|
|
1 |
|
|
синтезирующие |
6 |
2 |
Staphylococcus aureus |
|||
антибиотик |
|
|
|
|
|
(грамположительная |
|
|
Питательная |
|
|
бактерия) |
|
|
5 |
3среда на агаре5 |
3 |
2 |
Streptococcus sp. |
|
|
4 |
|
|
|
|
(грамположительная |
|
|
1 |
4 |
|
бактерия) |
|
|
Пенициллин G |
Гризеофульвин |
3 Escherichia coli |
|||
|
|
6 |
2 |
|
|
(грамотрицательная |
|
|
|
|
бактерия) |
||
|
|
|
|
|
|
|
|
Агар, на котором |
|
|
|
4 |
Pseudomonas aeruginosa |
|
|
|
|
|
(грамотрицательная |
|
|
растет контрольный |
5 |
3 |
|
|
|
Замедленный |
|
|
бактерия) |
|||
микроорганизм |
|
|
|
|
||
рост |
|
|
4 |
|
5 |
Candida albicans (дрожжи) |
контрольного |
|
|
Тетрациклин |
|
6 |
Trichophyton rubrum (грибы) |
микроорганизма |
|
|
|
|||
Усовершенствование штаммов |
|
|
|
|
|
|
|
|
|
|
Гибрид |
|
Обратное скрещивание |
|
|
|
|
|
|
|
|
|
|
|
F7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
50 000 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Пенициллин |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F6 |
|
|
продукта (ед./мл) |
40 000 |
|
|
|
|
|
|
|
|
|
F5 |
|
и селекция |
30 000 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
F4 |
|
20 000 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
Мутагенез |
Выход |
|
|
|
|
||
|
|
|
|
F3 |
|
|
|
|
|
|
|
||
Выход продукта |
|
F2 |
|
10 000 |
|
|
|
|
|||||
в мутанте |
|
|
|
|
|
|
|
|
|||||
Мутант, выбранный для |
|
|
|
|
|
|
|
|
|
|
|||
следующего раунда |
F1 |
|
|
|
|
|
|
|
|
|
|||
скрещивания |
|
|
|
|
|
0 |
|
|
|
|
|||
F1–F7 – дочерние поколения |
Дикий штамм |
|
|
|
|
1940 |
50 |
60 |
70 |
80 |
|||
|
|
|
|
|
|
|
|
|
|||||
Устойчивость к антибиотику |
|
|
|
|
|
|
|
|
|
||||
а Изменение мишени действия антибиотика |
|
б Ферментативные модификации |
|
|
|||||||||
|
Белок, связывающийся с антибиотиком |
или выведение антибиотика из клетки |
|
||||||||||
Ингиби- |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
рование |
|
|
|
Клеточная |
АТРаза, осу- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
стенка |
|
|
|
|
|
|
|
||
|
|
|
|
ществляющая |
|
|
|
|
|
|
|
||
|
|
Ингибирование |
|
|
|
|
|
|
|
|
|||
|
|
|
выведение |
|
|
|
|
|
|
|
|||
|
|
отсутствует |
|
|
|
|
|
|
|
|
|
|
|
Ингиби- |
|
|
Ингиби- |
|
|
Плазмида |
|
|
|
|
|||
рование |
|
|
рование |
|
|
Модифицирующие |
|
|
|
||||
отсут- |
|
|
|
РНК-поли- |
|
|
|
||||||
|
|
|
|
|
ферменты |
|
|
|
|||||
ствует |
|
|
Ингиби- |
мераза |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
рование |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДНК-топо- |
|
|
|
Ферменты, |
|
|||
|
|
|
|
|
изомераза |
|
|
ДНК |
разрушающие |
|
|||
|
|
|
|
|
|
|
|
|
|
антибиотик |
|
||
|
|
|
|
Ингибирование |
|
|
|
|
|
|
|
|
|
|
|
|
|
отсутствует |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Активная |
|
Формы |
|
|
|
|
|
|
|
|
Разные антибиотики |
|
Неактивная |
антибиотиков |
|
|
43 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Антибиотики
β-Лактамные антибиотики:
структура, биосинтез и механизм действия
ВВЕДЕНИЕ. Благодаря высокой эффективности действия, низкой токсичности, а также наличию разработанных методов химического и ферментативного получения β-лактамные антибиотики (производные пенициллина и цефалоспорина) нашли наиболее широкое применение в современной медицине. Мировое производство β-лактамных антибиотиков составляет 30 000 т, а около 50% всего рынка антибиотиков приходится на долю цефалоспорина. В то время как цефалоспорин используется только для лечения человека, пенициллин применяют и в ветеринарии. Наиболее важными веществами, из которых получают полусинтетические β-лактамные антибиотики, являются пенициллин G (бензилпенициллин) и цефалоспорин С. При внесении изменений в молекулярную структуру этих антибиотиков меняются фармакологические свойства и расширяется спектр действия нового антибиотика. Важными характеристиками антибиотиков являются их стабильность в кислых условиях среды (в желудочно-кишечном тракте – при пероральном введении), а также устойчивость к действию β-лакта- мазы – основного фермента, который обеспечивает резистентность бактерий к действию антибиотиков. Как правило, ген β-лактамазы находится в плазмидной ДНК бактерий.
ПЕНИЦИЛЛИН. Грибы вида Penicillium chrysogenum
продуцируют изопенициллин N, имеющий в боковой цепи L-α-аминоадипиновую кислоту. Добавление к среде роста веществ-предшественников, ацильная группа которых участвует в реакции трансацетилирования, позволяет получать производные пенициллина, обладающие различными фармакологическими свойствами. Так, в присутствии фенилуксусной кислоты образуется пенициллин G. Это вещество и получаемая из него 6-аминопенициллановая кислота (6-АРА) – важнейшие промежуточные продукты при производстве полусинтетических пенициллинов и цефалоспоринов.
третьего поколения имеют широкий спектр действия, включающий и грамположительные, и грамотрицательные бактерии, и практически не вызывают побочных эффектов у пациентов.
БИОСИНТЕЗ. В геноме P. chrysogenum найдены три гена, продукты которых участвуют в биосинтезе изопенициллина N. Эти гены расположены рядом друг с другом и образуют так называемый генный кластер. Продукт одного из этих генов – синтетаза – обеспечивает присоединение L-валина и L-цистеина к L-α-ами- ноадипиновой кислоте. Образовавшийся трипептид под действием другой синтетазы превращается в изопенициллин N, содержащий β-лактамное кольцо. На следующем этапе происходит обмен боковой цепи (L-α-аминоадипила) на другие ацильные группы. Эту реакцию катализирует ацил-КоА:изопеницил- лин-N-ацилтрансфераза. Для получения цефалоспоринов осуществляют расширение гетероцикла изопенициллина N при участии фермента экспандазы. О-Ацилтрансфераза, выделенная из A. chrysogenum, модифицирует только 3-ацетоксиметильную группу, не затрагивая N-ациламиногруппу. У A. chrysogenum (в отличие от P. chrysogenum) гены, продукты которых участвуют в биосинтезе цефалоспорина С, расположены на двух различных хромосомах. Эти гены уже клонированы, и ведутся исследования с целью осуществления направленной (искусственной) регуляции биосинтеза антибиотиков.
МЕХАНИЗМ ДЕЙСТВИЯ β-ЛАКТАМНЫХ АНТИБИОТИКОВ. β-Лактамные антибиотики препятствуют образованию поперечных пептидных связей в молекуле муреина – основного компонента клеточных стенок бактерий. Таким образом, антибиотики этой группы действуют на микроорганизмы, содержащие в клеточной стенке муреин. Для человека нежелательные побочные эффекты от приема антибиотиков связаны с возможными нарушениями баланса кишечной флоры и возникновением аллергических реакций.
ЦЕФАЛОСПОРИН. Цефалоспорин С был впервые описан в 1953 г. как новый ряд β-лактамного антибиотика, образующегося в Acremonium chrysogenum (ранее Cephalosporium acremonium). A. chrysogenum
не имеет собственной N-трансацетилазы, поэтому, в отличие от биосинтеза пенициллинов, в этом случае нет возможности обеспечить биосинтез новых фармакологических продуктов добавлением в среду роста тех или иных веществ. Полусинтетические цефалоспорины получают двумя способами: из 7-ами- ноцефалоспорановой кислоты (7-АСА), которая образуется при удалении амидной боковой цепи цефалоспорина С, и ее 3-дезацетоксипроизводного (7-ADCA). В настоящее время существует уже три поколения цефалоспоринов, различающиеся по спе-
44 цифичности действия. Цефалоспорины второго и
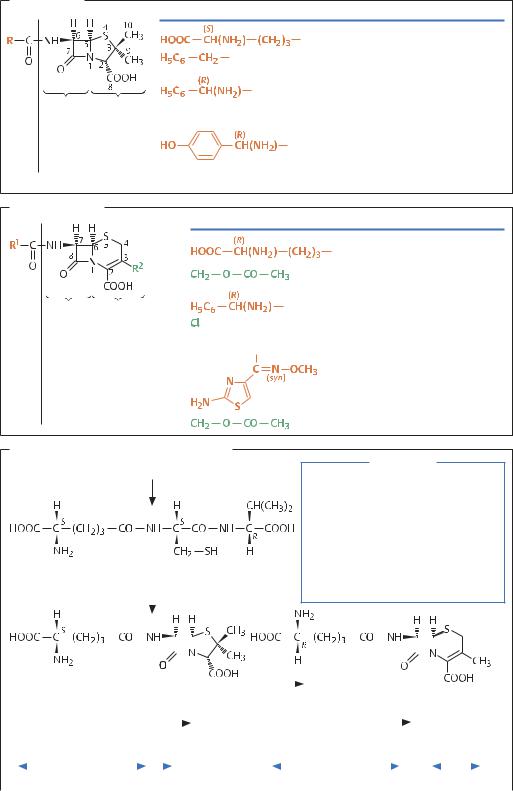
Пенициллин |
|
|
R |
Название |
Свойства |
|||
|
|
|
|
|||||
|
|
|
|
|
Изопенициллин N |
|
|
|
|
|
|
|
|
Пенициллин G Неустойчив в кислой среде, |
|||
|
|
|
|
|
|
|
чувствителен к β-лактамазе |
|
|
|
|
|
|
Ампициллин |
Устойчив в кислой среде, |
||
Ациль- β-Лактам- |
Тиазолиди- |
|
|
чувствителен к β-лактамазе, |
||||
ная |
ное кольцо |
новое кольцо |
|
|
действует также на грам- |
|||
группа |
|
|
|
|
|
|
отрицательные бактерии |
|
|
|
|
|
|
Амоксициллин |
Устойчив в кислой среде, |
||
|
6β-Аминопеницилла- |
|
|
чувствителен к β-лактамазе, |
||||
|
|
|
широкий спектр действия, |
|||||
|
новая кислота (6-АРА) |
|
|
|||||
|
|
|
высокая степень резорбции |
|||||
|
|
|
|
|
|
|
||
Цефалоспорины |
R1/R2 |
|
Название |
Свойства |
||||
|
|
|
|
|
||||
|
|
|
|
|
|
Цефалоспорин С Неустойчив в кислой |
||
|
|
|
|
|
|
|
|
среде, чувствителен |
|
|
|
|
|
|
|
|
к β-лактамазе |
Ациль- β-Лактам- |
Дигидротиази- |
|
Цефаклор |
Устойчив в кислой |
||||
ная |
ное кольцо |
новое кольцо |
|
|
|
среде, не чувствите- |
||
группа |
|
|
|
|
|
|
|
лен к β-лактамазе, |
|
7β-Аминоцефалоспорановая |
|
|
|
широкий спектр |
|||
|
|
|
|
действия |
||||
|
кислота (7-АСА, |
|
|
|
|
|||
|
|
|
|
|
|
|||
|
R2 = CH |
–O–CO–CH |
) |
|
Цефотаксим |
Устойчив в кислой |
||
|
2 |
|
3 |
|
|
|||
|
|
|
|
|
|
|
|
среде, не чувствите- |
|
7β-Аминодезацетоксицефало- |
|
|
|
лен к β-лактамазе, |
|||
|
|
|
|
очень широкий |
||||
|
спорановая кислота (7-АDСА, |
|
|
|
||||
|
|
|
|
спектр действия |
||||
|
R2 = CH3) |
|
|
|
|
|
||
|
|
|
|
|
|
|
||
Биoсинтез и структура генных кластеров |
|
|
|
|
||||
|
L-α-Аминоадипиновая кислота + L-Цистеин + L-Валин |
|
Фермент/ген |
|||||
|
1 ACVS |
pcbAB δ-L-α-Аминоадипил-L-цис- |
||||||
|
|
|
|
1 |
||||
|
|
|
|
2 IPNA |
pcbC |
теинил-D-валин-синтетаза |
||
|
|
|
|
|
Изопенициллин- |
|||
|
|
|
|
|
3 AT |
penDE |
N-синтетаза |
|
|
|
|
|
|
Ацил-КоА: изопенициллин- |
|||
|
|
|
|
|
4 IPNE |
cefD |
N-ацилтрансфераза |
|
|
|
|
|
|
Изопенициллин- |
|||
|
|
|
|
|
|
|
N-эпимераза |
|
δ-L-α-Аминоадипил-L-цистеинил-D-валин |
5 |
REX/H cefEF |
Экспандаза/гидроксилаза |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
AT |
cefG |
Ацил-КоА: цефалоспоран- |
||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
ацилтрансфераза |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изопенициллин N |
|
|
|
|
|
Дезацетоксицефалоспорин C |
|
|
||||||||||||||||||
|
|
|
|
4, 5 |
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пенициллин G |
|
|
|
|
|
|
|
|
|
Цефалоспорин C |
|
|
|||||
|
Структура генных кластеров |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
P. chrysogenum |
|
|
|
|
|
|
|
|
|
|
|
A. chrysogenum |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pcbAB |
|
pcbC penDE |
|
|
|
|
pcbAB |
pcbC |
cefEF cefG |
|
45 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
