
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
продукты |
Биоматериалы |
|
масляной кислоты все чаще находят применение в со- |
||
|
ВВЕДЕНИЕ. Материалы на основе поли-3-гидрокси- |
|
Специальные |
временной промышленности. Необычными свойства- |
|
ми, чрезвычайно интересными для технологического |
||
|
||
|
применения, обладают природные белки натурального |
|
|
шелка (фиброин и спидроин) или белок мидий, поэто- |
|
|
му в настоящее время ведутся активные исследования |
|
|
возможностей получения этих веществ методами ге- |
|
|
нетической инженерии. Производные бактериородоп- |
|
|
сина, синтезируемого Halobacterium salinarum, воз- |
|
|
можно, найдут применение в качестве оптического |
|
|
носителя информации. |
|
|
ПОЛИМЕРЫ, СПОСОБНЫЕ К БИОРАЗЛОЖЕНИЮ. В про- |
|
|
мышленности уже получают из L-молочной кислоты |
|
|
полилактид (Nature WorksTM). Производится также сопо- |
|
|
лимер получаемого биотехнологическим путем 1,3-про- |
|
|
пандиола и терефталевой кислоты (SoronaTM). При полу- |
|
|
чении 1,3-пропандиола используются рекомбинантные |
|
|
штаммы E. coli, метаболизм которых изменен внедрени- |
|
|
ем гена глицерин-дегидратазы методами метаболиче- |
|
|
ской инженерии. Многие микроорганизмы, например |
|
|
Ralstonia eutropha, в определенных условиях способны |
|
|
запасать в клетке полигидроксимасляную кислоту, со- |
|
|
держание которой может достигать 90% сухой клеточ- |
|
|
ной массы. Состав запасных полимеров зависит от со- |
|
|
става питательной среды, поэтому, добавляя в среду |
|
|
роста различные вещества-предшественники, можно уп- |
|
|
равлять процессом образования продукта. Для техноло- |
|
|
гического применения наиболее интересен сополимер |
|
|
3-гидроксимасляной и 3-гидроксивалериановой кислот, |
|
|
который проявляет свойства полипропилена, однако в от- |
|
|
личие от последнего может разлагаться биологическим |
|
|
путем. Получение этого сополимера ферментацией пока |
|
|
очень дорогой процесс, поэтому это вещество находит |
|
|
лишь ограниченное применение – в медицине (препарат |
|
|
Biopol®). Оперон синтеза поли-3-гидроксимасляной кис- |
|
|
лоты содержит 3 гена, которые уже клонированы. Транс- |
|
|
формация растений и клеток Escherichia coli плазмидами, |
|
|
содержащими эти гены, позволила получать поли-3-гид- |
|
|
роксимасляную кислоту с выходом до 95% сухой клеточ- |
|
|
ной массы. Для выделения образующегося в клетках по- |
|
|
лимера используют экстракцию органическими |
|
|
растворителями или энзиматическое расщепление. |
|
|
ФИБРОИН И СПИДРОИН. Белки образуются в специаль- |
|
|
ных железах гусеницы тутового шелкопряда (Bombyx |
|
|
mori) для создания кокона при окукливании, а также в |
|
|
паутинных железах многих паукообразных (например, |
|
|
паука крестовика Nephila claviceps). Натуральное волок- |
|
|
но имеет очень хорошие технические перспективы, в ча- |
|
|
стности для создания парашютной ткани, так как многие |
|
|
их свойства уникальны. Волокна каркасной нити паути- |
|
|
ны, состоящие из белка спидроина, при равной толщине |
|
|
волокна в несколько раз прочнее стали и при этом спо- |
|
|
собны растягиваться на 30% своей длины без разрыва |
|
68 |
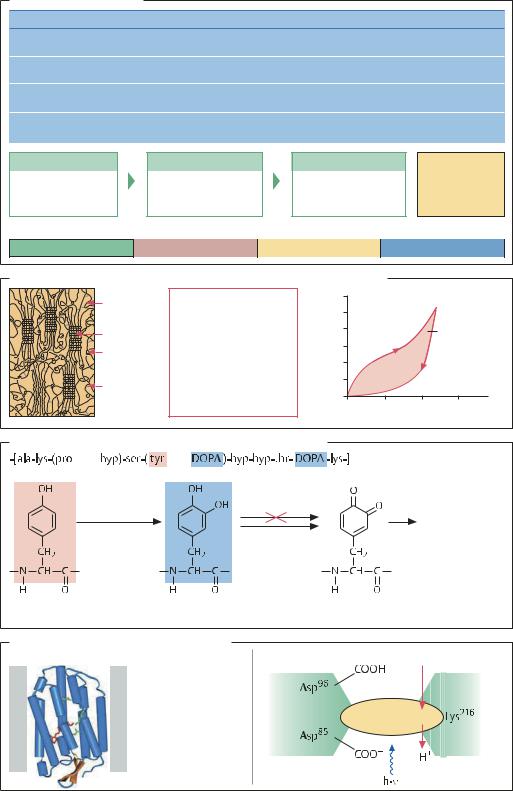
(BioSteelTM). Фиброин и спидроин являются фибрилляр- |
ными белками, гены которых удалось клонировать и модифицировать для экспрессии в клетках E. coli и Pichia pastoris. Выход рекомбинантных белков фиброина и спидроина составляет около 1 г/л.
БЕЛКИ С АДГЕЗИОННЫМИ СВОЙСТВАМИ. Мидии Mytilus edulis обладают способностью прикрепляться к раковинам ракообразных или поверхности обшивки кораблей
итаким образом перемещаться на большие расстояния. Эти моллюски синтезируют специфический белок, проявляющий адгезионные свойства. Белок-предшествен- ник имеет молекулярную массу 130 кДа и состоит преимущественно из полярных аминокислот – тирозина, серина, треонина, лизина и пролина. В ходе посттрансляционных модификаций остатки тирозина и пролина преобразуются в о-гидрокситирозин или 3- или 4-гидро- кси-L-пролин соответственно. На воздухе полипептиптидные цепи полимеризуются, и образуются дихиноны. Методами генетической инженерии удалось осуществить гетерологичную экспрессию фрагмента белка адгезии размером 25 кДа в клетках E. coli с достаточно высоким выходом. Однако в этих клетках-хозяевах не происходит посттрансляционных модификаций белков, поэтому выделенный рекомбинантный продукт обрабатывают ферментом тирозиназой, который гидролизует остатки тирозина до о-гидрокситирозина, что обеспечивает образование поперечных сшивок между полипептидными цепями. Полученный белок используют в медицинских целях, в том числе в стоматологии для заполнения полостей в зубе.
БАКТЕРИОРОДОПСИН. Галобактерия Halobacterium salinarum обитает в средах с повышенным содержанием поваренной соли: концентрация NaCl 3–5 М является нормальной для ее роста. При фототрофном росте бактериородопсин служит в качестве протонного насоса
итаким образом снабжает клетку энергией. Молекулы бактериородопсина формируют в клеточной мембране агрегаты (бляшки), которые легко выделяются в составе так называемой «пурпурной мембраны», на 75% по массе состоящей из белков и на 25% из липидов. Препараты «пурпурных мембран» очень стабильны. Кофактор бактериородопсина ретиналь и процесс его цис-транс- изомеризации связан с необычной функцией: бактериородопсин действует как светозависимый протонный насос, число оборотов которого может достигать 100 в секунду. В восстановленной форме бактериоро-
допсин имеет пурпурный цвет (λmax = 570 нм), а при протонировании ретиналя и остатка лизина в положе-
нии 216 становится желтым (λmax = 410нм). Замена определенных аминокислотных остатков путем направленного мутагенеза дает возможность регулировать скорость циклического светозависимого изменения цвета бактериородопсина. Чрезвычайно перспективным представляется использование бактериородопсина и его производных в качестве оптического носителя информации (фотоэлемента).
Ферментация и очистка |
|
|
|
|
|
|
|
|
|
|
||
Организм |
Продукт |
|
|
|
|
Фирма-производитель |
|
|||||
Ralstonia eutropha |
Сополимер 3-гидроксимасляной |
|
|
Metabolix (коммерческий продукт) |
|
|||||||
|
и 3-гидроксивалериановой кислот |
|
|
|
|
|
|
|
|
|||
Escherichia coli |
Поли(3-гидроксимасляная кислота), |
|
|
ATO-DLO |
|
|
|
|
|
|||
|
клонирован оперон из Alcaligenes latus |
|
|
|
|
|
|
|
|
|||
Lactobacillus |
Хирально чистый L-полилактид |
|
|
Cargill (производство) |
|
|||||||
|
из L-молочной кислоты |
|
|
|
|
|
|
|
|
|
||
E. coli |
Сополимер пропан-1,3-диола |
|
|
DuPont, Geneva (производство) |
|
|||||||
с генами Klebsiella |
и терефталевой кислоты |
|
|
|
|
|
|
|
|
|
||
Ralstonia eutropha |
|
|
Биореактор |
|
|
Выделение |
|
|
|
|
|
|
Гетеротрофный |
|
Непрерывная |
|
Ферментативные |
|
|
Выход продукта |
|
||||
штамм-продуцент |
|
ферментация, глюкоза, |
методы |
|
|
|
более 80 г/л |
|
||||
|
|
пропионовая кислота, |
|
|
|
|
|
(более 2 г/л в ч) |
|
|||
|
|
30 °С, ~ 40 ч |
|
|
|
|
|
|
|
|
|
|
Структура оперона синтеза поли(3-гидроксимасляной кислоты) из Ralstonia eutropha |
|
|
|
|
||||||||
Промотор |
|
|
РНК-Синтаза |
3-Кетотиолаза |
Ацетил-КоА-редуктаза |
|
||||||
Волокна каркасной нити паутины паука-крестовика (Nephila claviceps) |
|
|
|
|
||||||||
|
β-слои |
Основной компонент |
разрыв,на |
Н/м |
6 |
|
|
|
|
|
||
|
(gly–gly–x)12-спейсер |
|
|
|
|
|
|
|||||
|
Аморфные |
белка каркасной нити |
|
|
5 |
|
|
|
|
|
||
|
нити |
|
(gly–pro–gly–gly–x)3–63 – |
|
|
|
|
|
|
|
||
|
|
|
|
2 |
4 |
|
|
|
Энергия, |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Водородные |
Эластичность |
35% |
Прочность |
9 |
3 |
|
|
|
выделяющаяся |
|
|
|
10 |
|
|
|
|
в виде тепла |
|
|||||
|
Сшивки |
|
|
|
|
2 |
|
|
|
|
||
|
|
|
Прочность |
4 109 Н/м2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мостики |
Прочность |
105 Дж/кг |
|
|
0 |
|
|
|
|
|
|
|
|
|
на разрыв |
|
|
0 |
5 |
|
10 |
15 |
|
|
|
|
|
|
|
|
|
|
Растяжимость, % |
|
|||
Белок с адгезионными свойствами из мидий Mytilus edulis |
|
|
|
|
|
|
|
|||||
или |
|
|
или |
|
|
|
|
hyp |
= |
4-гидроксипролин |
|
|
|
|
|
|
|
|
|
|
DOPA = |
3,4-дигидрокси- |
|
||
|
|
|
|
|
|
|
|
|
|
фенилаланин |
|
|
Тирозиназа |
|
Аскорбиновая кислота |
|
|
Окисление, |
|
||||||
из шампиньонов |
|
|
|
|
|
|
|
образование |
|
|||
|
|
|
|
|
|
|
|
|
|
сшивок |
|
|
|
|
|
|
Кислород воздуха |
|
|
|
|
и связывание |
|
||
|
|
|
|
|
|
|
|
с поверхностью |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
Генно-инженерный |
|
|
Активирован в виде преполимера, |
|
|
|
|
|
|
|
||
белок-предшественник |
|
стабилизирован аскорбиновой кислотой |
|
|
|
|
|
|||||
Бактериородопсин как протонный насос |
Донор |
|
|
|
|
|
Поток |
|
||||
Цитоплазма |
|
|
|
|
|
|
|
|
|
|||
|
|
|
протонов |
|
|
|
|
|
протонов |
|
||
|
|
Бактериородопсин |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
(по рентгено- |
|
|
|
|
|
|
|
|
|
|
Мембрана |
Мембрана |
структурным данным |
|
|
|
|
|
|
|
|
|
|
с разрешением 0,23 нм); |
|
|
Ретиналь-CH = NH |
|
|
|||||||
|
|
|
|
|
|
|||||||
|
|
красным |
|
|
|
|
|
|||||
|
|
обозначен ретиналь, |
|
|
|
|
|
|
|
|
|
|
|
|
зеленым – |
|
|
|
|
|
|
|
|
|
|
|
|
Asp85, Asp96, Lys216 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Акцептор |
|
|
|
|
|
Протонирование |
|
|
|
|
|
|
протонов |
|
|
|
|
|
ретиналя |
69 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Специальные продукты
70
Биотрансформация
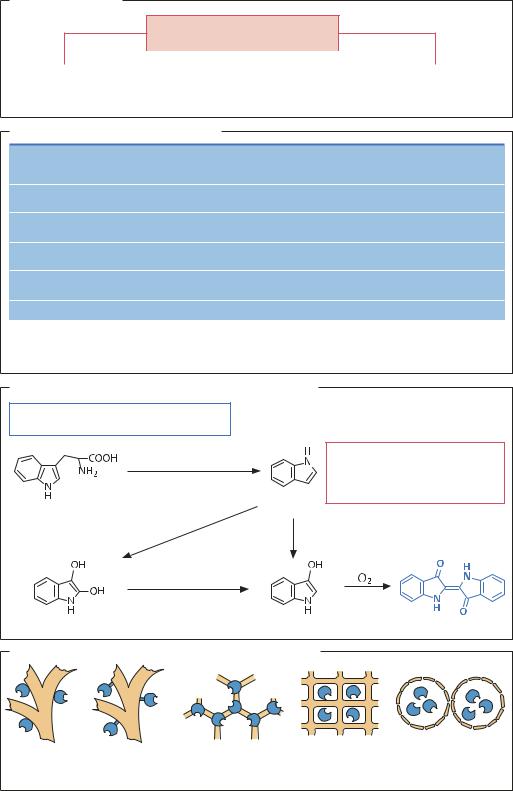
ВВЕДЕНИЕ. Биотрансформация – основная функция организма, необходимая для осуществления нормального обмена веществ и обезвреживания токсичных веществ, в том числе ксенобиотиков. В биотехнологии под термином биотрансформация принято понимать биокатализ, то есть процесс ферментативного превращения природного или синтетического вещества-предшественника в продукт с необходимыми свойствами. Этот процесс может осуществляться в биореакторах микроорганизмами, целыми клетками животных или растений, их отдельными органеллами, а также иммобилизованными на носителях ферментами или клетками. В последние годы сильно выросла роль генетической инженерии для усовершенствования ферментов и получения рекомбинантных организмов. Термины «биокатализ», «ферментация» и «биотрансформация» в определенном смысле можно считать синонимами. Процесс биотрансформации включает одну или несколько стадий – каждую стадию катализирует отдельный фермент. Применение выделенных ферментов имеет ряд преимуществ: можно оптимизировать температурный режим проведения реакции, так как белок менее чувствителен к условиям среды, чем более сложные биологические системы (органеллы или клетки); отсутствует необходимость поддерживать стерильные условия реакции; фермент взаимодействует с субстратом более эффективно. Использование органелл или целых клеток более целесообразно в тех случаях, когда выделение фермента является сложной процедурой, если очищенный фермент нестабилен или процесс трансформации включает несколько стадий и все необходимые ферменты находятся в клетке.
МИКРООРГАНИЗМЫ используются как для получения природных метаболитов (например, глу-тами- новой кислоты), так и для превращения веществ, которые не являются их природными субстратами (к примеру, гидроксилирование стероидов по 11β-по- ложению). Как правило, ферменты катализируют реакции нормального метаболизма с высокой субстратной специфичностью. Экспрессия генов или целых генных кластеров, клонированных из другого организма, позволяет расширить круг веществ, подвергающихся биотрансформации, как, к примеру, в случае получения индиго. Метаболическая инженерия и белковый дизайн позволяют находить новые метаболические пути на основе анализа генома и играют важную роль при разработке методов промышленной биотрансформации.
ЖИВОТНЫЕ КЛЕТКИ широко используются для синтеза фармацевтических препаратов и антител в биореакторах. В настоящее время проводятся работы по созданию искусственной печени для очищения крови от некоторых токсических веществ. Токсины, выделен-
ные из крови при диализе, в результате биотрансформации осаждаются на молекулах альбумина.
РАСТИТЕЛЬНЫЕ КЛЕТКИ. Наиболее известный пример использования растительных клеток для биотрансформации – реакции специфического гидроксилирования. Так, в культуре Digitalis lanata в результате гидроксилирования дигитоксина по положению 12 образуется дигоксин. Биореакторы для культивирования растительных клеток по техническим причинам пригодны лишь для ограниченного числа процессов, например для синтеза таксола (PaclitaxelTM) Taxus brevifolia.
ОТДЕЛЬНЫЕ ФЕРМЕНТЫ целесообразно применять, если реакция биотрансформации проходит всего в одну стадию и может протекать в системе in vitro. В большинстве случаев в промышленности используются не требующие кофакторов ферменты, например, для реакций субстрат-специфичного гидролиза или этерификации. В последнее время изолированные ферменты также стали применяться для осуществления реакций присоединения по двойной связи, например в карбонильных группах.
«РЕКОМБИНАНТНЫЕ» ПУТИ ОБМЕНА ВЕЩЕСТВ. Наиболее яркими примерами использования этого подхода в промышленности является производство аскорбиновой кислоты в Erwinia herbicola (см. ранее)
иполучение индиго в рекомбинантных клетках Escherichia coli. Методами генетической инженерии в клетках E. coli была дополнительно усилена активность триптофаназы, катализирующей реакцию превращения триптофана в индол, а затем с помощью TOL-плазмиды в клетки был введен ген нафталиндиоксигеназы из Pseudomonas sp. Полученный рекомбинантный штамм обладает способностью синтезировать индиго – один из самых распространенных красителей для тканей. Для получения L- или D-аминокислоты из синтетических гидантоинов используют хозяйские клетки E. coli с векторными кассетами, содержащими рекомбинантные гидантоиназы
икарбамилазы («синтетическая биология»).
Биотрансформация
Биотрансформация/биокатализ
Синтез необходимых продуктов
|
|
|
|
|
|
|
Ферментация |
|
«Покоящиеся» или иммобилизованные клетки |
|
Ферментативный катализ |
||
Живые клетки |
|
Kлетки в виде суспензии |
|
Один или несколько |
||
в биореакторах |
|
или иммобилизованные на носителе |
|
изолированных ферментов |
||
|
|
|
|
|
|
|
Примеры реакции биотрансформации
Реакция |
Организм/Фермент |
Процесс |
Фирма-разработчик |
|
|
|
|
D-сорбит → L-сорбоза |
Acetobacter suboxydans |
Ф |
Roche |
Фенил-D-лактат → 4-гидроксифенил- |
Beauveria gossypii |
Ф |
BASF |
D-лактат |
|
|
|
Фумаровая кислота → |
Escherichia coli |
ИмК |
Tanabe, DSM |
L-аспарагиновая кислота |
|
|
|
D-глюкоза → D-фруктоза |
Глюкозоизомераза |
ИмК, ИмФ |
Novo, Clinton |
|
из Streptomyces sp. |
|
|
D,L-ацетоксиметоксифенилэтиламин → |
Липаза из Pseudomonas |
ИмФ |
BASF |
L-фенилэтиламин |
cepacia |
|
|
Триптофан → индиго |
Pекомбинантный штамм E. coli |
ИмРК |
Genencor |
||
Ф – ферментация; |
|
|
|
|
|
ИмК – иммобилизованные клетки; |
|
|
|
|
|
ИмФ – иммобилизованные ферменты; |
|
|
|
|
|
ИмРК – иммобилизованные рекомбинантные клетки |
|
|
|
|
|
Производство индиго в рекомбинантных штаммах E. coli |
|
|
|||
Мутантный штамм E. coli – |
|
|
|
|
|
суперпродуцент индола |
|
|
|
|
|
|
|
|
Клонирование генов |
||
|
Триптофаназа |
|
из Pseudomonas sp.: |
||
|
|
|
а нафталиндиоксигеназа |
||
|
|
|
б ксиленоксидаза |
||
Триптофан |
|
Индол |
|
|
|
|
а |
б |
Ксиленоксидаза |
|
|
|
Нафталин- |
|
|||
|
|
|
|
|
|
|
диоксигеназа |
|
|
|
|
Спонтанная дегидратация |
|
|
|
|
|
цис-Индол-2,3-дигидродиол |
|
Индоксил |
|
Индиго |
|
Некоторые способы иммобилизации клеток и ферментов |
|
|
|||
Адсорбция |
Ковалентное |
Образование |
Включения |
Микрокапсулирование |
на носителе |
связывание |
поперечных |
в нерастворимый |
|
|
с носителем |
сшивок |
гель |
|
71
