
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
Биотехнология в медицине
152
Антитела
ВВЕДЕНИЕ. Антитела – это белки, обеспечивающие защитную функцию иммунной системы. Они циркулируют в крови и лимфе позвоночных животных. Антитела обладают способностью высокоспецифично связываться с антигеном, в качестве которого может выступать чужеродный белок, токсин, полисахарид или липосахарид оболочки вируса или патогенного микроорганизма. Образование специфических антител начинается при попадании антигена в организм; при аутоиммунных заболеваниях такая реакция провоцируется собственными белками. Даже низкомолекулярные соединения (гаптены), будучи связанными с подходящими носителями, могут вызывать образование специфических антител. Метод пассивной иммунизации основан на использовании антител в качестве вакцин против инфекции и отравления токсинами. Антитела также находят широкое применение в лабораторной практике: они служат для выявления специфических белковых продуктов. Очистка рекомбинантных антител в промышленности осуществляется иммуннохроматографическими методами. СТРУКТУРА АНТИТЕЛ. К антителам относятся иммуноглобулины. Иммуноглобулины человека по структуре и функциям принято делить на пять классов: IgG, IgM, IgA, IgE и IgD. IgG, преобладающий среди других иммуноглобулинов сыворотки крови, представляет собой тетрамер из двух идентичных легких (L) цепей и двух идентичных тяжелых (Н) цепей, соединенных дисульфидными мостиками. В молекуле иммуноглобулина различают константные (структурные) (CH, CL) и вариабельные (VH, VL) домены. Иммуноглобулины расщепляются протеиназой папаином на два Fab-фрагмента и один Fc-фрагмент. Fc- фрагмент (от англ. fragment crystallizable – способный кристаллизоваться) взаимодействует с рецепторами на клеточной поверхности, а Fab-фраг- мент (от англ. аntigen binding fragment – связывающий антиген) связывает антиген. Антиген-связываю- щий фрагмент содержит участки, определяющие комплементарность антител к антигену (СDR – от англ. complementarity-determining regions). Эти участки называют гипервариабельными, так как они проявляют очень высокую изменчивость аминокислотной последовательности: 6 комплементарных областей построены из 20 аминокислот, следовательно, согласно комбинаторике, теоретически возможно 206 × 20 = 20120 вариантов строения Fab.
БИОСИНТЕЗ АНТИТЕЛ. Антитела синтезируются исключительно В-лимфоцитами. Огромное разнообразие антител обеспечивается благодаря тому, что для каждого типа цепей существует набор генных сегментов (в сумме их число превышает 1000), которые объединяются случайным образом в процессе рекомбинации. Кроме того, сам процесс рекомбинации при
образовании дочерних В-клеток оказывается не очень точным – часто происходят мутации (случайные выпадения или вставки нуклеотидов) в областях генов, кодирующих вариабельные участки иммуноглобулинов. Таким образом достигается большое разнообразие фенотипов иммуноглобулинов при сравнительно небольшом размере генома.
ПОЛУЧЕНИЕ АНТИТЕЛ. Поликлональные антитела – это смесь антител, образованных В-лимфоцитами в ответ на введение антигена. Различные антитела узнают различные части молекулы антигена (эпитопы), поэтому препарат поликлональных антител всегда в какой-то мере гетерогенный. Обычно антитела выделяют из обогащенной антителами сыворотки крови, которую получают путем многократного введения антигена животным (кролику, овце, козе, корове, лошади). Иммунизацию можно повторять через 1–2 недели, и из крупных животных (лошади, коровы или козы) удается получать значительные количества сыворотки. Антитела из сыворотки выделяют осаждением и хроматографически. Для повышения специфичности сыворотки к определенному антигену применяют методы аффинной хроматографии с иммобилизованным белком А из Staphylococcus aureus. Этот белок (MR 42) с высокой специфичностью связывается с Fc-фрагментом IgG. Очищенный препарат IgG подвергают лиофилизации в стерильных условиях; его можно хранить в холодильнике в течение нескольких лет. Промышленное производство антител осуществляется в строгом соответствии с «Правилами организации производства и контроля качества лекарственных средств», принятыми Всемирной организацией здравоохранения.
РИСКИ. В организм антитела вводят парентерально (то есть в обход желудочно-кишечного тракта), так как в пищеварительном тракте они нестабильны. Антитела, полученные из животных, распознаются иммунной системой человека как чужеродные, поэтому при повторном введении возможно возникновение иммунной реакции. В медицине эту проблему решают частой сменой антител, полученных из различных животных. Альтернативой может быть использование антител, выделенных из крови доноров. Хотя в развитых странах существуют крупные банки донорской крови, где кровь доноров тщательно проверяется на наличие инфекционных агентов, все же риск заражения при использовании антител из крови доноров остается достаточно высоким.
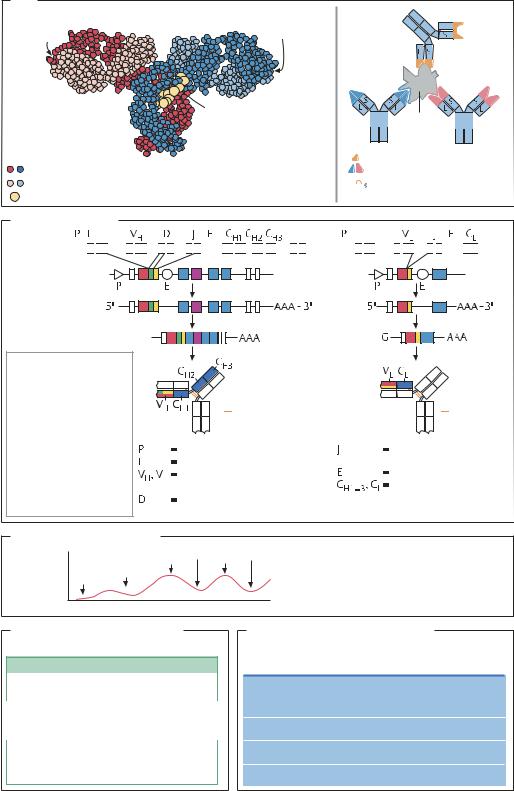
IgG
Антиген-связывающий |
|
|
центр антитела – Fab-фрагмент |
Fab-фрагмент |
Паратоп |
паратоп |
|
|
(CDR 1) |
|
(CDR 1) |
(CDR 2) |
|
(CDR 2) |
(CDR 3) |
|
(CDR 3) |
Fc-фрагмент
Тяжелые цепи (Н) Легкие цепи (L) Углеводный компонент
Биосинтез антител
Углеводная цепь
CDR 1–3 = Участки, определяющие комплементарность антител к антигену
Антитело С
Антитело В |
Антитело А |
|
|
|
Антиген |
Различные паратопы антитела
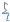
 Различные эпитопы антигена
Различные эпитопы антигена
Гаметная ДНК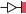







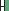


















 Перестройки генома
Перестройки генома
В-клеточная ДНК |
|
|
|
Транскрипция |
|
||
|
|
|
|
|
|
||
|
|
|
|
|
Сплайсинг |
|
|
Большое разнообразие |
|
|
|
Трансляция |
|
||
|
|
|
|
|
|
||
фенотипов: |
|
|
|
|
|
|
|
VL: 250 V и 4 J-сегментов × |
|
|
|
|
|
||
3 варианта соединения = |
|
|
|
|
|
|
|
3000 VL; |
|
|
|
|
Цистеиновые |
|
Цистеиновые |
VH: 250 V, 15 D и 4 J-сег- |
|
|
|
мостики |
|
мостики |
|
ментов × 3 = 45 000 VH; |
|
|
|
|
|
|
|
3000 L-цепей × 45 000 |
|
Промотор |
|
|
Соединительный сегмент |
||
H-цепей = 1,35 × 108 |
|
|
|
||||
|
Лидерная последовательность |
J (от англ. joining) |
|||||
вариантов антител, вклад |
|
||||||
также вносят соматические |
Вариабельные домены |
|
Энхансер |
||||
мутации, полученные |
|
тяжелых или легких цепей |
|
Константные домены |
|||
в период созревания |
|
Сегмент D (от англ. diversity – |
|
тяжелых или легких цепей |
|||
специфических антител |
|
разнообразие) |
|
|
|||
Поликлональные антитела |
|
|
|
|
|
||
|
|
3 |
2 |
3 |
2 |
|
|
Титр антител |
|
|
1 |
Инъекция антигена |
|||
|
2 |
|
|
||||
1 |
|
|
2 |
Повторная инъекция антигена |
|||
|
|
|
|||||
|
|
|
3 |
Взятие крови |
|
||
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Недели |
|
|
|
|
|
Очистка хроматографическими |
|
|
Коммерчески доступные антитела |
||||
методами |
|
|
|
|
Некоторые коммерчески доступные поликлональные |
||
|
|
|
|
|
|||
Несколько литров крови |
|
|
антитела для пассивной иммуннизации |
||||
|
|
|
|
|
|||
Удаление клеток крови центрифугированием, |
|
Антитела |
Источник |
получение плазмы |
|
||
|
|
|
|
|
|
Против столбнячного токсина |
Сыворотка лошади |
|
|
||
Фракция IgG |
|
||
|
|
|
|
Осаждение этанолом или сульфатом аммония |
|
Против возбудителя сонной болезни |
Сыворотка лошади |
|
|
|
|
Очистка |
|
Против вируса кори |
Сыворотка человека |
Хроматографическая очистка, |
|
Иммуноглобулин G |
Сыворотка человека |
аффинная хроматография с белком А |
|
153
медицине |
Моноклональные антитела |
|
которые представляют собой смесь различных анти- |
||
|
ВВЕДЕНИЕ. В отличие от поликлональных антител, |
|
в |
тел, продуцируемых В-лимфоцитами в ответ на |
|
Биотехнология |
||
введение животному антигена, препараты монокло- |
||
|
||
|
нальных антител гомогенны. Для их получения ис- |
|
|
пользуют гибридомную технологию, то есть создают |
|
|
«бессмертную» линию клеток, продуцирующих анти- |
|
|
тела определенной специфичности. |
|
|
ТЕХНОЛОГИЯ ГИБРИДОМ. Животных (обычно мышей) |
|
|
иммунизируют антигеном. Когда в организме живот- |
|
|
ного количество антител достигает высокого уровня, |
|
|
из селезенки выделяют лимфоциты. Затем осущест- |
|
|
вляют слияние этих клеток с клетками миеломной |
|
|
линии, которые обладают способностью к неограни- |
|
|
ченному росту. Часть полученных слитых клеток |
|
|
способны продуцировать антитела, как исходные |
|
|
лимфоциты, и обладают способностью к неограни- |
|
|
ченному росту, как клетки миеломы. Такие клетки |
|
|
удается выделить из смеси специальными иммуно- |
|
|
логическими методами селекции. Подходящие клоны |
|
|
замораживают при низкой температуре, и они сохра- |
|
|
няют способность к образованию антител в течение |
|
|
многих лет. |
|
|
ВЫДЕЛЕНИЕ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ. Клетки |
|
|
гибридомы обладают способностью к неограниченно- |
|
|
му росту. Их выращивают в культуре, а затем из |
|
|
культуральной жидкости выделяют моноклональные |
|
|
антитела (до 30 мг/л). В состав среды роста, кроме |
|
|
глюкозы и глутамина, входит сыворотка зародыша |
|
|
теленка, богатая важнейшими цитокинами и другими |
|
|
веществами, необходимыми для роста (например, |
|
|
лактоферрином). В настоящее время широкое рас- |
|
|
пространение получили сложные искусственные сре- |
|
|
ды. Клетки гибридомы обычно растут в аэробных ус- |
|
|
ловиях на поверхности среды, однако их можно |
|
|
выращивать и в суспензии. Для их роста необходимо |
|
|
постоянное поступление в среду кислорода и СО2. |
|
|
В лабораторных условиях клетки гибридомы выращи- |
|
|
вают в медленно вращающихся емкостях. Для |
|
|
получения антител в промышленных масштабах ис- |
|
|
пользуют биореакторы объемом до 10 м3 (в основ- |
|
|
ном реакторы с механическим перемешиванием или |
|
|
эрлифтные реакторы), в которых клетки гибридом |
|
|
культивируют на особых питательных средах с под- |
|
|
держанием постоянного уровня О2 и СО2. В период |
|
|
разработки технологии ферментации гибридом клет- |
|
|
ки выращивали на носителях с большой площадью |
|
|
поверхности, например керамических носителях с |
|
|
крупными порами, что защищало их от механическо- |
|
|
го повреждения, однако в настоящее время для про- |
|
|
мышленного получения антител, как правило, ис- |
|
|
пользуют суспензии свободных клеток гибридом. |
|
154 |
Процесс ферментации осуществляется в периодиче- |
|
ском или в непрерывном режиме, в последнем слу- |
чае выход продукта может достигать нескольких граммов антител на литр культуры. Для концентрирования культуральной жидкости часто используют методы ультрафильтрации, после которой следует первичная очистка антител методом аффинной хромато-графии с белком А, а затем – тонкая очистка, включающая ионообменную и гель-хроматогра- фию для удаления посторонних белков и агрегатов антител.
ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА. Медицинское применение мышиных моноклональных антител для лечения или диагностики заболеваний человека в системе in vivo влечет за собой риск возникновения иммунной реакции, так как антиген-связывающие участки антител мышей и человека могут значительно отличаться друг от друга. Иммунизация человека в экспериментальных целях невозможна по этическим соображениям, в то время как культивирование клеток миеломы человека является чрезвычайно сложной технической задачей. По этим причинам были разработаны другие методы получения антител: 1) в клеточных культурах лимфоцитов человека при добавлении в среду роста антигена и специфических факторов (таких как гормоны роста и цитокины) (иммунизация in vitro); 2) из селезенки иммунодефицитных мышей, которым введены лимфоциты человека; 3) получение рекомбинантных мышиных антител, несущих антиген-связывающие участки антител человека.
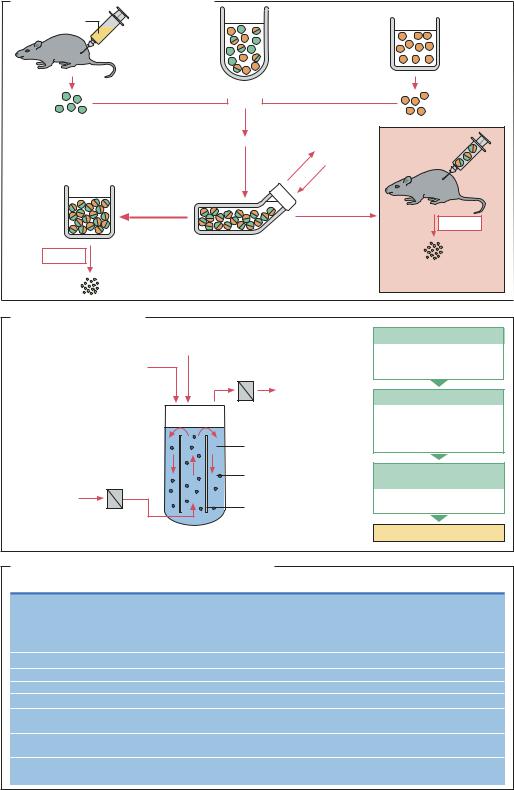
Получение моноклональных антител |
|
|
|
Антиген |
|
|
|
|
|
|
Культура |
|
|
|
клеток |
|
|
|
миеломы |
Слияние клеток в присутствии полиэтиленгликоля |
|
||
Клетки |
|
|
Клетки миеломы |
селезенки |
Отбор |
|
|
|
|
||
|
слившихся |
|
|
|
клеток |
Замораживание |
|
|
|
Индукция |
|
|
Отбор клеток, |
Размора- |
|
|
роста опухоли |
||
|
синтезирующих |
||
|
живание |
|
|
|
антитела |
|
|
|
желаемой |
|
|
Получение |
специфичности |
|
|
больших |
|
|
|
объемов |
|
|
|
клеточных |
|
|
in vivo |
культур |
|
|
|
in vitro |
|
|
Антитела |
|
|
|
|
|
|
|
Запрещено законом |
Антитела |
|
|
об использовании |
|
|
лабораторных животных |
|
Ферментация и очистка |
|
|
|
|
Стерильная среда |
|
Собранные клетки |
|
|
Центрифугирование, |
|
|
|
|
|
Посевной материал |
Стерильный |
концентрирование |
|
фильтр |
внеклеточной среды |
||
|
|
Отработанный |
Неочищенный белок |
|
|
газ |
|
|
|
Анионообменная хромато- |
|
|
|
|
|
|
|
|
графия с использованием |
|
|
|
белков А или G, |
|
|
Эрлифтный реактор |
гель-хроматография |
Стерильный |
|
Клетки гибридомы |
Моноклональные |
фильтр |
|
антитела |
|
|
|
||
Подача воздуха |
|
|
Подготовка препарата, |
|
Центральная труба |
контроль качества |
|
|
|
||
|
|
|
Несколько г/л |
Примеры применения моноклональных антител |
|
||
(некоторые препараты находятся на стадии испытаний) |
|
||
Название |
Применение |
Белок-мишень/функция |
Антитела |
|
|
|
|
Различные |
Диагностика |
Гонадотропин, гормон роста, раковые |
Мышиные |
|
|
эмбриональные антигены, герпес, |
|
|
|
Legionella и др. |
|
Zenapax™ |
Трансплантация почек |
Блокирует IL-2α-субъединицу |
Человеческие |
CEA-Scan™ |
Онкологические заболевания |
Раковый эмбриональный антиген |
Мышиные |
Remicade™ |
Болезнь Крона |
Блокирует TNF-альфа |
Химерные |
Omalizumab™ |
Аллергия, астма |
Блокирует IgE |
Человеческие |
Amevive™ |
Псориаз |
Антиген белка CD2 лимфоцитов |
Фрагмент челове- |
|
|
|
ческих антител |
Erbitux™, |
Рак кишечника |
Блокирует рецепторы VEGF |
Человеческие |
Avastin™ |
|
|
|
Zevalin™, |
Неходжкинская лимфома |
Индуцирует лизис B-клеток |
Химерные |
Rituxan™ |
|
|
|
155
