
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
Антибиотики |
β-Лактамные антибиотики: промышленное получение |
|
|||
ВВЕДЕНИЕ. В молекуле пенициллина в гетероцикле |
для производства полусинтетических пенициллинов |
||||
|
|||||
|
три стереоспецифических центра, следовательно, |
и цефалоспоринов. В современном производстве хи- |
|||
|
при химическом синтезе могут образовываться во- |
мический гидролиз практически полностью заменен |
|||
|
семь стереоизомеров (3(S):5(R):6(R)), из которых |
на ферментативный гидролиз под действием иммо- |
|||
|
лишь один стереоизомер проявляет биологическую |
билизованной пенициллин-G-амидазы из E. coli. Оп- |
|||
|
активность. По сравнению с химическим синтезом |
тимальными условиями для реакции гидролиза явля- |
|||
|
ферментация с использованием оптимизированных |
ются рН 7,5–8,0 и температура 35–40 °С. Высокая |
|||
|
штаммов Penicillium chrysogenum представляется |
стабильность фермента позволяет повторять цикл |
|||
|
значительно более выгодной с экономической точки |
до 1000 раз, поэтому реакцию проводят в непрерыв- |
|||
|
зрения. Добавление в среду роста алифатических |
ном режиме. В результате последующей очистки |
|||
|
или ароматических карбоновых кислот позволяет по- |
продукта |
осаждением и фильтрацией получают |
||
|
лучать различные производные – предшественники |
6-АРА высокой степени чистоты, а затем ее либо |
|||
|
других антибиотиков, среди которых наибольшее |
подвергают ацилированию по положению 6 для полу- |
|||
|
значение имеют пенициллины V и G. Пенициллин G |
чения полусинтетических пенициллинов, либо пре- |
|||
|
используется для производства 6-аминопеницилла- |
вращают в 7-ADCA – промежуточное соединение в |
|||
|
новой кислоты (6-АРА) – важнейшего продукта при |
синтезе цефалоспоринов. |
|
||
|
получении полусинтетических пенициллинов и цефа- |
ЦЕФАЛОСПОРИНЫ И 7-A(D)CA. Метод ферментатив- |
|||
|
лоспоринов. |
ного получения цефалоспоринов с использованием |
|||
|
ПЕНИЦИЛЛИН G И 6-АМИНОПЕНИЦИЛЛАНОВАЯ КИС- |
Acremonium chrysogenum аналогичен |
описанному |
||
|
ЛОТА (6-АРА). В промышленности при получении пе- |
выше способу производства пенициллинов, однако |
|||
|
нициллина G используют штаммы-суперпродуценты |
в случае цефалоспоринов выход продукта несколько |
|||
|
P. chrysogenum, культуру которых выращивают в био- |
ниже. A. chrysogenum не имеет собственной N-транс- |
|||
|
реакторах с рабочим объемом до 200 м3. Чтобы из- |
ацетилазы, поэтому все полусинтетические антибио- |
|||
|
бежать подавления роста клеток катаболитами, фер- |
тики ряда цефалоспоринов синтезируют на основе |
|||
|
ментацию осуществляют в непрерывном режиме, |
7-аминоспорановой кислоты (7-АСА) или ее дезаце- |
|||
|
т. е. в биореактор постоянно подают свежую культу- |
токсипроизводного (7-ADCA). 7-ACA получают путем |
|||
|
ральную среду. Для образования и роста мицелия |
гидролиза в мягких условиях. По экономическим и |
|||
|
грибов необходимо хорошее снабжение кислородом, |
экологическим причинам все большее распростране- |
|||
|
поэтому в ферментерах предусмотрены специальные |
ние приобретает двухстадийный процесс. Получение |
|||
|
приспособления для аэрации и тщательного переме- |
7-АСА начинается с иммобилизованной оксидазы D- |
|||
|
шивания культуры. Сложная питательная среда |
аминокислот. На этой стадии путем окислительного |
|||
|
содержит лактозу в качестве источника углерода, |
дезаминирования образуется α-кетоадипил-7-ACA, |
|||
|
а жидкий кукурузный экстракт служит источником |
которая спонтанно декарбоксилируется до глутарил- |
|||
|
азота. Синтез антибиотиков начинается примерно че- |
7-ACA. В ходе реакции, катализируемой иммобили- |
|||
|
рез 40 ч, т. е. по окончании фазы роста. Идиофаза – |
зованной |
глутарил-7-ACA-ацилазой, |
образуется |
|
|
период, когда происходит синтез антибиотиков, – |
7-ACA. Из нее можно получить до 50 полусинтетиче- |
|||
|
длится около 100 ч, и в это время в среду добавля- |
ских цефалоспоринов. Одностадийный гидролиз осу- |
|||
|
ют фенилуксусную кислоту. Клетки секретируют пе- |
ществляют с использованием цефалоспорин-7-аци- |
|||
|
нициллин G в культуральный бульон. После отделе- |
лазы. Для получения 7-ADCA и производных |
|||
|
ния мицелия фильтрацией или центрифугированием |
цефалоспоринов используют рекомбинантные штам- |
|||
|
культуральную жидкость подвергают двухстадийной |
мы Penicillium chrysogenum, в которых клонирован ген |
|||
|
экстракции с использованием амилацетата (или бу- |
экспандазы из Acremonium chrysogenum или Strepto- |
|||
|
тилацетата) при рН 2,5–3,0 и 0–3 °С. Метод основан |
myces clavuligerus. Образующаяся адипил-ADCA рас- |
|||
|
на том, что большинство антибиотиков хорошо рас- |
щепляется амидазой (например, из Pseudomonas |
|||
|
творяются в органических растворителях, практиче- |
diminuta). Расширение кольца пенициллина до деза- |
|||
|
ски не смешивающихся с водой. Непрерывную экс- |
цетоксицефалоспорина также возможно во внекле- |
|||
|
тракцию антибиотика из водной фазы в органическую |
точных условиях с использованием иммобилизован- |
|||
|
можно осуществлять в противоточном режиме, при |
ных ферментов. |
|
||
|
котором две жидкие фазы движутся в противополож- |
|
|
|
|
|
ных направлениях. Затем первичный продукт (около |
|
|
|
|
|
3 т/сут. в биореакторе с объемом 110 м3) перекри- |
|
|
|
|
|
сталлизовывают. Следующий этап переработки за- |
|
|
|
|
46 |
ключается в гидролизе пенициллина G с образовани- |
|
|
|
|
ем 6-АРА – важнейшего соединения, необходимого |
|
|
|
||
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
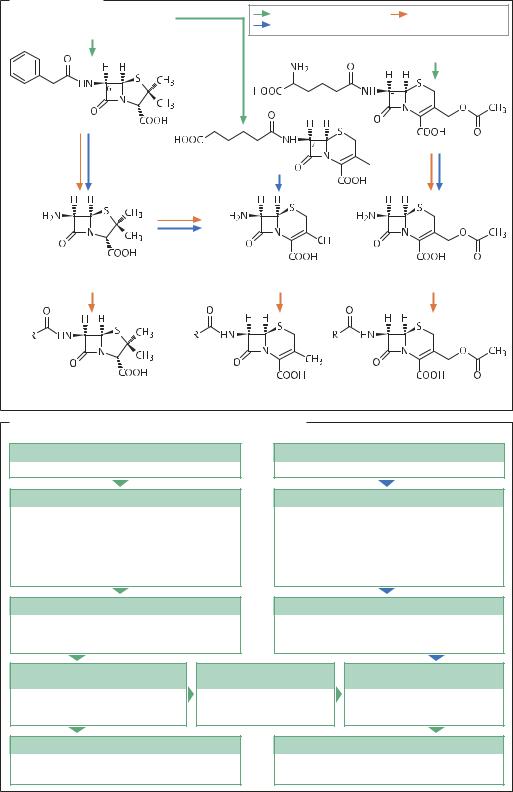
Методы синтеза |
|
|
|
|
|
Penicillium chrysogenum |
|
Ферментация |
|
Дополнительные |
|
На среде с фенилуксусной кислотой |
|
Ферментативный катализ |
химические реакции |
||
|
Экспандаза; |
|
|
Acremoneum chrysogenum |
|
|
|
|
|
Ферментация |
|
|
глутариловая |
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
Пенициллин G |
|
|
|
|
|
Иммобили- |
|
|
|
|
Цефалоспорин С |
зованная |
Глутарил-3-дезацетокси- |
|
|
Иммобили- |
|
пенициллин-G- |
|
|
|||
амидаза |
цефалоспорин* |
|
|
|
зованный |
|
|
|
|
|
фермент |
6-Аминопенициллановая |
7-Аминодезацетоксицефало- |
|
7-Аминоцефало- |
||
кислота (6-АРА) |
спорановая кислота (7-ADCA) |
спорановая кислота (7-АСА) |
|||
Полусинтетические пенициллины |
|
Полусинтетические цефалоспорины |
|||
* Производное 7-ADCA за счет расширения цикла пенициллина (in vivo) или 6-АDA (биотехнологическим путем) |
|||||
Промышленное получение β-лактамных антибиотиков |
|
|
|||
Антибиотики пенициллинового ряда |
|
Антибиотики цефалоспоринового ряда |
|||
Посевной материал |
|
|
Посевной материал |
||
Суспензия спор P. chrysogenum |
|
Суспензия спор А. chrysogenum |
|||
Предферментация, ферментация |
|
Предферментация, ферментация |
|||
Лактоза, жидкий кукурузный экстракт, CaCO3; |
Ферментация с добавлением субстрата, усиленное |
||||
ферментация с добавлением субстрата (глюкозы), |
снабжение кислородом в течение 120 ч; |
||||
усиленное снабжение кислородом; добавление |
добавление жирных кислот, например |
||||
веществ-предшественников, например D-фенил- |
метилолеата, приводит к повышению выхода |
||||
уксусной кислоты, приводит к образованию био- |
продукта; > 17 г/л после 150 ч ферментации |
||||
синтетических пенициллинов; |
|
|
|
|
|
выход: > 30 г/л после 120 ч ферментации |
|
|
|
|
|
Первичная обработка |
|
|
Первичная обработка |
||
1) Отделение мицелия |
|
1) |
Отделение мицелия |
|
|
2) Экстракция в противотоке с использованием |
2) |
Ионообменная хроматография, осаждение |
|||
амилацетата или бутилацетата |
|
|
или адсорбция на амберлите ХАD |
||
Ферментативный гидролиз |
Реакция |
|
Химический гидролиз |
||
с образованием 6-АРА |
расширения кольца |
с образованием 7-АСА |
|||
Иммобилизованная |
Четырехстадийная |
|
Иммобилизованные оксидаза |
||
пенициллин-G-амидаза из E. coli, |
химическая реакция, |
|
D-аминокислот и глютарил- |
||
в непрерывном режиме, при 37 °C |
выход ~ 70% |
|
|
7-АСА-ацилаза, выход > 90% |
|
Полусинтетические пенициллины |
|
Полусинтетические цефалоспорины |
|||
Присоединение ацильных боковых групп |
Присоединение ацильных боковых групп |
||||
(реакция Шоттена–Баумана) |
|
(реакция Шоттена–Баумана) |
|||
|
|
|
|
|
47 |
Антибиотики |
Пептидные антибиотики |
|
|||
и антибиотики – производные аминокислот |
|||||
|
|||||
|
ВВЕДЕНИЕ. В предыдущем разделе обсуждались ме- |
организмов. Нерибосомный синтез пептидов возмо- |
|||
|
тоды получения β-лактамных антибиотиков – важней- |
жен благодаря функционированию специальных фер- |
|||
|
шей группы антибиотиков, применяемых в медицине. |
ментных комплексов – синтетаз, по строению сход- |
|||
|
В настоящее время продемонстрировано антимикроб- |
ных с синтетазой жирных кислот у эукариот. |
|||
|
ное действие более 500 веществ, состоящих из пеп- |
В этих ферментативных реакциях образуются корот- |
|||
|
тидов или являющихся производными аминокислот. |
кие линейные полипептиды, которые затем замыка- |
|||
|
Некоторые из этих соединений используются в меди- |
ются в цикл, образуя, например, лантибиотики. Раз- |
|||
|
цине, в частности для стимуляции заживления ран, |
мер таких пептидов, как правило, не превышает |
|||
|
а другие нашли применение в сельском хозяйстве. |
20 аминокислотных остатков. Они формируют в |
|||
|
К этой группе антибиотиков относятся циклосерин, |
фосфолипидной мембране каналы, проницаемые |
|||
|
фосфинотрицин, циклические пептидные антибиотики |
для катионов. Кроме того, в их состав часто входят |
|||
|
(грамицидин, бацитрацин), хелатообразующие пепти- |
небелковые аминокислоты, а также дополнительные |
|||
|
ды (блеомицин), хромопептиды (актиномицин), а так- |
структурные элементы. Большинство пептидных ан- |
|||
|
же депсипептиды (виргиниамицин). Большинство |
тибиотиков, синтезированных вне рибосом, являют- |
|||
|
этих соединений получают из клеток стрептомицетов, |
ся сильными токсинами, поэтому они применяются |
|||
|
а некоторые – из других грамположительных микро- |
лишь для специальных целей, например для зажив- |
|||
|
организмов, в том числе стрептококков и бацилл. |
ления ран или ожогов. Бацитрацин применяется в |
|||
|
АНТИБИОТИКИ – ПРОИЗВОДНЫЕ АМИНОКИСЛОТ. |
качестве кормовой добавки; циклоспорин из Tolypoc- |
|||
|
Образующийся в процессе жизнедеятельности Strep- |
ladium inflatum – иммуносупрессор (назначается при |
|||
|
tomyces orchidaceus D-циклосерин представляет |
трансплантации органов). Колистин (полимиксин Е) |
|||
|
собой аналог D-аланина – вещества, входящего в со- |
из клеток Bacillus polymyxa иногда используется |
|||
|
став муреина клеточной стенки бактерий. Антибак- |
как антибактериальный препарат при лечении |
|||
|
териальное действие D-циклосерина заключается |
инфекций, вызванных грамотрицательными бакте- |
|||
|
в ингибировании |
аланинрацемазы, |
участвующей |
риями. Цитостатик блеомицин, образующийся в |
|
|
в синтезе муреина. В отличие от многих других анти- |
клетках Streptomyces verticillus, относится к важ- |
|||
|
биотиков D-циклосерин действует на Mycobacterium |
ным препаратам противораковой терапии. Блеоми- |
|||
|
tuberculosis, поэтому в сочетании с рифампицином |
цин в комплексе с Fe2+ способен действовать в |
|||
|
он показан при лечении туберкулеза легких (заме- |
качестве ДНКазы, т. е. осуществлять разрывы в дву- |
|||
|
тим, что в Западной Европе в последние годы |
цепочечной ДНК. Актиномицин, синтезирующийся |
|||
|
туберкулез почти не встречается). Аланил-аланил- |
многими штаммами Streptomyces, узнает в молекуле |
|||
|
фосфинотрицин, |
выделенный из |
Streptomyces |
ДНК палиндромную последовательность 5'-TGAC-3' |
|
|
hygroscopicus, является аналогом L-глутамина и ин- |
и взаимодействует с нею, блокируя трансляцию |
|||
|
гибирует глутаминсинтетазу растений. Промышлен- |
ДНК, и в результате останавливает транскрипцию |
|||
|
ное получение фосфинотрицина (Glyphosat®, Ba- |
(при высоких концентрациях – репликацию). Ранее |
|||
|
sta®) основано на химическом синтезе этого |
актиномицин использовался в противораковой тера- |
|||
|
соединения. Клонирование гена ацетилтрансферазы |
пии. В антибиотиках группы депсипептидов, действу- |
|||
|
из S. hygroscopicus в сельскохозяйственных растени- |
ющих на грамположительные бактерии, аминокис- |
|||
|
ях обеспечивает устойчивость трансгенных растений |
лотные остатки соединены между собой поочередно |
|||
|
к фосфинотрицину. |
|
|
эфирными и амидными связями. Один из предста- |
|
|
ПЕПТИДНЫЕ АНТИБИОТИКИ. Пептидные антибиотики |
вителей этого ряда препаратов виргиниамицин – |
|||
|
синтезируются как на рибосомах, так и вне их. Син- |
продукт жизнедеятельности Streptomyces virginiae и |
|||
|
тез на рибосомах приводит к образованию линейных |
широко применяется при откорме скота и в птице- |
|||
|
полипептидов, которые подвергаются посттрансля- |
водческом хозяйстве. Ряд сидерохромов представ- |
|||
|
ционным модификациям. Примером такой модифи- |
лен пептидными антибиотиками, содержащими ионы |
|||
|
кации может служить реакция эпимеризации – пре- |
железа и гидроксамовую кислоту. Они используются |
|||
|
вращение L-аминокислоты в D-аминокислоту. Так, |
при лечении заболеваний, связанных с нарушениями |
|||
|
низин – пептидный антибиотик, образующийся на |
обмена железа. |
|||
|
рибосомах в клетках некоторых штаммов молочно- |
|
|||
|
кислых бактерий. Его антимикробное действие за- |
|
|||
|
ключается в ингибировании образования цитоплаз- |
|
|||
|
матической мембраны грамотрицательных бактерий, |
|
|||
|
поэтому препарат низина используют в производстве |
|
|||
48 |
кисломолочных продуктов в качестве консервирую- |
|
|||
щего средства, препятствующего росту других микро- |
|
||||
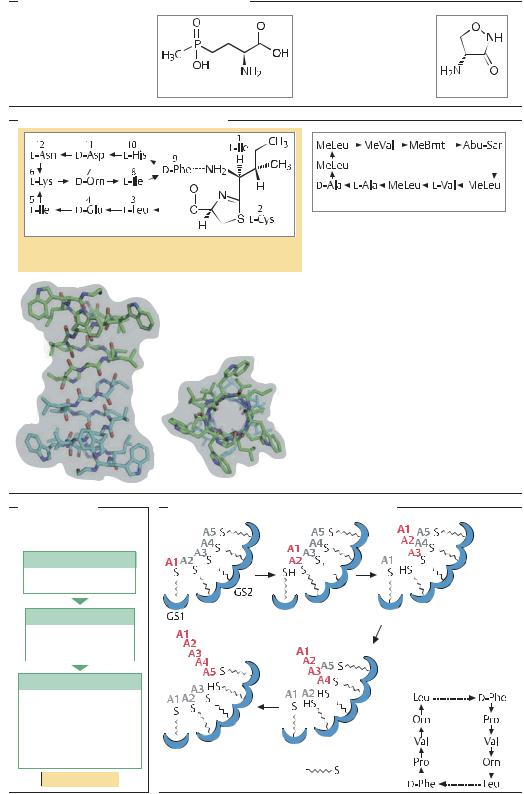
Антибиотики – производные аминокислот
С5Н12NO4Р |
|
|
|
|
С3Н6N2O2 |
|
|
|
|
|
|
|
|
|
|
||
MR |
181,13 |
|
|
|
MR |
102,09 |
|
|
Код CAS |
35597-44-5 |
|
|
|
Код CAS |
68-41-7 |
|
|
|
(S)-Форма |
|
|
|
|
|
|
|
|
|
Фосфинотрицин |
|
|
|
|
Циклосерин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Циклические пептидные антибиотики
Бацитрацин
С66Н103N17O16S
хорошо растворим в воде
вид сбоку
Ферментация
(производство
бацитрацина):
Предферментация
Реактор 1–3 м3, 6 ч при 37 °С
Биореактор
Около 100 м3, 30 ч при 7 °С, сахароза, отходы переработки сои, соли
Обработка
Для медицинских целей: экстракция 1-бутанолом, ионообменная хроматография; Производство кормовой добавки: высушивание биомассы распылением
9 г/л за 30 ч
|
|
|
|
|
Циклоспорин А |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С62Н111N11O12 |
|
|
|
|
MR |
1422,71 |
|
MR |
1202,63 |
Код CAS 59865-13-3 |
|
|
|
Abu |
L-Аминомасляная кислота |
||||
|
Код CAS |
1405-87-4 |
|
||||
|
|
Sar |
Саркозин |
||||
|
|
|
|
||||
|
|
|
|
MeBmt |
Бутенилдиметилтреонин |
||
Грамицидин А, |
|
|
MeLeu |
N-Метиллейцин |
|||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
А- и B-цепи |
|
|
|
|
|
|
|
|
Антибиотик |
Метод получения |
|||||
в фосфолипидной |
|||||||
мембране (1MAG) |
Фосфинотрицин |
В основном химический |
|||||
|
|
|
|||||
|
|
|
|
|
|
синтез |
|
|
|
|
Бацитрацин А |
Bacillus licheniformis |
|||
|
|
|
Полимиксин |
Bacillus polymyxa |
|||
|
|
|
Грамицидин |
Bacillus sp. |
|||
|
|
|
Блеомицин |
Streptomyces verticillus |
|||
|
|
|
Циклоспорин |
Tolypocladium inflatum |
|||
|
|
|
Виргиниамицин |
Streptomyces virginiae |
|||
|
вид сверху |
Валиномицин |
Streptomyces fulvisimus |
||||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
Биосинтез грамицидина S (Bacillus brevis)

 L-Phe
L-Phe  D-Фенил-
D-Фенил-
aланин (D-Phe)

 L-Пролин (Pro)
L-Пролин (Pro)

 L-Валин (Val)
L-Валин (Val)
 L-Орнитин (Orn)
L-Орнитин (Orn)

 L-Лейцин (Leu)
L-Лейцин (Leu)
Грамицидин S
GS1 = синтетаза 1, |
130 кДа |
|
|
|
|
|
|
|
|
||
GS2 = синтетаза 2, |
500 кДа |
Пантеин |
49 |
||
