
- •Содержание
- •Предисловие
- •Предисловие ко 2-му изданию
- •Введение
- •Этапы развития биотехнологии
- •Биотехнология сегодня
- •Биотехнологическое производство пищевых продуктов
- •Алкогольные напитки
- •Пивоварение
- •Ферментация в пищевой промышленности
- •Пищевые продукты и молочнокислое брожение
- •Этиловый спирт
- •1-Бутанол, ацетон
- •Уксусная кислота
- •Лимонная кислота
- •Молочная и глюконовая кислоты
- •Аминокислоты
- •L-Глутаминовая кислота
- •D,L-Метионин, L-лизин и L-треонин
- •Антибиотики
- •Антибиотики: источники, применение и механизмы действия
- •Антибиотики: получение. Устойчивость к антибиотикам
- •β-Лактамные антибиотики: промышленное получение
- •Гликопептидные, полиэфирные и нуклеозидные антибиотики
- •Аминогликозидные антибиотики
- •Тетрациклины, хиноны, хинолоны и другие ароматические антибиотики
- •Поликетидные антибиотики
- •Получение новых антибиотиков
- •Специальные продукты
- •Витамины
- •Нуклеозиды и нуклеотиды
- •Биодетергенты и биокосметика
- •Микробные полисахариды
- •Биоматериалы
- •Биотрансформация
- •Биотрансформация стероидов
- •Ферменты
- •Ферменты
- •Ферментативный катализ
- •Ферменты в клинических анализах
- •Тесты с помощью ферментов
- •Применение ферментов в промышленных технологиях
- •Ферменты в производстве моющих средств
- •Ферменты, расщепляющие крахмал
- •Ферментативное расщепление крахмала в промышленности
- •Ферментативное превращение сахаров
- •Утилизация целлюлозы и полиозы
- •Использование ферментов в целлюлозно-бумажной промышленности
- •Пектиназы
- •Ферменты в производстве молочных продуктов
- •Использование ферментов в хлебобулочной и мясоперерабатывающей промышленности
- •Ферменты в кожевенной и текстильной промышленности
- •Перспективы получения ферментов для промышленных технологий
- •Белковая инженерия
- •Пекарские и кормовые дрожжи
- •Пекарские и кормовые дрожжи
- •Белки и жиры из одноклеточных организмов
- •Аэробная очистка сточных вод
- •Анаэробная очистка сточных вод и переработка ила
- •Биологическая очистка газовых выбросов
- •Биологическая очистка почв
- •Микробиологическое выщелачивание руд и биокоррозия
- •Инсулин
- •Гормон роста и другие гормоны
- •Гемоглобин, сывороточный альбумин и лактоферрин
- •Факторы свертывания крови
- •Антикоагулянты и тромболитики
- •Ингибиторы ферментов
- •Иммунная система
- •Стволовые клетки
- •Тканевая инженерия
- •Интерфероны
- •Интерлейкины
- •Эритропоэтин и другие факторы роста
- •Другие белки, имеющие медицинское значение
- •Вакцины
- •Рекомбинантные вакцины
- •Антитела
- •Моноклональные антитела
- •Рекомбинантные и каталитические антитела
- •Методы иммуноанализа
- •Биосенсоры
- •Биотехнология в сельском хозяйстве
- •Животноводство
- •Перенос эмбрионов и клонирование животных
- •Картирование генов
- •Трансгенные животные
- •Генетическая ферма и ксенотрансплантация
- •Растениеводство
- •Культивирование растительных клеток: поверхностные культуры
- •Культивирование растительных клеток: суспензионные культуры
- •Трансгенные растения: методы получения
- •Трансгенные растения
- •Вирусы
- •Бактериофаги
- •Микроорганизмы
- •Бактерии
- •Некоторые бактерии, важные для биотехнологии
- •Грибы
- •Дрожжи
- •Усовершенствование штаммов микроорганизмов
- •Основы биотехнологических методов
- •Микроорганизмы: рост в искусственных условиях
- •Кинетика образования продуктов метаболизма и биомассы в культуре микроорганизмов
- •Технология ферментации
- •Промышленные процессы ферментации
- •Культивирование животных клеток
- •Биореакторы для культивирования животных клеток
- •Биореакторы с иммобилизованными ферментами и клетками
- •Очистка биотехнологических продуктов
- •Очистка биотехнологических продуктов: хроматографические методы
- •Экономические аспекты биотехнологического производства
- •Методы генетической инженерии
- •Структура ДНК
- •Функции ДНК
- •Эксперимент в генетической инженерии
- •Методы выделения ДНК
- •Ферменты, модифицирующие ДНК
- •ПЦР: лабораторная практика
- •ДНК: химический синтез и определение размера молекул
- •Секвенирование ДНК
- •Введение ДНК в живые клетки (трансформация)
- •Идентификация и клонирование генов
- •Экспрессия генов
- •Выключение генов
- •Геном прокариот
- •Геном эукариот
- •Геном человека
- •Функциональный анализ генома человека
- •ДНК-анализ
- •Белковые и ДНК-чипы
- •Маркерные группы
- •Тенденции развития
- •Генная терапия
- •Поиск биологически активных веществ
- •Протеомика
- •Обмен веществ
- •Метаболомика и метаболическая инженерия
- •Системная биология
- •«Белая» биотехнология
- •Сертификация биотехнологической продукции
- •Этические аспекты генетической инженерии
- •Патентование в биотехнологии
- •Биотехнология в разных странах
- •Биотехнология в разных странах
- •Литература
- •Источники иллюстраций
- •Указатель микроорганизмов
Биотехнология в медицине
128
Факторы свертывания крови
ВВЕДЕНИЕ. Для предотвращения кровопотери при повреждении сосудов существует эффективный механизм, заключающийся в образовании тромба. Этот процесс, называемый гемостазом, представлен сложным набором реакций, проходящим в несколько этапов: активация зимогенов (предшественников протеиназ), протеолиз и ингибирование протеолиза. Cложная система регуляции свертывания крови предотвращает образование тромбов в неповрежденных сосудах. При свертывании крови растворимый белок фибриноген превращается в нерастворимый полимер фибрин путем протеолиза, катализируемого сериновой протеиназой тромбином. В таком «мягком» тромбе фактор XIIIа (фермент трансглутаминаза) обеспечивает формирование амидных связей, что приводит к формированию нерастворимого сгустка. В свою очередь тромбин образуется из протромбина под действием фактора Xа, а в регуляции этого процесса принимают участие белки фактора VIII. Мутации в генах белков фактора VIII являются причиной наиболее распространенных генетических заболеваний крови – гемофилии А и В.
ГЕМОФИЛИЯ. Первые упоминания об этой болезни встречаются на глиняных дощечках, дошедших до нас из Древнего Египта. Существует три клинических типа заболевания: гемофилия А, гемофилия В и болезнь фон Виллебранда. Гемофилия А встречается только у мужчин с частотой 1 на 5000. Причина патологии заключается в нарушении биосинтеза фактора VIII. У больных гемофилией А содержание фактора VIII в крови составляет менее 1% нормы, по этой причине спонтанное кровотечение, как правило, приводит к смерти. В генах фактора VIII, расположенных на Х-хромосоме, у больных гемофилией А обнаруживается инверсия интрона F8A, которая и приводит к нарушению биосинтеза белка в клетках печени. Фактор VIII – это гликопротеин (МR 300), представляющий собой одну полипептидную цепь из 2332 аминокислотных остатков. Она содержит 25 участков гликозилирования, и содержание сахара может достигать 35%. Его пространственная структура установлена с помощью электронной криомикроскопии. Ген фактора VIIIa имеет размер ~186 т.п.н. и содержит 26 экзонов. Посттрансляционное гликозилирование особенно важно в В-домене белка, который под действием тромбина отщепляется, что и приводит к активации фактора VIII. Болезнь фон Виллебранда, встречающаяся с частотой 1 на 1000 среди мужчин и женщин, вызвана нарушениями биосинтеза фактора фон Виллебранда (vWF) на внутренней стенке кровеносных сосудов. Ген vWF находится в хромосоме 12. Фактор фон Виллебранда, как и фактор VIII, – гликопротеин большого размера со сложной структурной органи-
зацией. Около 100 молекул vWF связываются с молекулой фактора VIII, и образующийся комплекс vWF–VIII активирует систему факторов X/IXа, которая обеспечивает агрегацию тромбоцитов при образовании тромба. При гемофилии В, встречающейся только у мужчин с частотой 1 на 25 000, нарушен синтез фактора IX – гликопротеина с молекулярной массой 55 кДа. Наряду с фактором VIII фактор IX участвует в активации фактора X. Ген, кодирующий фактор IX, расположен на X-хромосоме (Xq27) и имеет размер ~34 т.п.н.
КЛОНИРОВАНИЕ. При клонировании факторов крови, впервые осуществленного в 1982 г. компаниями Genentech и Genetic Institutes, оказалось, что главное затруднение связано с очень низким содержанием мРНК (лишь 10–5 от всей мРНК в печени). Полную кДНК удалось выделить из клеток лимфомы методом «прогулки по геному», а затем была создана векторная система, включающая в себя элементы вируса SV40 и аденовируса. Такая система позволила экспрессировать факторы крови в CHO- и BHKклетках.
ПРОИЗВОДСТВО. Производство лекарственных препаратов, содержащих факторы крови, началось в 1964 г. Факторы VIII, IX и vWF получали криопреципитацией из крови доноров, а затем очищали методами иммунохроматографии. Однако при этом значительно возрастала степень риска заражения реципиента через кровь донора, так как, например, для обеспечения одного больного гемофилией А фактором VIII в течение года требовалась кровь нескольких тысяч доноров. В результате более 60% пациентов, которые использовали донорские факторы крови, приобрели инфекционные заболевания. По этой причине генно-инженерный метод получения факторов VIII
иIX, разработанный в 1992 г., имеет огромное значение. Из-за высокого уровня гликозилирования фактора VIII синтез его биологически активной формы возможен исключительно в животных клетках (CHO-
иBHK-клетках), где уровень экспрессии чрезвычайно низок и составляет микрограммы продукта на литр клеточной культуры. Объем его рынка составляет около 500 млн долл. США в год (2004 г.).
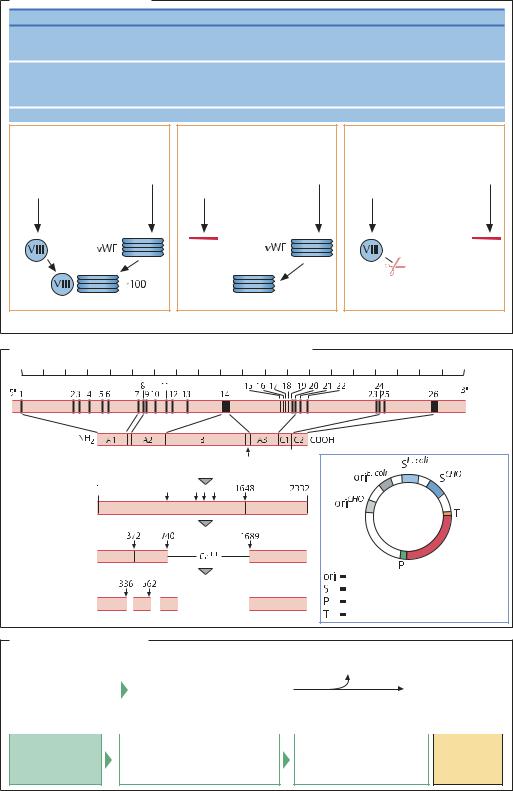
Тяжелые болезни крови |
|
|
|
|
|
|
||
|
|
Гемофилия А |
Болезнь фон Виллебранда |
Гемофилия В |
||||
Наследуемость |
|
1:5000, только мужчины |
1:1000, мужчины и женщины, |
1:25000, преиму- |
||||
|
|
|
|
как правило аутосомно- |
|
щественно мужчины |
||
|
|
|
|
доминантный тип наследования |
|
|
||
Клинические |
|
Мышечные и суставные |
Кровотечения из носа, значи- |
В детстве спонтанные |
||||
проявления |
|
кровотечения, крово- |
тельные потери крови в менстру- |
кровоизлияния |
||||
|
|
излияния в мозг |
альном цикле, продолжительные |
в суставы |
||||
|
|
|
|
кровотечения при порезах |
|
|
||
Хромосомный локус |
Xq28 |
|
12р12 |
|
Xq27 |
|||
Нормальный синтез |
Дефектный синтез |
Дефектный синтез при болезни |
||||||
комплекса фактора VIII |
при гемофилии А |
фон Виллебранда |
||||||
|
Хромосома 12: |
|
|
Хромосома 12: |
|
|
Хромосома 12: |
|
X-хромосома: |
|
ген фактора |
X-хромосома: |
ген фактора |
X-хромосома: |
ген фактора |
||
ген |
фон Виллебранда |
ген |
|
фон Виллебранда |
ген |
|
фон Виллебранда |
|
фактора VIII |
Внутренняя |
фактора VIII |
|
Внутренняя |
фактора VIII |
Внутренняя |
||
Клетки |
|
стенка |
Клетки |
|
стенка |
Клетки |
стенка |
|
кровеносного |
|
кровеносного |
кровеносного |
|||||
печени |
|
сосуда |
печени |
сосуда |
печени |
сосуда |
||
|
|
|
Блокирован |
|
|
|
|
Блокирован |
|
|
|
|
|
|
|
|
Быстрая |
|
|
|
|
|
|
|
|
деградация |
|
|
|
|
|
|
|
|
в отсутствие vWF |
Полноценный фактор VIII |
Только vWF |
|
|
|
||||
Комплекс фактора VIII состоит из фактора VIII и фактора фон Виллебранда (vWF) |
|
|
||||||
Фактор VIII: структура гена и экспрессирующий вектор |
|
|
|
|||||
0 |
|
50 |
100 |
|
150 |
|
200 т.п.н. |
|
|
|
|
|
|
|
|
|
Ген |
|
|
|
|
|
|
|
|
содер- |
|
|
|
|
|
|
|
|
жит 26 |
|
|
|
|
|
|
|
|
экзонов |
Одноцепо- |
|
|
|
|
|
|
|
|
чечный |
|
|
|
|
|
|
|
|
фактор VIII |
|
Связывание с фактором |
Связывание |
|
|
|
||
|
|
с фосфоли- |
|
|
|
|||
|
|
|
фон Виллебранда |
|
|
|
||
|
|
|
пидами |
|
|
|
||
|
|
|
|
|
|
|
|
|
Белок плазмы |
|
110–200 кДа |
|
80 кДа |
|
|
|
|
|
|
|
Тромбин |
|
|
|
|
|
Активация |
|
50 кДа 43 кДа |
|
|
73 кДа |
|
|
|
|
|
|
Активация белка С |
|
Точка начала репликации |
|||
|
|
|
|
Селективный маркер |
||||
|
|
|
|
|
|
|||
Инактивация |
45 кДа |
|
|
73 кДа |
Промотор (из генома аденовируса) |
|||
|
|
|
|
|
|
Терминатор |
|
|
Получение фактора VIII |
|
|
|
|
|
|
||
Из крови доноров |
|
|
Фактор фон Виллебранда |
|
|
|
|
||||
500 доноров |
|
|
|
Очистка |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
100 л плазмы, |
|
|
|
Осажение, многоступенчатая |
|
|
1 мг фактора VIII |
||||
1 кг криопреципитата |
|
|
|
иммунохроматография |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рекомбинантный фактор VIII |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Биореактор с культурой клеток |
|
Очистка |
|
|
Около 2 мг |
||
Рекомбинантные |
|
|
|
|
|
|
|
фактора VIII |
|||
200 ч, 35 °С, |
|
Осажение, многоступенчатая |
|||||||||
клетки CHO |
|
|
|
из 1 л клеточ- |
|||||||
|
|
|
|
сложная питательная среда |
|
иммунохроматография |
|
|
ной культуры |
||
129
медицине |
Антикоагулянты и тромболитики |
|
ВВЕДЕНИЕ. Образование тромбов (инфаркт миокар- |
||
да, инсульт, закупорка сосудов) является самой |
||
в |
распространенной причиной смерти в большинстве |
|
Биотехнология |
||
развитых стран. В Германии от тромбозов ежегодно |
||
|
||
|
умирают 60 000 человек. Антикоагулянты препятст- |
|
|
вуют образованию первичных тромбов (в том числе |
|
|
при операциях), а тромболитики осуществляют про- |
|
|
теолитическое разрушение тромбов. В медицине |
|
|
находят применение такие антикоагулянты, как |
|
|
гепарин и производное кумарина, а также рекомби- |
|
|
нантные ингибиторы тромбина – гирудин (природ- |
|
|
ный источник – медицинские пиявки) и антитром- |
|
|
бин III человека (АТ-III). В качестве тромболитиков |
|
|
используют бактериальную стрептокиназу, а также |
|
|
препараты урокиназы и тканевого активатора плаз- |
|
|
миногена (tPA и rPA), полученные методами гене- |
|
|
тической инженерии. |
|
|
ГЕПАРИН – серосодержащий глюкозоаминогликан |
|
|
(мукополисахарид) с MR от 3 до 60 кДа. Его экстра- |
|
|
гируют из кишечника свиней или легких крупного ро- |
|
|
гатого скота. Гепарин синтезируется тучными клетка- |
|
|
ми и, оказавшись в плазме крови, активирует АТ-III, |
|
|
который в свою очередь связывается с тромбином и |
|
|
препятствует образованию фибрина. |
|
|
ГИРУДИН – ингибитор тромбина, обнаруженный в |
|
|
секрете слюнных желез медицинской пиявки. В на- |
|
|
стоящее время рекомбинантный гирудин получают |
|
|
ферментацией в клетках Escherichia coli и в других |
|
|
организмах-хозяевах. Действие гирудина аналогично |
|
|
действию АТ-III: он связывается с тромбином, тем са- |
|
|
мым препятствуя образованию фибрина из фибрино- |
|
|
гена. |
|
|
ТКАНЕВОЙ АКТИВАТОР ПЛАЗМИНОГЕНА (tissue plas- |
|
|
minogen activator, tPA). Расщепление фибрина при |
|
|
заживлении раны осуществляется сериновой протеи- |
|
|
назой плазмином. Активная форма плазмина образу- |
|
|
ется из плазминогена под действием тканевого акти- |
|
|
ватора плазминогена (tPA, MR 72). Это еще одна |
|
|
сериновая протеиназа, которая специфически расще- |
|
|
пляет пептидную связь между остатками аргинина и |
|
|
валина (в положениях 561 и 562) в молекуле плаз- |
|
|
миногена. Белок построен из пяти доменов, функции |
|
|
которых установлены на основании гомологии с дру- |
|
|
гими изученными белками. Функция двух доменов, |
|
|
имеющих форму торов, заключается в связывании с |
|
|
молекулой фибрина, а так называемый протеазный |
|
|
домен содержит активный центр фермента. Ген tPA |
|
|
человека был клонирован в 1982 г., а с 1988 г. пре- |
|
|
параты этого белка поступили на рынок. Наличие |
|
|
в зрелом tPA восьми дисульфидных связей и трех |
|
|
крупных углеводных компонентов, составляющих |
|
|
~25% массы и необходимых для связывания с суб- |
|
130 |
стратом, не позволяет использовать бактериальные |
|
клетки в качестве клеток-хозяев. Для получения |
рекомбинантного tPA выбирают клетки мышей или клеточные линии СНО, а образующийся белок очищают различными способами, включающими осаждение в кислой среде, а также ионообменную, гидрофобную и аффинную хроматографию. Мутанты производят фермент с искусственно измененным сайтом гликозирирования и четырьмя аминокислотными заменами (TNK-tPATM), который прочно связывается с фибрином и имеет более продолжительное время полураспада в сыворотке. В этой связи вместо использования инфузии можно провести однократное введение. Мутанты E. coli с нарушенной функцией гликозилирования синтезируют фермент, лишенный петлевого-1 и eGF-доменов (RepilysinTM), однако его выделение из телец включения оказывается затруднительным. По сравнению с tPA время пребывания этого белка в сыворотке в 3–4 раза больше, а аллергенные свойства выражены слабее. tPA также секретируется с молоком трансгенных коз и овец, которые трансформированы вектором, содержащим фрагмент tPA-кДНК под промотором лактальбумина. Белок tPA, кроме того, получают из молока трансгенных коз и овец, в которых ген tPA клонирован за промотором лактальбумина. Для контроля однородности полученного таким способом tPA требуется применение специальных аналитических методов.
ДРУГИЕ ТРОМБОЛИТИКИ. Урокиназа – сериновая протеиназа; в виде проурокиназы присутствует в сыворотке крови и в моче. Подобно tPA, урокиназа гидролизует плазминоген с образованием плазмина. Обнаружены две формы белка с MR 54 и 30: белок меньшего размера образуется из большего при автолизе, и обе формы обладают биологической активностью. Урокиназу выделяют из мочи, культуры клеток почек человека или в виде рекомбинантного продукта из клеток E. coli. Стрептокиназа образуется в различных гемолитических стрептококках. Этот белок не обладает каталитической активностью, однако вызывает конформационные изменения в молекуле плазминогена, что приводит к автолизу с образованием плазмина. Стрептокиназу получают из культур стрептококков методами хроматографии. Применение других, более дешевых способов очистки белка, связано с риском возникновения сильных иммунных реакций.
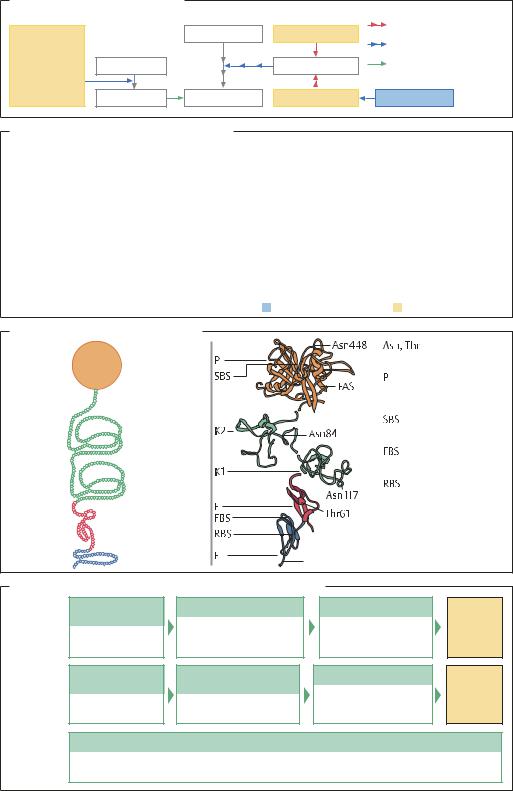
Упрощенная схема тромболиза |
|
|
||
|
Тромболиз |
Свертывание крови |
|
Ингибирование |
|
|
Фибриноген |
Гирудин |
|
Тканевой |
|
Активация |
||
|
|
|
||
активатор |
|
|
Тромбин |
Протеолитическое |
плазминогена, |
Плазминоген |
|
||
урокиназа, |
|
|
|
расщепление |
стрептокиназа |
Плазмин |
Фибрин |
Антитромбин-III |
Гепарин |
|
||||
Антикоагулянты (А) и тромболитики (Т) |
|
|
||
|
Тип |
Действие |
Производитель |
Гепарин |
А |
Серосодержащий полисахарид, связывается |
Celsus |
|
|
с антитромбином III и инактивирует тромбин |
|
Гирудин |
А |
Ингибирует тромбин |
Novartis, Behringwerke* |
Антитромбин-III |
А |
Ингибирует тромбин |
Genzyme Transgenic Corp. |
Стрептокиназа |
Т |
Активирует плазминоген |
Kabi Upjoin* |
Урокиназа |
Т |
Активирует плазминоген |
Grüenenthal* |
Тканевой активатор |
T |
Активирует плазминоген |
Genentech*, Boehring, |
плазминогена |
|
|
Ingelheim*, Roche* |
|
|
|
|
* Препарат разрешен к применению |
Природное соединение |
Рекомбинантный белок |
||||
Тканевой активатор плазминогена |
|
|
|
|||
|
Ретеплаза – |
|
|
Участки |
||
|
|
|
гликозилирования |
|||
Протеазный |
мутантный белок, |
|
||||
|
|
|
||||
домен |
не содержащий |
|
Домен с протео- |
|||
|
домена |
|
|
|||
|
|
|
литической |
|||
|
фактора роста |
|
||||
|
|
активностью |
||||
|
и «тора 1», |
|
|
|||
|
|
|
|
|
||
|
может |
|
|
Участок связыва- |
||
|
существовать |
|
||||
«Тор 2» |
|
ния субстрата |
||||
в крови в 3 раза |
|
|||||
|
дольше, чем |
|
|
Участок связыва- |
||
|
нативный белок |
|
||||
|
|
ния с фибрином |
||||
|
|
|
|
|||
«Тор 1» |
|
|
|
Участок связыва- |
||
|
|
|
|
|||
|
|
|
|
ния с рецептором |
||
Фактор роста |
|
|
|
|
|
|
(домен Е) |
|
|
|
|
|
|
«Палец» |
|
|
N-Конец |
|
|
|
(домен F) |
|
|
|
|
||
Получение тканевого активатора плазминогена (пример) |
|
|
||||
|
Рекомбинантные |
Клеточный реактор |
Выделение и очистка |
Выход |
||
Клеточный |
клетки СНО |
|
|
|
||
Реактор объемом до 20 м3, |
Многостадийная |
|
продукта |
|||
реактор |
|
|
||||
Вектор |
сложная питательная |
иммунохроматография |
несколько |
|||
|
||||||
|
СНО-NEOSPLA |
среда, 37°С, 20 сут. |
|
|
мг/л в сут. |
|
|
Трансгенное |
Характеристика |
Выделение и очистка |
Выход |
||
Трансгенные |
животное |
животного |
|
|
||
Осаждение в кислых |
продукта |
|||||
козы |
|
|
||||
Вектор LSAP + PA |
|
до 30 г/л |
||||
|
Период лактации 240 дней, |
условиях, бутилсефароза, |
||||
|
|
3–4 л молока в день |
иммунохроматография |
молока |
||
|
|
|
||||
|
|
Контроль качества |
|
|
||
|
Обращенно-фазовая ВЭЖХ, электрофорез в денатурирующих условиях, ELISA, |
|
||||
|
пептидное картирование, определение степени гликозилирования и другие методы |
|
||||
|
|
|
|
|
131 |
|
