
- •1Врач-анестезиолог, отделение общей анестезиологии, Кливлендский клинический фонд, Кливленд, Огайо, сша.
- •Классификация нервных волокон
- •Электромиография и исследование нервно-мышечной проводимости
- •1Вместо лидокаина можно использовать хлоропрокаин.
- •1В состав гидрокодонсодержащих препаратов входит также и ацетаминофен (викодин, др.).
- •1В состав оксикодонсодержащих препаратов может входить ацетаминофен (перкоцет) или аспирин (перкодан).
- •1В состав некоторых пропоксифенсодержащих препаратов входит ацетаминофен (дарвоцет).
- •1В большинстве случаев авторы не рекомендуют проведение постоянной поддерживающей инфузии.
- •Раздел IV
- •1. Частота сердечных сокращений
- •2. Ударный объем
- •1. Функциональные кривые желудочка
- •2. Оценка систолической функции
- •Фракция выброса
- •3. Оценка диастол ической функции
- •Эндотелиальные факторы
- •Анатомия и физиология коронарного кровообращения
- •1. Анатомия
- •2. Факторы, определяющие величину коронарного кровотока
- •3. Кислородный баланс в миокарде
- •Потребность миокарда в кислороде
- •I. Наджелудочковые аритмии
- •II. Желудочковые аритмии
- •2. Выбор анестетиков и вспомогательных средств:
- •1. Общие принципы
- •2. Премедикация
- •1. Митральный стеноз
- •2. Митральная недостаточность
- •3. Пролапс митрального клапана
- •4. Аортальный стеноз
- •5. Гипертрофическая кардиомиопатия
- •6. Аортальная недостаточность
- •7. Трикуспидальная недостаточность
- •Гипоплазия левых отделов сердца
- •1. Обструктивные поражения
- •2. Простые шунты
- •3. Сложные шунты
- •Внесердечные заболевания
- •Гипогликемия
- •1Частота импульсов автоматически изменяется в зависимости от потребности в сердечном выбросе.— Примеч. Пер.
- •1. Преиндукционный период
- •2. Индукция анестезии
- •3. Предперфузионный период
- •4. Перфузионный период
- •5. Завершение ик
- •6. Постперфузионный период
- •7. Послеоперационный период
- •Анестезия при трансплантации сердца
- •1. Тампонада сердца
- •2. Констриктивныи перикардит
- •Расслаивание аорты
- •1. Аэробный метаболизм
- •2. Анаэробный метаболизм
- •3. Влияние анестезии на клеточный метаболизм
- •1. Грудная клетка и дыхательная мускулатура
- •2. Трахеобронхиальное дерево
- •3. Кровообращение и лимфоток в легких
- •4. Иннервация
- •1.Эластическое сопротивление
- •2. Легочные объемы
- •3. Неэластическое сопротивление
- •4. Работа дыхания
- •5. Влияние анестезии на механику дыхания
- •1. Вентиляция
- •2. Легочный кровоток
- •3. Шунты
- •4. Влияние анестезии на газообмен
- •Напряжение газов в альвеолах, артериальной и венозной крови
- •1.Кислород
- •Высокий альвеолярно-артериальный градиент по кислороду
- •2. Углекислый газ
- •1.Кислород
- •2. Углекислый газ
- •1. Дыхательные центры
- •2. Центральные рецепторы
- •3. Периферические рецепторы
- •4. Влияние анестезии на регуляцию дыхания
- •Состояния, при которых необходима раздельная вентиляция легких
- •Тяжелая гипоксемия при заболевании одного легкого
- •1. Опухоли
- •2. Легочные инфекции
- •3. Бронхоэктазы
- •1. Предоперационный период
- •2. Интраоперационный период
- •3. Послеоперационный период
- •Анестезия при торакоскопических операциях
- •Легочный лимфангиоматоз
- •1. Предоперационный период
- •2. Интраоперационный период
- •3. Послеоперационный период
- •1. Церебральное перфузионное давление
- •2. Ауторегуляция мозгового кровообращения
- •3. Внешние факторы
- •Внутричерепное давление
- •Влияние анестетиков и вспомогательных средств на цнс
- •1. Испаряемые анестетики
- •Мк и внутричерепной объем крови
- •2. Закись азота
- •1.Для индукции анестезии
- •2. Вспомогательные средства
- •3. Вазопрессоры
- •4. Вазодилататоры
- •5. Миорелаксанты
- •Патологическое пристрастие к алкоголю и наркотическим препаратам
- •Как проводят эст?
- •Неосмотическая секреция адг
- •Гиперосмоляльность и гипернатриемия
- •Гипернатриемия при низком содержании натрия в организме
- •Гипоосмоляльность и гипонатриемия
- •Гипонатриемия с повышенной осмоляльностью плазмы
- •Застойная сердечная недостаточность
- •Внепочечные потери
- •Тяжелая физическая нагрузка
- •Изолированное снижение секреции калия в дистальном отделе нефрона
- •Повышенное поступление калия
- •Гиперкальциемия
- •Клинические проявления гиперкальциемии
- •1.Гемолитические реакции
- •2. Негемолитические иммунные реакции
- •Нитропруссид
- •Кислоты и основания
- •Сопряженные пары и буферы
- •Клинические нарушения
- •Компенсаторные механизмы
- •Нервно-мышечные нарушения
- •Травмы и заболевания грудной клетки
- •Болезни плевры
- •Обструкция дыхательных путей
- •Наследственные нарушения обмена веществ
- •Центральная стимуляция дыхания
- •Хлоридчувствительный метаболический алкалоз
- •1. Антагонисты альдостерона
- •2. Неконкурентные калийсберегающие диуретики
- •Сердечно-сосудистая система
- •Предоперационное обследование
- •Миорелаксанты
- •Предоперационный период
Тяжелая физическая нагрузка
бета2-Адреноблокаторы
Периодический гиперкалиемический паралич
Сукцинилхолин
Передозировка дигоксина
Аргинин HCl
Снижение почечной экскреции калия
Почечная недостаточность
Уменьшение минералокортикоидной активности
Первичная надпочечниковая недостаточность
Болезнь Аддисона
Двустороннее удаление надпочечников
Врожденная гиперплазия надпочечников
Дефицит 21-гидроксилазы
Гипоренинемический гипоальдостеронизм
Синдром приобретенного иммунодефицита
Побочные эффекты лекарственных препаратов
Конкурентные калийсберегающие диуретики
Спиронолактон
Ингибиторы АПФ
Циклоспорин
Нестероидные противовоспалительные средства
Гепарин
Изолированное снижение секреции калия в дистальном отделе нефрона
Псевдогипоальдостеронизм
Неконкурентные калийсберегающие диуретики
Амилорид
Триамтерен
Серповидно-клеточная анемия
Пересаженная почка
Системная красная волчанка
Обструкция мочевыводящих путей
Повышенное поступление калия
Трансфузия цельной крови с длительным сроком хранения
Заменители поваренной соли
Калиевая соль пенициллина
Гиперкалиемия вследствие снижения почечной экскреции калия
Снижение почечной экскреции калия возникает в следующих случаях:
(1) выраженное уменьшение скорости клубочковой фильтрации;
(2) снижение активности альдостерона или
(3) нарушение секреции калия в дистальных отделах нефрона.
При скорости клубочковой фильтрации менее 5 мл/мин почти всегда возникает гиперкалиемия. На фоне высокой калиевой нагрузки (алиментар-ного, метаболического или ятрогенного характера) гиперкалиемия может развиться и при менее выраженном нарушении почечной функции. Помимо того, уремия снижает активность Na+/K+-3a-висимой АТФ-азы.
Снижение активности альдостерона наблюдается при первичном нарушении синтеза гормона в надпочечниках или дефекте в системе ренин-ангиотензин-альдостерон При первичной надпочечниковой недостаточности (болезнь Аддисона) и дефиците 21-гидроксилазы нарушается синтез альдостерона. Синдром изолированного гипоальдостеронизма (синонимы: гипорениновый альдостеронизм или почечный канальцевый ацидоз IV типа) обычно сочетается с сахарным диабетом и почечной дисфункцией; у таких больных нарушена способность к повышению секреции альдостерона в ответ на гиперкалиемию. Заболевание обычно протекает бессимптомно, но при увеличении поступления калия и применении калийсберегающих диуретиков развивается гиперкалиемия. Кроме того, для гипоренинемического гипоальдостеронизма характерны потери натрия и гиперхлоремический метаболический ацидоз. Подобная картина была описана у некоторых больных СПИД, имеющих сопутствующую надпочечниковую недостаточность (вследствие цитомегаловирусной инфекции).
Применение препаратов, воздействующих на систему ренин-ангиотензин-альдостерон, влечет за собой риск развития гиперкалиемии, особенно при почечной недостаточности. Нестероидные противовоспалительные средства (кроме, возможно, сулиндака) угнетают опосредуемое простагландинами высвобождение ренина. Ингибиторы АПФ препятствуют образованию ангиотензина II, который стимулирует секрецию альдостерона. Большие дозы гепарина тоже способны нарушать секрецию альдостерона. Калийсберегающий диуретик спиронолактон является конкурентным антагонистом альдостероновых рецепторов в почках. Механизм возникновения гипоренинемического гипоальдостеронизма под действием циклоспорина не ясен.
Выведение калия через почки может снижаться из-за врожденного или приобретенного нарушения его секреции в дистальном отделе нефрона. Подобные нарушения возникают даже при нормальной функции почек, они не поддаются лечению минералокортикоидами. При псевдогипоальдостеронизме отмечается врожденная резистентность почек к альдостерону. Заболевания, при которых нарушается секреция калия, включают системную красную волчанку, серповидно-клеточную анемию, обструкцию мочевыводящих путей, а также циклоспориновую нефропатию пересаженной почки.
Гиперкалиемия вследствие повышенного поступления калия в организм
В норме увеличение поступления калия в организм редко сопровождается гиперкалиемией — за исключением тех случаев, когда в/в быстро вводят большое его количество. Вместе с тем калиевая нагрузка может вызвать гиперкалиемию при почечной недостаточности, при дефиците инсулина, а также у больных, получающих бета2-адреноблокаторы. Часто остаются незамеченными такие источники поступления калия, как калиевая соль пенициллина, заменители поваренной соли (как правило, это соли калия), перелитая цельная кровь с длительным сроком хранения. К 21-му дню хранения концентрация калия в плазме цельной крови может достигнуть 30 мэкв/л.
Клинические проявления гиперкалиемии
Наиболее значимо влияние гиперкалиемии на скелетные мышцы и миокард. Генерализованная мышечная слабость возникает при концентрации калия в плазме > 8 мэкв/л. Ее причиной является стойкая спонтанная деполяризация и инактивация натриевых каналов мембраны мышечных клеток (как при применении сукцинилхолина), что в конце концов приводит к восходящему параличу.
При концентрации калия в плазме > 7 мэкв/л замедление деполяризации в миокарде становится клинически значимым (рис. 28-6). По мере возрастания концентрации калия в плазме динамика изменений на ЭКГ выглядит следующим образом: высокий заостренный зубец Т (часто сочетается с укороченным интервалом QT) расширение комплекса QRS удлинение интервала PQ исчезновение зубца Р снижение амплитуды зубца R депрессия сегмента ST (иногда подъем) комплексы ЭКГ синусоидальной формы фибрилляция желудочков и асистолия. Гиперкалиемия незначительно влияет на сократимость миокарда. Гиперкалъциемия, гипонатриемия и ацидоз усиливают действие гиперкалиемии на сердце.
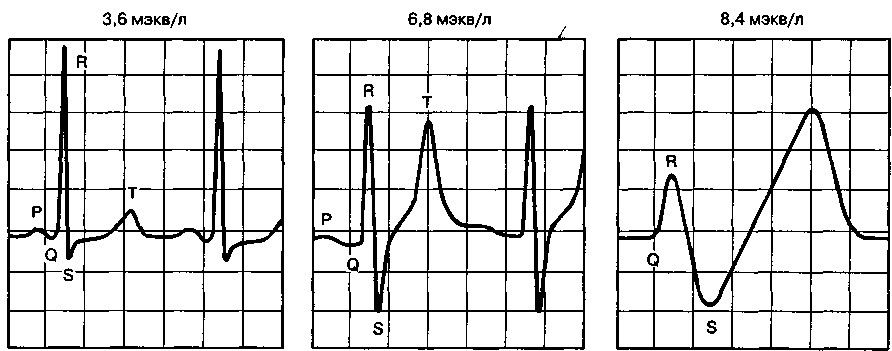
Рис. 28-6. Электрокардиографические признаки гиперкалиемии. По мере возрастания концентрации калия в плазме динамика электрокардиографических изменений выглядит следующим образом: высокий остроконечный симметричный зубец Т, часто в сочетании с укороченным интервалом QT расширение комплекса QRS, удлинение интервала PQ, исчезновение зубца Р, снижение амплитуды зубца R, депрессия (иногда подъем) сегмента ST комплексы синусоидальной формы наконец, фибрилляция желудочков или асистолия
Лечение гиперкалиемии
Гиперкалиемия > 6 мэкв/л является показанием к лечению ввиду высокого риска смертельного исхода. Устраняют кардиотоксические проявления, мышечную слабость и нормализуют концентрацию калия в плазме. Методы лечения зависят от тяжести клинических проявлений и причин гиперкалиемии. При гиперкалиемии, сопряженной с гипоальдостеронизмом, назначают заместительную терапию минералокортикоидами. Необходимо отменить прием препаратов, способствующих гиперкалиемии, а также уменьшить или прекратить поступление калия в организм.
Кальций (5-10 мл 10 % раствора глюконата кальция или 3-5 мл 10 % раствора хлористого кальция) частично устраняет кардиотоксические эффекты гиперкалиемии и поэтому используется при выраженной клинической симптоматике. Действие кальция наступает быстро, но, к сожалению, носит преходящий характер. У больных, принимающих дигоксин, кальций рекомендуется применять с осторожностью, поскольку он способствует возникновению гликозидной интоксикации.
При метаболическом ацидозе инфузия бикарбоната натрия (обычно 45 мэкв) способствует поступлению калия в клетки и в течение 15 мин может снизить его концентрацию в плазме. (З^-Адреномиметики способствуют перемещению калия в клетки и применяются при острой гиперкалиемии, сопряженной с массивными гемотрансфузиями (гл. 29); адреналин в низких дозах (0,5-2 мкг/мин) позволяет быстро снизить концентрацию калия в плазме и, кроме того, оказывает положительное инотропное действие. Инфузия глюкозо-инсулиновой смеси (30-50 г глюкозы и 10 ЕД инсулина) способствует перемещению калия в клетки, но максимальный эффект развивается не сразу, а в течение 1 ч.
При относительно сохранной функции почек показан фуросемид, который повышает экскрецию калия с мочой. При тяжелой дисфункции почек вывести калий из организма удается только с помощью ионообменных смол (например, полистиролсульфонат натрия внутрь или в клизме): 1 г полистирол-сульфоната натрия связывает 1 мэкв К+ и высвобождает 1,5 мэкв Na+; доза при приеме внутрь составляет 20 г в100 мл 20% раствора сорбитола.
Диализ показан при выраженной или рефрактерной гиперкалиемии. Гемодиализ значительно быстрее и эффективнее, чем перитонеальный, снижает концентрацию калия в плазме. Гемодиализ позволяет удалить до 50 мэкв калия в 1 ч, перитонеальный диализ — 10-15 мэкв/ч.
Анестезия
При гиперкалиемии плановые операции откладывают, пока концентрация калия в крови не будет снижена до нормы. Необходимо также не допустить ее повторного повышения. Проводят тщательный ЭКГ-мониторинг. Противопоказано введение сукцинилхолина и любых калийсодержащих инфузионных растворов (например, раствора Рингера с лактатом). Во избежание повторного повышения концентрации калия в плазме во время операции необходимо предупреждать возникновение метаболического и дыхательного ацидоза. ИВЛ целесообразно проводить в режиме умеренной гипервентиляции. И, наконец, необходим мониторинг нервно-мышечной проводимости, поскольку гиперкалиемия усиливает действие миорелаксантов.
Нарушения обмена кальция
Кальций содержится в основном в костях (98 %), но поддержание его нормальной внеклеточной концентрации чрезвычайно важно. Ионы кальция вовлечены практически во все физиологические процессы, включая мышечное сокращение, высвобождение нейромедиаторов и гормонов, свертывание крови и метаболизм костной ткани. Следовательно, нарушения обмена кальция способны привести к тяжелым расстройствам многих физиологических процессов.
Обмен кальция в норме
В норме суточное потребление кальция составляет 600-800 мг. Всасывание происходит главным образом в проксимальном отделе тонкой кишки. В кишечнике также осуществляется секреция кальция, скорость которой постоянна и не зависит от абсорбции. Обычно до 80 % потребляемого кальция выделяется с калом.
Экскреция кальция осуществляется через почки, составляя в среднем 100 мг/сут, и может варьироваться от 50 до > 300 мг/сут. В норме 98 % фильтруемого в почечных клубочках кальция реабсорбируется. Реабсорбция кальция (как и натрия) происходит в проксимальных канальцах и в восходящей части петли Генле. В дистальных канальцах реабсорбция кальция зависит от секреции паратиреоидного гормона (ПТГ), тогда как реабсорбция натрия — от секреции альдостерона. Повышение концентрации ПТГ в крови увеличивает реабсорбцию кальция в дистальных канальцах и снижает его экскрецию почками.
Концентрация кальция в плазме
В норме концентрация кальция в плазме составляет 8,5-10,5 мг/100 мл (2,1-2,6 ммоль/л). Приблизительно 50 % кальция плазмы находится в свободной ионизированной форме, 40 % связано с белками (в основном с альбумином) и 10 % — с анионами (с цитратом и аминокислотами). Физиологически активным является свободный ионизированный кальций, величина концентрации которого ([Са2+]) наиболее важна в клинической практике. В норме [Са2+] равна 4,5-5 мг/100 мл (2,2-2,5 мэкв/л, или 1,1-1,25 ммоль/л). Изменение концентрации альбумина в плазме влияет на общую концентрацию кальция, но не на концентрацию ионизированного кальция: при изменении концентрации альбумина в плазме на 1 г/100 мл общая концентрация кальция изменяется в том же направлении на 0,8-1 мг/100 мл.
Изменение рН непосредственно влияет на степень связывания кальция с белками и, таким образом, на концентрацию ионизированного кальция. Уменьшение рН плазмы на каждые 0,1 сопровождается увеличением концентрации ионизированного кальция на 0,16 мг/100 мл; соответственно, при повышении рН плазмы на каждые 0,1 концентрация ионизированного кальция уменьшается на 0,16 мг/100 мл.
Регуляция внеклеточной концентрации ионизированного кальция
Поступление кальция во внеклеточную жидкость происходит либо при всасывании из кишечника, либо в результате резорбции из костной ткани; не более 0,5-1 % кальция костей участвует в обмене с внеклеточной жидкостью. Кальций может покидать внеклеточное пространство за счет: 1) депонирования в костях; 2) экскреции с мочой; 3) секреции в ЖКТ и 4) экскреции с потом. Внеклеточная концентрация ионизированного кальция регулируется ПТГ, витамином D и кальцитонином. Эти гормоны оказывают действие на кости, дистальные почечные канальцы и тонкую кишку.
Главным регулятором концентрации Са2+ в плазме является ПТГ. Снижение концентрации Са2+ в плазме стимулирует секрецию ПТГ, а повышение — ингибирует. ПТГ оказывает следующие эффекты:
1) мобилизует кальций из костей;
2) стимулирует реабсорбцию кальция в дистальных почечных канальцах;
3) опосредованно увеличивает всасывание кальция в тонкой кишке путем ускорения синтеза 1,25-дигидроксихолекальциферола в почках.
В организме существует несколько форм витамина D, но максимальной биологической активностью обладает 1,25-дигидроксихолекальциферол. В ходе метаболизма холекальциферол (большей частью эндогенный) превращается в печени в 25-холекальциферол, который затем в почках преобразуется в 1,25-дигидроксихолекальциферол. Секреция ПТГ и гипофосфатемия усиливают второй этап (почечный) метаболического превращения. Витамин D стимулирует всасывание кальция в кишечнике, способствует действию ПТГ на кости и увеличивает реабсорбцию кальция в дистальных канальцах почек.
Кальцитонин — это полипептидный гормон, который вырабатывается парафолликулярными клетками щитовидной железы. Гиперкальциемия стимулирует секрецию кальцитонина, а гипокальциемия, наоборот, угнетает. Кальцитонин подавляет резорбцию костей и стимулирует почечную экскрецию кальция.
