
- •Передмова
- •Предмет та задачі аналітичної хімії
- •Глава 1. Деякі положення теорії електролітичної дисоціації
- •1.1. Електроліти, ступінь електролітичної дисоціації
- •1.2. Водневий показник водних розчинів електролітів (рН)
- •Практична робота складання рівнянь реакцій у молекулярній та іонній формах
- •Приклад
- •Завдання для самостійної роботи
- •Практична робота обчислення концентрації іонів гідрогену та гідроксид-іонів, рН та рОн у розчинах сильних електролітів
- •Приклади
- •Задачі для самостійної роботи
- •Глава 2. Кислотно-основна рівновага
- •2.1. Хімічна рівновага. Константа хімічної рівноваги
- •2.2. Рівновага в розчинах слабких електролітів
- •2.3. Рівновага в розчинах солей, що гідролізуються
- •2.4. Буферні системи
- •Практична робота рівновага в розчинах амфотерних електролітів
- •Завдання для самостійної роботи
- •Глава 3. Рівновага в гетерогенних системах
- •3.1. Добуток розчинності
- •3.2. Порядок дробного (вибіркового) осадження
- •3.3. Чинники, що впливають на осадження осадів та їх розчинність
- •Розв’язання
- •Завдання для самостійної роботи
- •Глава 4. Рівновага в окисно-відновних системах
- •4.1. Окисно-відновні системи
- •4.2. Окисно-відновний потенціал (редокс-потенціал)
- •4.3. Константа рівноваги редокс-реакції
- •Завдання для самостійної роботи
- •Глава 5. Рівновага комплексоутворення
- •5.1. Поняття про комплексні сполуки
- •Класифікація комплексних сполук
- •5.2.Рівноваги в розчинах комплексних сполук. Константи стійкості та нестійкості
- •5.3. Вплив різних чинників на процес комплексоутворення
- •5.4. Способи руйнування та утворення комплексів. Використання комплексних сполук в практиці аналізу
- •Розв'язання
- •Розв'язання
- •Задачі для самостійної роботи
- •Основні поняття
- •Дробний аналіз
- •Систематичний аналіз
- •IV. В залежності від способу виконання розрізняють реакції, що виконані:
- •Аналітичні ознаки реакцій
- •Правила роботи і техніка безпеки в хімічній лабораторії
- •Перша допомога при нещасних випадках
- •Якісний аналіз неорганічних сполук
- •Аналіз катіонів
- •Лабораторна робота
- •Загальна характеристика
- •Реакції Калій-катіона
- •1. Дія натрій гексанітрокобальтату(ііі) Na3[Co(nо2)6 ] (фармакопейна реакція)
- •2. Дія натрій гідрогентартрату NaHc4h4o6 (фармакопейна реакція)
- •3. Дія натрій тетрафенілборату Na[b(c6h5)4] (фармакопейна реакція)
- •4. Реакція забарвлення полум'я (реакція фармакопейна)
- •Реакції Натрій-катіона
- •1. Дія розчину метоксифенілацетатної кислоти c6h5ch(och3)cooh (фармакопейна реакція)
- •2. Дія калій гексагідроксостибату(V) k[Sb(oh)6] (фармакопейна реакція)
- •3. Дія цинктриураніл октаацетату Zn(uo2)3(ch3coo)8.
- •4. Реакція забарвлення полум’я (реакція фармакопейна)
- •Реакції амоній-катіона
- •1. Дія лугів (фармакопейна реакція)
- •3. Дія магній оксиду MgO (фармакопейна реакція)
- •Біологічна роль та практичне використання катіонів і аналітичної групи та їх сполук в медицині та фармації
- •Лабораторна робота
- •Загальна характеристика
- •1. Дія 2 м розчину хлоридної кислоти hCl (дія групового реагенту)
- •Плюмбум(іі) гідроксид має амфотерні властивості і розчиняється в надлишку реагенту:
- •3. Дія розчину калій йодиду кі
- •4. Дія розчину калій хромату k2CrO4
- •Реакція Аргентум(і)-катіона
- •Реакції Плюмбум(іі)-катіона
- •1. Дія розчину калій йодиду ki
- •Реакції димеркурій(і)-катіона
- •1. Дія розчину калій йодиду кі
- •Контрольні питання
- •Біологічна роль та практичне використання катіонів II аналітичної групи та їх сполук у медицині та фармації
- •Лабораторна робота
- •Загальна характеристика
- •Загальноаналітичні реакції катіонів III групи
- •1. Дія 1м розчину сульфатної кислоти h2so4 (дія групового реагенту)
- •2. Дія карбонатів
- •3. Дія хроматів
- •Реакції Барій-катіона
- •1. Дія дихромат-іону
- •2. Реакція забарвлення полум’я (фармакопейна реакція)
- •Реакції Кальцій-катіона
- •1. Дія розчину сульфатної кислоти h2so4
- •2. Дія розчину амоній оксалату (nh4)2c2o4 (фармакопейна реакція)
- •3. Дія розчину гліоксальгідроксіанілу (фармакопейна реакція)
- •4. Дія розчину калій гексаціаноферату(іі) k4[Fe(cn)6] (фармакопейна реакція)
- •5. Реакція забарвлення полум’я (фармакопейна реакція)
- •Реакції Стронцій-катіона
- •1. Реакція з гіпсовою водою
- •2. Реакція забарвлення полум'я
- •Контрольні запитання
- •Біологічна роль та практичне використання катіонів III аналітичної групи та їх сполук у медицині та фармації
- •Лабораторна робота реакції катіонів IV аналітичної групи
- •Загальна характеристика
- •Загальноаналітичні реакції катіонів IV аналітичної групи
- •1. Дія 6м розчину лугу (дія групового реагенту)
- •Реакція Станум(іі)-катіона
- •1. Дія надлишку лугу в присутності розчиненої солі бісмут(ііі) нітрату Ві(no3)3.
- •Реакція Хром(ііі)- катіона
- •1. Дія гідроген пероксиду h2o2 в присутності надлишку лугу
- •Реакції Цинк(іі)-катіона
- •1. Дія розчину калій гексаціаноферату(II) (фармакопейна реакція)
- •2. Дія сульфідів (фармакопейна реакція)
- •3. Дія дитизону
- •Реакції Алюміній(ііі)-катіона
- •1. Дія алізарину (1,2-діоксіанрахінону)
- •2. Дія розчину натрій ацетату
- •Реакції сполук Арсену
- •1. Дія розчину натрій дигідрогенфосфіту NaH2po2 (фармакопейна реакція)
- •2. Дія розчину натрій сульфіду Na2s (фармакопейна реакція)
- •3. Дія розчину магній сульфату MgSo4 (фармакопейна реакція)
- •Визначення домішок сполук Арсену(ііі) та Арсену(V) у лікарських засобах.
- •Контрольні питання
- •Біологічна роль та практичне використання катіонів IV аналітичної групи та їх сполук у медицині і фармації
- •Лабораторна робота реакції катіонів V аналітичної групи
- •Загальна характеристика
- •Загальноаналітичні реакції катіонів V аналітичної групи
- •1. Дія розчину амоніаку nh3·h2o (дія групового реагенту)
- •2. Дія рочину лугу NaOh або кон
- •Реакції Магній(іі)-катіона
- •1. Дія розчину натрій гідрогенфосфату Na2hpo4 (фармакопейна реакція)
- •2. Дія розчину 8-гідроксихіноліну (фармакопейна реакція)
- •Реакція Ферум(іі)-катіона
- •1. Дія розчину калій гексаціаноферату(ііі) k3[Fe(cn)6] (фармакопейна реакція)
- •Реакції Ферум(ііі)-катіона
- •1. Дія розчину калій гексаціаноферату(іі) k4[Fe(cn)6] (фармакопейна реакція)
- •2. Дія розчину амоній тіоціанату nh4ncs (фармакопейна реакція)
- •3. Дія розчину тіогліколевої кислоти hsch2cooh (фармакопейна реакція)
- •Реакція Манган(іі)-катіона
- •1. Дія діамоній гексаоксопероксидисульфату (nh4)2s2o8
- •Реакції Бісмут(ііі)-катіона
- •1. Дія свіжоприготованого натрій тетрагідроксостаніту(іі) Na2[Sn(oh)4]
- •2. Гідроліз солей Бісмуту
- •3. Дія розчину тіосечовини (nh2)2cs (фармакопейна реакція)
- •4. Дія розчину натрій сульфіду Na2s (фармакопейна реакція)
- •Контрольні питання
- •Біологічна роль та практичне застосування катіонів V аналітичної групи та їх сполук у медицині та фармації
- •Лабораторна робота аналіз суміші катіонів V аналітичної групи
- •Лабораторна робота реакції катіонів VI аналітичної групи
- •Загальноаналітичні реакції катіонів VI аналітичної групи
- •1. Дія розчину амоніаку (дія групового реагенту)
- •Реакції Купрум(іі)-катіона
- •1. Дія надлишку розчину амоніаку nн3·н2о
- •2. Дія розчину натрій тіосульфату Na2s2o3
- •Реакції Кобальт(іі)-катіона
- •1. Дія розчину амоній тіоціанату nh4ncs
- •Реакція Нікол(іі)-катіона
- •1. Дія диметилгліоксиму (реактиву Чугаєва) (фармакопейна реакція)
- •Реакції Меркурій(іі)-катіона
- •1. Дія розчину лугу (фармакопейна реакція)
- •2. Дія розчину калій йодиду кі (фармакопейна реакція)
- •3. Реакція з міддю та іншими металами (фармакопейна реакція)
- •Дія розчину натрій сульфіду Na2s
- •Аналіз аніонів
- •Лабораторна робота реакції аніонів і аналітичної групи
- •Загальна характеристика
- •Дія групового реагенту
- •Реакції сульфат-іона
- •Реакції сульфіт - іона
- •1. Дія мінеральної кислоти (фармакопейна реакція)
- •2. Дія розчину дийоду і2 (фармакопейна реакція)
- •Реакції тіосульфат-іона
- •1. Дія хлоридної кислоти hCl
- •2. Дія розчину дийоду і2
- •3. Дія аргентум (і) нітрату AgNo3
- •Реакції карбонат- та гідрогенкарбонат- іонів
- •1. Дія мінеральних кислот
- •2. Дія магній сульфату MgSo4 (фармакопейна реакція)
- •3. Дія фенолфталеїну (реакція фармакопейна)
- •Реакції фосфат- та гідрогенфосфат- іонів
- •1. Дія аргентум(і) нітрату AgNo3 (фармакопейна реакція)
- •2. Дія розчину магнезіальної суміші (MgCl2, nh4Cl, nh3·h2o)
- •Реакції тетраборат- та метаборат-іонів
- •1. Дія солей Барію
- •2. Реакція забарвлення полум'я (фармакопейна реакція)
- •Реакції хромат- та дихромат-іонів
- •1. Дія розчину солей Барію
- •2. Дія розчину калій йодиду кі
- •Реакція оксалат-іона
- •1. Дія розчину кальцій хлориду СаСl2
- •Контрольні питання
- •Біологічна роль і практичне використання аніонів і аналітичної групи та їх сполук у медицині та фармації
- •Реакції хлорид-іона
- •Реакції бромід-іона
- •1. Дія аргентум(і) нітрату AgNo3 (фармакопейна реакція)
- •2. Дія окисників
- •2.1. Дія хлорної води
- •2.2. Дія калій преманганату
- •Реакції йодид-іона
- •1. Дія окисників (фармакопейна реакція)
- •2. Дія солей Плюмбуму(іі)
- •Реакція сульфід-іона
- •1. Дія мінеральних кислот
- •Контрольні питання
- •Біологічна роль і практичне використання аніонів II аналітичної групи та їх сполук у медицині та фармації
- •1. Дія дифеніламіну (фармакопейна реакція)
- •2. Дія Ферум(іі)-катіонів
- •Реакції нітрит-іона
- •1. Дія кислоти
- •2. Реакція з антипірином (фармакопейна реакція)
- •Реакції ацетат-іона
- •1. Реакція естерифікації (фармакопейна реакція)
- •2. Дія ферум(III) хлориду (фармакопейна реакція)
- •Контрольні питання
- •Біологічна роль і практичне використання аніонів ш аналітичної групи та їх сполук у медицині та фармації
- •3.2 Відкриття аніонів
- •Контрольні завдання
- •Додатки
- •Забарвлення полум'я сполуками деяких елементів
- •Способи виразу вмісту компонентів у розчині
- •Кількісні характеристики процесу гідролізу солей
- •Аніони, які утворюють газоподібні продукти
- •Глава 1. Деякі положення теорії електролітичної дисоціації
- •Глава 2. Кислотно-основна рівновага
- •Глава 3. Рівновага в гетерогенних системах
- •Глава 4. Рівновага в окисно-відновних системах
- •Глава 5. Рівновага комплексоутворення
Глава 2. Кислотно-основна рівновага
2.1. Хімічна рівновага. Константа хімічної рівноваги
В будь-якій хімічній системі при перебігу реакції настає момент, коли співвідношення між концентраціями вихідних речовин та продуктів реакції стає постійним. При цьому перебіг процесу не припиняється, просто це означає, що швидкості прямої та зворотної реакцій стають рівними. Такий рівноважний стан називається динамічним (рухливим).
У стані рівноваги концентрації вихідних речовин та продуктів реакції за даних умов залишаються незмінними. Такі концентрації називають рівноважними.
Кількісною характеристикою хімічної рівноваги є константа рівноваги К.
Розкрити поняття константи рівноваги хімічної реакції можна на підставі закону діючих мас (К.М.Гульдберг та П. Вааге), який формулюють таким чином:
ш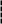 видкість
хімічної реакції прямо пропорційна
добутку концентрацій реагуючих речовин
в ступенях, що дорівнюють їхнім
стехіометричним коефіцієнтам
видкість
хімічної реакції прямо пропорційна
добутку концентрацій реагуючих речовин
в ступенях, що дорівнюють їхнім
стехіометричним коефіцієнтам
Терміном "діючі маси" автори закону позначали концентрації. Сам термін "концентрація" був введений пізніше Вант-Гоффом.
Для реакції:
aA + bB ↔ cC + dD
згідно з законом діючих мас, швидкість прямої Vпр та оборотної Vобор реакцій виражають рівняннями:
Vпр = kпр[A]a[B]b
Vобор = kобор[С]с[D]d
У стані рівноваги швидкості прямої та зворотної реакцій однакові, тобто
Vпр = Vобор:
kпр[A]a[B]b = kобор[С]с[D]d
Перетворимо це рівняння таким чином, щоб всі константи були ліворуч, а концентрації праворуч:
![]()
Відношення констант швидкості прямої та оборотної реакцій також є константою. Її називають концентраційною константою рівноваги даної реакції і позначають Кс.
![]()
Таким чином, можна дати формулювання константи хімічної рівноваги:
К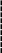 онстанта
хімічної рівноваги
прямо пропорційна добутку концентрацій
продуктів реакції в
ступенях, що дорівнюють їхнім
стехіометричним коефіцієнтам
та зворотно пропорційна добутку
концентрацій
вихідних речовин в ступенях, що дорівнюють
їхнім стехіометричним коефіцієнтам.
онстанта
хімічної рівноваги
прямо пропорційна добутку концентрацій
продуктів реакції в
ступенях, що дорівнюють їхнім
стехіометричним коефіцієнтам
та зворотно пропорційна добутку
концентрацій
вихідних речовин в ступенях, що дорівнюють
їхнім стехіометричним коефіцієнтам.
Величина константи рівноваги залежить від природи реагуючих речовин і температури. Константа рівноваги визначає глибину перебігу процесу в момент досягнення стану рівноваги. Чим більша величина К, тим повніше взаємодіють речовини.
2.2. Рівновага в розчинах слабких електролітів
Слабкі кислоти та основи у водних розчинах дисоціюють частково і в дуже незначній кількості ( α <<1). В таких розчинах встановлюється рівновага між іонами та недисоційованими молекулами.
Рівновага в розчинах слабких кислот
Наприклад, для оцтової кислоти:
CH3COOH ↔ H+ + CH3COO–
Вираз для константи рівноваги:
![]()
Рівновагу, що встановилася при дисоціації оцтової кислоти, характеризує константа рівноваги Ka , яку можна назвати константою дисоціації (іонізації) оцтової кислоти або константою кислотності.
Оскільки константи рівноваги для багатьох слабких електролітів мають дуже малі значення, то часто наводять не самі ці значення, а їхні десяткові логарифми lgK або показники – від'ємні десяткові логарифми рК = - lgK
Так, для процесу дисоціації оцтової кислоти Кa = 1,86 ·10-5 , можна записати lgKa = - 4,73 або рКa= - lgKa = - lg1,86·10-5 = 4,73
Константа дисоціації і ступінь електролітичної дисоціації є кількісними характеристиками електролітів. Для слабких електролітів ці дві величини пов’язує між собою закон розведення В. Оствальда. Математичний вираз закону розведення В. Оствальда:
![]()
де: Кдис – константа дисоціації;
α – ступінь дисоціації;
с – концентрація електроліту.
Для бінарних слабких електролітів α << 1, тоді величина (1-α) практично дорівнює одиниці. Тоді математичний вираз закону розведення В. Оствальда спрощується:
![]()
Для одноосновних слабких кислот НА:
[H+]
=
![]()
де: Ка – константа дисоціації;
α – ступінь дисоціації;
с – концентрація кислоти.
Звідси,
рН = ½ (рКa +рса)
Багатоосновні кислоти дисоціюють ступінчасто. Наприклад, в розчині ортофосфатної кислоти встановлюються рівноваги:
H3PO4
↔ H+
+ H2PO4–
![]()
H2PO4–
↔ H+
+HPO42–
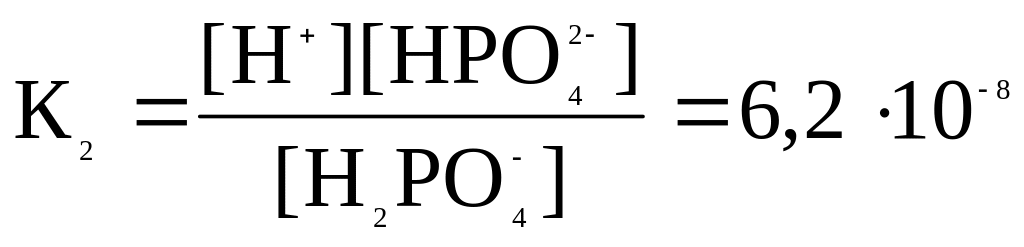
HPO42–
↔ H+
+ PO43–
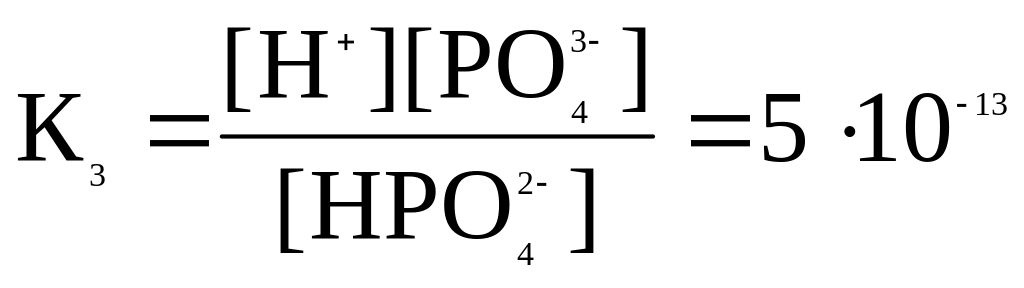
Добуток всіх констант ступінчастої дисоціації дорівнює повній константі кислотності Ка:
К1·К2·К3 = Кa
Тобто, для ортофосфатної кислоти повна константа кислотності для схеми:
H3PO4 ↔ 3H+ + PO43–
![]()
Рівновага в розчинах слабких основ
Наприклад, рівновага в розчині амоніаку:
NH3·H2O ↔ NH4+ + OH–
![]()
Кb – константа дисоціації (іонізації) слабкої однокислотної основи або просто константа основності цієї основи
рКb = -lgKb
Враховуючи, що іонний добуток води Кw = [H+]·[OH-], після певних перетворень, отримуємо:
Кw =Kb·Ka
Тобто, іонний добуток води Кw дорівнює добутку констант кислотності та основності.
Для показника рКw отримуємо:
рКw = рKb + рKa
Визначимо рівноважне значення рН в розчині слабкої однокислотної основи.
Оскільки рКw = рН + рОН = 14, то
рН = рКw – рОН = 14 – рОН
Визначимо
величину рОН = -lg[OH-].
Оскільки [OH-]
=
![]() ,
то
логарифмуючи цей вираз, отримаємо:
,
то
логарифмуючи цей вираз, отримаємо:
- lg[OH-] = ½ (- lgKb - lgсb)
або
рОН = ½ (рKb - рсb)
тоді
рН = 14 - рОН = 14 – ½ (рKb - рсb)
Таким чином, рН в розчинах слабких кислот та основ визначається за формулами:
кислоти |
основи |
рН = ½ (рКa +рса) |
рН = 14 – ½ (рKb - рсb) |
