
- •Глава 1. Гипертоническая болезнь (эссенциальная гипертензия)
- •Глава 2. Стенокардия......................................................................................................................48
- •2.4.1.3. Ингибиторы ангиотензинпревращающего фермента...............................................................71
- •Глава 3 Инфаркт миокарда ........................................................................................................88
- •Глава 4. Осложнения инфаркта миокарда ........................................................................136
- •Глава 5. Нрс ……………………………………………………………...............................157
- •Глава 6. Недостаточность кровообращения ......................................................................230
- •7.4. Аортальная недостаточность...........................................................................................................267
- •Глава 1 Гипертоническая болезнь (эссенциальная гипертензия) и симптоматические гипертензии
- •1.1. Классификация гипертонической болезни
- •I стадия II стадия III стадия
- •1.2. Патогенез гипертонической болезни
- •2. Факторы, связанные с образом жизни:
- •1.3. Клиническая картина и особенность течения гипертонической болезни
- •1.4.1. Электрокардиографические признаки гипертрофи левого желудочка
- •1.4.2. Рентгеноскопия и рентгенография грудной клетки
- •1.4.3. Эхокардиографические критерии гипертрофии левого желудочка
- •1.4.4. Оценка состояния глазного дна
- •1.4.5. Изменение почек при гипертонической болезни
- •1.5. Симптоматические артериальные гипертензии
- •1.5.1. Почечные артериальные гипертензии
- •1.5.2. Вазоренальная артериальная гипертензия
- •1.5.2.1. Атеросклероз почечных артерий
- •1.5.2.2. Фибромускулярная дисплазия почечный артерий
- •1.5.3. Болезнь Такаясу
- •1.5.4. Эндокринные артериальные гипертензии
- •1.5.4.1. Акромегалия
- •1.5.4.2. Болезнь и синдром Иценко-Кушинга
- •1.5.4.3. Феохромоцитома
- •1.5.4.4. Синдром Конна
- •1.5.4.5. Диффузный или диффузно-узловой токсический зоб
- •1.5.4.6. Гиперпаратиреоз
- •1.5.4.7. Климактерическая артериальная гипертензия
- •1.5.4.8. Артериальная гипертензия при использовании гормональных контрацептивов
- •1.5.5. Церебральные артериальные гипертензии
- •1.5.6.. Гемодинамические артериальные гипертензии
- •1.5.6.1. Склеротическая систолическая артериальная гипертензия
- •1.5.6.2. Коарктация аорты
- •1.5.6.3. Аортиты
- •1.5.6.4. Аортальная недостаточность
- •1.5.6.5. Атриовентрикулярная блокада III степени
- •1.5.6.7. Застойная артериальная гипертензия при сердечной недостаточности
- •1.5.7. Артериальная гипертензия лекарственного генеза
- •1.6. Принципы дифференциальной диагностики симптоматических гипертензий
- •Лечение гипертонической болезни
- •1 Изменение образа жизни в лечении гипертонической болезни:
- •1.7.1. Характеристика гипотензивных средств
- •1.7.1.1. Бета-адреноблокаторы
- •1.7.2. Альфа-1-адреноблокаторы
- •1.7.3. Антагонисты кальция
- •1.7.4. Диуретики
- •1.7.5. Ингибиторы ангиотензинпревращающего фермента
- •1.7.6. Монотерапия гипертонической болезни
- •1.7.7. Комбинированное использование антигипертензивных препаратов
- •1.7.8. Лечение изолированной систолической артериальной гипертензии у пожилых больных
- •1.7.9. Гипертензивные (гипертонические) кризы и их лечение
- •Глава 2 Стенокардия
- •2.1. Классификация и клинические формы стенокардии
- •2.1.1. Стабильная стенокардия
- •2.1.2. Нестабильная стенокардия
- •2.1.3. Острая коронарная недостаточность
- •2.2. Диагностика стенокардии
- •2.2.1. Диагностика стенокардии с помощью нагрузочных проб
- •2.2.1.1. Пробы, проводимые при отсутствии изменений конечной части желудочкового комплекса – зубца т и сегмента s-t
- •2.2.1.2. Функциональные нагрузочные пробы при наличии изменения конечного комплекса qrs-t (подъем или депрессия сегмента s-t или инверсия зубца т)
- •2.3. Дифференция диагностика стенокардии (кардиалгий)
- •II группа. Основной клинический синдром – постоянные боли в области грудной клетки, длительностью от нескольких суток до нескольких недель или месяцев, не купирующиеся приемом нитроглицерина.
- •III группа. Основной клинический синдром – боли в грудной клетке, появляющиеся при физической нагрузке, стрессе, в покое длительностью от нескольких минут до 1 ч, уменьшающиеся в покое.
- •IVб подгруппа. Основной клинический синдром – развитие болей в грудной клетке при приеме пищи, уменьшающихся в покое, не купирующихся приемом нитроглицерина.
- •2.4. Лечение больных стенокардией
- •2.4.1 Антиангинальные препараты
- •2.4.1.1. Нитросоединения (нитраты)
- •2.4.1.2. Бета-адреноблокаторы и антагонисты кальция
- •2.4.1.3. Ингибиторы ангиотензинпревращающего фермента
- •2.4.1.4. Антиагреганты
- •2.4.2. Выбор препаратов при лечении стенокардии
- •2.4.3. Оперативное лечение больных стенокардией
- •2.4.4. Использование низкоинтенсивного лазерного излучения в терапии стенокардии
- •Глава 3 Инфаркт миокарда
- •3.1. Этиология инфаркта миокарда
- •3.2. Диагностика инфаркта миокарда
- •3.2.1. Электрокардиографическая диагностика инфаркта миокарда
- •3.2.1.1. Крупноочаговый инфаркт миокарда
- •3.2.1.2. Мелкоочаговый инфаркт миокарда
- •3.2.1.3. Атипичные формы первого инфаркта миокарда
- •3.2.1.4. Изменения электрокардиограммы при повторных инфарктах миокарда
- •3.2.2. Биохимическая диагностика инфаркта миокарда
- •3.2.3. Сцинтиграфия миокарда
- •3.2.4. Эхокардиографическая диагностика
- •3.3. Дифференциальная диагностика инфаркта миокарда
- •3.4. Неосложненный инфаркт миокарда
- •3.4.1. Резорбционно-некротический синдром при инфаркте миокарда
- •3.4.2. Лечение неосложненного инфаркта миокарда
- •R Комментарии к лечению больных неосложненным инфарктом миокарда
- •R Наблюдение за больными инфарктом миокарда
- •R Уровень активности больных инфарктом миокарда
- • Анальгезия и использование антидепрессантов при инфаркте миокарда
- •R Магнезия (MgS04 25% раствор)
- •3.5. Инфаркт правого желудочка и его дисфункция
- •3.6. Подготовка к выписке больных инфарктом миокарда из стационара
- •3.7. Вторичная профилактика у больных инфарктом миокарда после выписки из стационара
- •3.8. Длительное ведение больных инфарктом миокарда
- •Глава 4 Осложнения инфаркта миокарда
- •4.1. Осложнения инфаркта миокарда
- •4.1.2. Кардиогенный шок.
- •4.1.3. Сердечная астма и отек легких.
- •4.1.4. Нарушения сердечного ритма и проводимости
- •4.1.4.1. Тахисистолические нарушения сердечного ритма
- •1 Лечение фибрилляции и трепетания предсердий, пароксизмальной наджелудочковой тахикардии
- •1 Желудочковая тахикардия и фибрилляция желудочков.
- •4.1.4.2. Брадиаритмии и блокады сердца
- •4.1.5. Разрывы миокарда
- •4.1.5.1. Острая митральная регургитация
- •4.1.5.2. Постинфарктный дефект перегородки
- •4.1.5.3. Разрыв свободной стенки левого желудочка
- •4.1.6. Аневризма левого желудочка
- •4.1.7. Тромбоэмболия легочной артерии
- •4.1.8. Перикардит
- •2 Лечение перикардита при инфаркте миокарда.
- •4.1.9. Острая язва желудка
- •4.1.10. Атония мочевого пузыря
- •4.1.11. Парез желудочно-кишечного тракта
- •4.1.12. Синдром Дресслера (постинфарктный синдром)
- •4.1.13. Хроническая недостаточность кровообращения
- •4.1.14. Показания для экстренного проведения аортокоронарного шунтирования при инфаркте миокарда
- •4.1.15. Рецидивирующий инфаркт миокарда
- •Глава 5 Нарушения сердечного ритма и проводимости: диагностика и лечение
- •5.1. Классификация антиаритмических средств и характеристика основных противоаритмических препаратов
- •5.2. Экстрасистолия
- •5.2.1. Электрокардиографическая диагностика желудочковой и наджелудочковой экстрасистолии
- •5.2.2. Лечение и профилактика наджелудочковой и желудочковой экстрасистолии в зависимости от механизмов их развития
- •5.2.2.1. Оценка механизмов развития экстрасистолии
- •5.3. Диагностика и лечение пароксизмальных тахикардий
- •5.3.1. Диагностика наджелудочковых тахикардий
- •5.3.1.1. Электрокардиографические критерии однофокусных предсердных тахикардий
- •5.3.1.2. Электрокардиографические критерии постоянно-возвратной или экстрасистолической формы предсердной тахикардии (форма Gallaverdin)
- •5.3.1.3. Электрокардиографические критерии многофокусной (политопной) или хаотической предсердной тахикардии
- •5.3.1.4. Электрокардиографические критерии реципрокных атриовентрикулярных тахикардий
- •5.3.2. Электрокардиографические признаки желудочковой тахикардии
- •5.3.3.1. Лечение атриовентрикулярных, очаговых (реципрокных) предсердных тахикардий
- •5.3.3.3. Лечение многофокусной, политопной или хаотической пароксизмальной предсердной тахикардии
- •5.3.4. Лечение желудочковых тахикардий
- •5.3.4.1. Лечение экстрасистолической или возвратной формы пароксизмальной желудочковой тахикардии
- •5.4. Фибрилляция (мерцание) и трепетание предсердий
- •5.4.1. Электрокардиографическая диагностика фибрилляции и трепетания предсердий
- •5.4.1.1. Электрокардиографическая диагностика трепетания предсердий
- •5.4.1.2. Электрокардиографические диагностические критерии фибрилляции (мерцания) предсердий
- •5.4.2. Классификация мерцания и трепетания предсердий
- •5.4.3. Лечение и профилактика пароксизмов фибрилляции и трепетания предсердий
- •5.4.3.1. Лечение и профилактика пароксизмов трепетания предсердий
- •I тип II тип эит (кардиоверсия) 150-400 j
- •5.4.3.2. Лечение и профилактика мерцания (фибрилляции) предсердий
- •2. Особенность течения пароксизмов мерцания предсердий:
- •5.5. Использование лазеротерапии для лечения нарушений сердечного ритма
- •5.6. Аритмии, обусловленные нарушением функции проводимости
- •. Алгоритм диагностики брадисистолических форм нарушений сердечного ритма, в том числе характерных для синдрома слабости синуовго узла, представлен на рис. 5.28.
- •5.6.2. Атриовентрикулярная блокада
- •5.6.3. Лечение синдрома слабости синусового узла и атриовентрикулярных блокад
- •5.6.3.1. Электрокардиостимуляция
- •Глава 6
- •6.1. Причины сердечной недостаточности
- •2. Некардиальные:
- •6.2. Патогенез недостаточности кровообращения
- •Митральная регургитация
- •1 Классификация недостаточности кровообращения.
- •Классификация недостаточности кровообращения в.Х. Василенко, н.Д. Стражеско при участии г.Ф. Ланга (1935) с дабавлениями н.М. Мухарлямова (1978).
- •I стадия. Подразделяется на период а и б.
- •6.4. Лечение хронической сердечной недостаточности
- •6.4.1. Фармакотерпия сердечной недостаточности
- •6.4.1.1. Применение ингибиторов ангиотензинпревращающего фермента для лечения сердечной недостаточности
- •6.4.1.2. Применение диуретиков для лечения сердечной недостаточности
- •1 Тактика назначения диуретиков:
- •1 Причины резистентности к диуретикам:
- •Выбор диуретика в зависимости от стадии (функционального класса) сердечной недостаточности.
- •6.4.1.3. Применение b-адреноблокаторов для лечения сердечной недостаточности
- •1 Противопоказания к использованию b-адреноблокаторов при сердечной недостаточности (помимо общих противопоказаний):
- •6.4.1.4. Применение сердечных гликозидов для лечения сердечной недостаточности
- •1 Взаимодействие сердечных гликозидов с другими препаратами:
- •6.4.1.5. Принципы лечения недостаточности кровообращения в зависимости от стадии заболевания
- •1 Принципы лечения недостаточности кровообращения в зависимости от стадии заболевания (Smith j.W. Et al., 1997).
- •2. Диуретики;
- •3. Диуретики;
- •1 Критерии стабильного клинического состояния при недостаточности кровообращении (Stevenson l.W. Et al., 1998)
- •6.4.2. Хирургическое лечение сердечной недостаточности
- •Глава 7 Приобретенные пороки сердца
- •7.1. Митральный стеноз
- •2 Классификация митрального стеноза по а.Н. Бакулеву и е.А. Дамир (1955).
- •Осложнения митрального стеноза
- •7.2. Митральная недостаточность
- •2 Показание к оперативному лечению:
- •7.3. Аортальный стеноз
- •7.4. Аортальная недостаточность
- •Основные клинические симптомы аортальной недостаточности, выявляемые при объективном обследовании:
- •7.5. Трикуспидальные пороки сердца
- •7.5.1. Трикуспидаольный стеноз.
- •7.5.2. Трикуспидальная недостаточность
- •2Этиология трикуспидальной недостаточности.
- •7.6. Дифференциальная диагностика пороков сердца
2.4.3. Оперативное лечение больных стенокардией
Если медикаментозное лечение не имеет успеха и интервалы между приступами ангинозных болей сокращаются, больному необходимо провести селективную коронарографию и определить возможность проведения оперативного вмешательства. Главной целью хирургического лечения больных стенокардией является облегчение клинических симптомов заболевания, улучшение качества и продолжительности жизни. Вопрос о показаниях к оперативному лечению является достаточно серьезным, поскольку хирургические операции на коронарных артериях могут привести к различным осложнениям и даже летальному исходу. Операционная летальность в лучших клиниках мира составляет 1-4% и значительно возрастает, если утяжеляется контингент больных, направляемых на операцию - смертность увеличивается до 20-45% у пациентов с сопутствующей аневризмой сердца, сниженной сократительной функцией миокарда, нестабильной стенокардией, прединфарктным состоянием (Соловьев Г.М. и соавт., 1990, Wilson R.E. et al., 1986, Kannel W.B. et al.,1986, Myler R.K. et al.,1990). Чем менее тяжел контингент больных, направляемых на операцию, тем лучше эффект (Blevins R.D. et al.,1986). По данным многих авторов, хирургическое лечение у 70-80% больных приводит к значительному урежению или полному прекращению приступов стенокардии на 3-4 года и более в условиях обычной активности организма (Шхвацабая И.К., 1975, Гасилин В.С., Сидоренко Б.А.,1987, Чазов Е.И.,1982, 1992, Halim M.A. et al.,1982, Mabin T.A. et al.,1985). Поэтому основная задача медикаментозной терапии состоит в предупреждении развития инфаркта миокарда, перехода нестабильной стенокардии и предынфарктного состояния в стабильную стенокардию с возможностью в дальнейшем проведения оперативного лечения.
В настоящее время используется несколько видов операций: аортокоронарное шунтирование в различных модификациях; баллонная дилатация коронарных артерий; протезирование (пластика) коронарных артерий; чрескожная транслюминарная ангиопластика; удаление бляшки с помощью фокусированного лазерного луча.
Аортокоронарное шунтирование. Впервые операция аорто-коронарного шунтирования проведена в СССР Амосовым в 1964 г. Сущность операции заключается в том, что после выявления локализации стеноза венечных артерий на нее накладывается шунт, который в обход стеноза доставляет кровь к сердечной мышце (см. рис. 2.5.).
Существуют разные мнения относительно выбора шунта, но некоторые данные свидетельствуют, что применение большой подкожной вены бедра для аортокоронарного шунтирования наиболее оправдано. Однако при ее использовании в качестве шунта иногда в нем наступает развитие атеросклероза и пролиферации интимы, что приводит к нарушению его проходимости. Если в качестве шунта используется внутренняя грудная артерия, то, по данным многих авторов, атеросклеротический процесс в стенке шунта не развивается. В ряде случаев используют в качестве шунта искусственную коронарную артерию (протез). В последние годы применяют сочетание шунтирования с подшиванием внутренней грудной артерии ниже шунта.
Показания к проведению аорто-коронарного шунтирования у больных стенокардией:
- поражение основного ствола левой коронарной артерии;
- стенокардия, развившаяся менее 3 месяцев назад;
- поражение трех коронарных артерий;
- поражение двух коронарных артерий, включая проксимальную часть левой нисходящей коронарной артерии;
- положительная нагрузочная проба (снижение сегмента ST более чем на 2 мм при проведении велоэргометрии (тредмила) или чреспищеводной электрокардиостимуляции), а также патологическиеизменения электрокардиограммы, выявляемые в покое;
- снижение сегмента ST в покое в сочетании с анамнестическими сведениями о ранее перенесенном инфаркте миокарда или артериальной гипертензии; либо пациенты III-IV функционального класса сердечной недостаточности по классификации NYHA.

Рис. 2.5. Схема проведения аортокоронарного шунтирования.
В обход стеноза наложен шунт, который доставляет кровь к сердечной мышце.
С целью сохранения проходимости аортокоронарного шунта назначают аспирин, варфарин и другие антикоагулянты.
В настоящее время используют два основных неинвазивных способа оценки проходимости шунта с помощью нагрузочных проб: электрокардиографический и использование радиоизотопов (технеций-99-пирфотех). Установлено, что если у больного после аортокоронарного шунтирования в покое и при проведении нагрузочных проб ишемические изменения не выявляются, то вероятность проходимости шунта составляет, в среднем, 90%, а если ишемические изменения, возникающие во время пробы, нормализуются в покое, то вероятность его проходимости составляет - 80%. Если ишемические изменения длительно не нормализуются или наблюдаются в покое с усугублением при проведении пробы, то вероятность окклюзии шунта составляет, в среднем, 80%. Многочисленные результаты ангиографических исследований, проведенных после аортокоронарного шунтирования, показали, что с каждым годом после операции проходимость шунта уменьшается, в среднем, на 10-20%. Осложнения, согласно многочисленным данным рандомизированных исследований, составляют от 0,2% до 4%.
Положительный клинический эффект после аортокоронарного шунтирования (исчезновение ангинозных болей и повышение работоспособности пациентов) наблюдается на протяжении 4-15 лет (в среднем 5-7 лет). Продолжительность клинического эффекта уменьшается, если операция проведена у больных нестабильной стенокардией, сразу после или через 1-2 года после перенесенного инфаркта миокарда.
Баллонная дилатация коронарных артерий. Методика баллонной дилатации коронарных артерий была предложена B. Dotter, R. Judkins в 1964 г. Широкое признание методика получила в 1974 г., когда A. Gruntzig предложил баллон-катетер с двумя просветами для дилатации стенозированной артерии. Методика баллонной дилатации заключается в следующем. С помощью коронарной ангиографии определяется точное место стеноза, затем в нее вводится дилатационный катетер, имеющий баллон длиной 2 см и расширяющийся при введении воздуха под давлением до 2-4 мм. Дилатирующийся баллон разрушает атеросклеротическую бляшку и стеноз ликвидируется (см. рис. 2.6.).
Показания к проведению баллонной дилатации коронарных артерий такие же, как для аортокоронарного шунтирования.
Противопоказания к проведению баллонной дилатации коронарных артерий:
- стеноз основного ствола левой коронарной артерии;
- субтотальные стенозы коронарных артерий;
- вазоспастическая стенокардия.
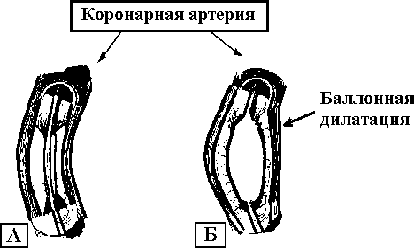
Рис. 2.6. Схема проведения баллонной дилатации коронарной артерии.
В коронарную артерию введен катетер с баллоном (А). Дилатирующий баллон разрушает атеросклеротическую бляшку и кровоток в артерии восстанавливается (Б).
Если раньше баллонная дилатация коронарных артерий использовалась преимущественно у больных стабильной стенокардией, то в настоящее время эта процедура проводится у большинства больных, при отсутствии противопоказаний, включая пациентов имеющих критическую степень стеноза (более 85-90%) при коронарографии. Осложнения этой процедуры наблюдаются, по данным разных авторов, от 5 до 15%, причем они обусловлены диссекцией коронарных артерий с последующим развитием инфаркта миокарда. Поэтому повсеместно пациентам после проведения баллонной дилатации и восстановления коронарного кровотока рекомендуется в дальнейшем проведение аортокоронарного шунтирования, так как продолжительность клинического эффекта после дилатации намного меньше, чем при аортокоронарном шунтировании, и составляет от 1 года до 2-4 лет.
Протезирование (пластика) коронарных артерий. Это оперативное вмешательство предложено в последние годы и заключается в том, что, если у больного коронарные артерии поражены на всем своем протяжении и нет возможности проведения аортокоронарного шунтирования или других каких-либо оперативных вмешательств, их заменяют на искусственные коронарные артерии (протезы). Положительный эффект при проведении этой операции отмечается на протяжении 5-12 лет, а осложнения наблюдаются от 0,4% до 4% случаев.
Чрескожная транслюминарная ангиопластика. Эта операция предложена в последние годы и проводится преимущественно при изолированном стенозе 1-2 коронарных артерий крупного или среднего калибра. Метод заключается в том, что в коронарную артерию вводится специальный проводник с утолщением на конце в виде оливы, покрытой алмазной пылью, размером 2-4 мм, который вращается со скоростью 20-100 оборотов в минуту. При прохождении проводника по неизмененным артериям, они расширяются, а на уровне стеноза - не дилатируются и олива, вращаясь, срезает атеросклеротическую бляшку, а место стеноза покрывается специальным составом, чтобы на его месте не образовывался тромб (см. рис. 2.7.). Следует отметить, что продукты распада бляшки меньше размера тромбоцита и они выводятся с почками. Положительный эффект при проведении этой операции в настоящее время изучается, но, по последним данным, отмечается в течение, по крайней мере, 5-8 лет. Осложнения при проведении чрескожной транслюминарной ангиопластики (перфорация стенки коронарной артерии, повреждение субэндокардиальных структур и образование тромба) наблюдаются в 1-2% случаев.
Рис. 2.7. Схема проведения чрескожной транслюминарной ангиоплатики коронарной артерии.
В коронарную артерию вводится специальный проводник (зонд) с утолщением на конце в виде оливы, покрытой алмазной пылью, который вращается со скоростью 20-100 оборотов в минуту. При прохождении проводника по неизмененным артериям, они расширяются, а на уровне стеноза - не дилатируются и олива, вращаясь, срезает атеросклеротическую бляшку.
Следует отметить, что продолжительность положительного клинического эффекта после проведения вышеуказанных оперативных вмешательств зависит не только от техники проведения и выбора операции, но и от образа жизни пациента: от соблюдения им гипохолестеринемической диеты, от степени физической активности, от регулярности приема антиагрегантов, антикоагулянтов и т.д.
Реканализация коронарных артерий (удаление бляшек) и миокарда с помощью фокусированного лазерного луча. Направляемый через гибкое оптическое волокно лазерный луч мощностью в несколько ватт удаляет бляшку, вызывая адсорбцию световой энергии с последующей ее трансформацией в тепловую, которая приводит вначале к плавлению, а затем – к ее испарению. Эффективность лечения с помощью мощного лазерного излучения зависит от состава бляшки (содержания липидов, гиалина, кальция), свойств лазерного луча (длины волны, степени фокусировки луча, мощности и длительности воздействия), а также от умения врача контролировать глубину воздействия и ограничивать термическое повреждение окружающей ткани (Grundfist W.S. et al., 1985). Осложнения этой процедуры наблюдаются, по данным разных авторов, до 20-30%, причем они обусловлены перфорацией и повреждением коронарных артерий с последующим развитием инфаркта миокарда. По этим причинам лазер не применяется в ежедневной клинической практике для лечения больных стенокардией. Прежде чем этот способ лечения будет широко применяться в клинической практике, необходимы дальнейшие исследования и совершенствование технологии.
В последние годы для лечения стенокардии стали использовать углекислый и иттритий-алюминиво-рубиновый лазеры для создания новых каналов в миокарде. Этот метод впервые был предложен M.Okada et al. (1986). В его основе лежит реваскуляризация миокарда при воздействии лазерного луча за счет стимуляции ангиогенеза, ангиогенных факторов роста в сердечной мышце. Лазерная реваскуляризация осуществляется при проведении левосторонней торакотомии или торакоскопии. Однако положительный эффект этой процедуры не подтверждается результатами объективного обследования с использованием сцинтиграфии миокарда, а также теста с физической нагрузкой, в частности, не наблюдается увеличения фракции выброса левого желудочка и повышения толерантности к нагрузке, что связывают с частичной денервацией сердца (Gassler N. et al., 1997, Kwong K.F. et al., 1998). Смертность в послеоперационном периоде составляет 9% (Horvath K.A. et al., 1997). Летальность на 30 день и через 12 месяцев состаляют, в среднем, 12% и 22% соответственно, что сопоставимо только в сравнении с результатами медикаментозной терапии (Nagele H. et al., 1998). Поэтому этот метод применяется в сочетании, например, с аортокоронарным шунтированием (Mack C.A. et al., 1997).

Рис. 2.7. Схема проведения чрескожной транслюминарной ангиоплатики коронарной артерии.
В коронарную артерию вводится специальный проводник (зонд) с утолщением на конце в виде оливы, покрытой алмазной пылью, который вращается со скоростью 20-100 оборотов в минуту. При прохождении проводника по неизмененным артериям, они расширяются, а на уровне стеноза - не дилатируются и олива, вращаясь, срезает атеросклеротическую бляшку.
Следует отметить, что продолжительность положительного клинического эффекта после проведения вышеуказанных оперативных вмешательств зависит не только от техники проведения и выбора операции, но и от образа жизни пациента: от соблюдения им гипохолестеринемической диеты, от степени физической активности, от регулярности приема антиагрегантов, антикоагулянтов и т.д.
Реканализация коронарных артерий (удаление бляшек) и миокарда с помощью фокусированного лазерного луча. Направляемый через гибкое оптическое волокно лазерный луч мощностью в несколько ватт удаляет бляшку, вызывая адсорбцию световой энергии с последующей ее трансформацией в тепловую, которая приводит вначале к плавлению, а затем – к ее испарению. Эффективность лечения с помощью мощного лазерного излучения зависит от состава бляшки (содержания липидов, гиалина, кальция), свойств лазерного луча (длины волны, степени фокусировки луча, мощности и длительности воздействия), а также от умения врача контролировать глубину воздействия и ограничивать термическое повреждение окружающей ткани (Grundfist W.S. et al., 1985). Осложнения этой процедуры наблюдаются, по данным разных авторов, до 20-30%, причем они обусловлены перфорацией и повреждением коронарных артерий с последующим развитием инфаркта миокарда. По этим причинам лазер не применяется в ежедневной клинической практике для лечения больных стенокардией. Прежде чем этот способ лечения будет широко применяться в клинической практике, необходимы дальнейшие исследования и совершенствование технологии.
В последние годы для лечения стенокардии стали использовать углекислый и иттритий-алюминиво-рубиновый лазеры для создания новых каналов в миокарде. Этот метод впервые был предложен M.Okada et al. (1986). В его основе лежит реваскуляризация миокарда при воздействии лазерного луча за счет стимуляции ангиогенеза, ангиогенных факторов роста в сердечной мышце. Лазерная реваскуляризация осуществляется при проведении левосторонней торакотомии или торакоскопии. Однако положительный эффект этой процедуры не подтверждается результатами объективного обследования с использованием сцинтиграфии миокарда, а также теста с физической нагрузкой, в частности, не наблюдается увеличения фракции выброса левого желудочка и повышения толерантности к нагрузке, что связывают с частичной денервацией сердца (Gassler N. et al., 1997, Kwong K.F. et al., 1998). Смертность в послеоперационном периоде составляет 9% (Horvath K.A. et al., 1997). Летальность на 30 день и через 12 месяцев состаляют, в среднем, 12% и 22% соответственно, что сопоставимо только в сравнении с результатами медикаментозной терапии (Nagele H. et al., 1998). Поэтому этот метод применяется в сочетании, например, с аортокоронарным шунтированием (Mack C.A. et al., 1997).
