
- •Предисловие
- •Общая патология Глава 1. Предмет и задачи патологии. Общее понятие о болезни Предмет "Патология" в системе подготовки провизора
- •Здоровье. Болезнь
- •Этиология. Патогенез. Нозология
- •Стадии развития болезни. Смерть и посмертные изменения
- •Принципы лечения больного
- •Глава 2. О роли наследственности, реактивности и резистентности в патологии Наследственность
- •Реактивность и резистентность
- •Структурно-функциональные изменения при старении человека
- •Адекватные и неадекватные защитные реакции организма
- •Неадекватность адаптивной перестройки организма как причина патологии
- •Глава 3. Общая патология клетки Структурно-функциональные феномены патологии клеток и тканей
- •Факторы, повреждающие клетку
- •Физические повреждающие факторы
- •Этапы свободнорадикального перекисного окисления липидов (спол) и пути антиоксидантной защиты клеток
- •Химические повреждающие факторы
- •Биологические повреждающие факторы
- •Фармакокинетика лекарственных веществ при патологии клеток и тканей
- •Глава 4. Гипоксия
- •Структурно-функциональные изменения при гипоксии
- •Глава 5. Механизмы восстановления нарушенных функций
- •Глава 6. Нарушения кровообращения Нарушения периферического кровообращения
- •Нарушения общего кровообращения
- •Глава 7. Воспаление
- •Местные и общие реакции при воспалении и их проявления. Классическая формула воспаления - боль, краснота, жар, припухлость, нарушение функций (dolor, rubor, calor, tumor, functio laesa)
- •Принципы коррекции воспалительного процесса
- •Глава 8. Иммунопатологические процессы Иммунные реакции
- •Аллергические реакции
- •Иммунодефицитные состояния
- •Глава 9. Инфекционный процесс. Лихорадка Инфекционный процесс
- •Факторы, неблагоприятно влияющие на выздоровление больных при химиотерапии инфекционных болезней
- •Лихорадка
- •Глава 10. Патология обмена веществ. Нарушения водно-электролитного обмена и кислотно-щелочного состояния Роль водно-электролитного обмена в организме и его регуляция
- •Нарушения водного баланса
- •Виды отеков
- •Нарушения обмена электролитов
- •Нарушения кислотно-щелочного состояния (кщс)
- •Глава 11. Патология обмена веществ. Нарушения обмена витаминов Понятие о витаминах. Их роль в организме
- •Причины и механизмы развития витаминной недостаточности
- •Нарушения баланса водорастворимых витаминов. Гипо- и авитаминоз витамина в1 (тиамина)
- •Гиповитаминоз витамина в2 (рибофлавина)
- •Гиповитаминоз витамина рр (никотиновой кислоты)
- •Гиповитаминоз витамина в6 (пиридоксина)
- •Гипо- и авитаминоз витамина с (аскорбиновой кислоты)
- •Гипо- и авитаминоз витамина в12 (цианокобаламина)
- •Витамин р (биофлавоноиды)
- •Нарушение баланса жирорастворимых витаминов. Гипо- и авитаминоз витамина а (ретинола)
- •Гиповитаминоз витамина е (токоферола)
- •Гиповитаминоз витамина d (эргокальциферола и холекальциферола)
- •Глава 12. Патология обмена веществ. Расстройства углеводного, липидного и белкового обмена Физиология и патология обмена углеводов
- •Физиология и патология обмена липидов
- •Физиология и патология белкового обмена
- •Патологические явления, вызванные дефицитом некоторых незаменимых аминокислот
- •Глава 13. Боль. Экстремальные состояния организма Боль
- •Экстремальные состояния организма. Стресс
- •Коллапс. Обморок
- •Глава 14. Опухолевые заболевания
- •Предрасполагающие факторы, клиническая картина и принципы терапии рака желудка, лёгкого и молочной железы
- •Частная патология Глава 15. Болезни системы крови Понятие о гемопоэзе и его регуляции
- •Понятие об анемии. Классификация анемий. Компенсаторно-приспособительные реакции при анемиях
- •Острая постгеморрагическая анемия
- •Дисгемопоэтические анемии Железодефицитная анемия
- •В12 и фолиево-дефицитная анемия
- •Гемолитические анемии
- •Приобретённые гемолитические анемии
- •Наследственные гемолитические анемии
- •Агранулоцитоз
- •Глава 16. Болезни сердечно-сосудистой системы Особенности энергетики и кровоснабжения миокарда
- •Ишемическая болезнь сердца (ибс)
- •Инфаркт миокарда
- •Гипертоническая болезнь. Физиологическая регуляция артериального давления
- •Гипертоническая болезнь (гб)
- •Аритмии сердца. Физиологические особенности системы автоматизма сердца и виды аритмий
- •Электрофизиологическая характеристика проводящей системы сердца и сократительного (рабочего) миокарда
- •Аритмии, вызванные преимущественно нарушением автоматизма
- •Аритмии, обусловленные нарушением автоматизма и возбудимости проводящей системы сердца и миокарда
- •Аритмии, обусловленные нарушением проводимости
- •Глава 17. Болезни органов дыхания Нарушения внешнего дыхания
- •Острый бронхит
- •Очаговая пневмония (бронхопневмония)
- •Крупозная пневмония
- •Бронхиальная астма
- •Хроническая пневмония
- •Туберкулёз лёгких
- •Глава 18. Патология пищеварительной системы. Понятие о недостаточности пищеварения
- •Нарушение пищеварения в полости рта
- •Нарушение аппетита
- •Расстройства акта глотания
- •Гастрит
- •Этиология хронического гастрита
- •Язвенная болезнь желудка и двенадцатиперстной кишки
- •Этиология язвенной болезни
- •Принципы фармакотерапии язвенной болезни
- •Заболевания печени. Функциональные особенности печени
- •Синдром печёночной недостаточности
- •Острый гепатит
- •Хронический гепатит
- •Желчекаменная болезнь (холелитиаз)
- •Цирроз печени
- •Заболевания поджелудочной железы
- •Патология кишечника. Синдромы функциональных нарушений при патологии тонкой и толстой кишки
- •Острый энтерит
- •Хронический энтероколит
- •Глава 19. Болезни почек Функциональные особенности почек. Факторы, нарушающие функции почек
- •Гломерулонефрит
- •Токсические (лекарственные) нефропатии
- •Пиелонефрит
- •Нефролитиаз (мочекаменная болезнь)
- •Почечная недостаточность
- •Острая почечная недостаточность (опн)
- •Хроническая почечная недостаточность (хпн)
- •Глава 20. Эндокринная патология Организация и регуляция эндокринных функций
- •Железы внутренней секреции и их гормоны
- •Причины эндокринных нарушений
- •Патология гипоталамо-гипофизарной системы
- •Несахарный диабет (несахарное мочеизнурение)
- •Адипозо-генитальная дистрофия
- •Гипофизарная кахексия (болезнь Симмондса)
- •Акромегалия. Гигантизм
- •Болезнь Иценко-Кушинга
- •Патология надпочечников при гиперфункции их коры
- •Патология надпочечников при гипофункции их коры
- •Диффузный токсический зоб (болезнь Гревса-Базедова)
- •Гипофункция щитовидной железы (гипотиреоз)
- •Эндокринная патология поджелудочной железы (сахарный диабет)
- •Патология половых желез. Патология яичника
- •Патология яичка
- •Глава 21. Нервные и психические болезни Паркинсонизм
- •Миастения
- •Неврозы
- •Истерия (истерический невроз)
- •Неврастения
- •Невроз навязчивых состояний
- •Нарушения сна
- •Общая психопатология
- •Расстройства познавательной деятельности
- •Расстройства памяти
- •Расстройства мышления
- •Расстройства эмоций (аффективные расстройства)
- •Двигательно-волевые расстройства
- •Расстройства сознания
- •Эпилепсия
- •Шизофрения
- •Аффективные расстройства
- •Словарь
- •Оглавление
- •Глава 16. Болезни сердечно-сосудистой системы 158
- •Глава 17. Болезни органов дыхания 180
- •Глава 18. Патология пищеварительной системы. Понятие о недостаточности пищеварения 199
- •Глава 19. Болезни почек 222
- •Глава 20. Эндокринная патология 235
- •Глава 21. Нервные и психические болезни 253
Принципы коррекции воспалительного процесса
|
Характер воздействия |
Цель терапии |
Принципы терапии |
|
Противовоспалительная терапия |
Необходима для уменьшения и ограничения воспалительного процесса |
1. Специфические (этиотропные) средства. Подавляют внедрение и развитие микроорганизмов, ослабляя тем самым воспалительную реакцию (антисептики, противомикробные средства) |
|
|
|
2. Патогенетическая терапия. Применяют неспецифические противовоспалительные средства, снижающие интенсивность воспаления: холод, средства, тормозящие образование, высвобождение и фиксацию медиаторов воспаления (антигистаминные, ингибиторы кининов и простагландинов); стабилизаторы мембран лизосом (амидопирин, ацетилсалициловая кислота и др.); глюкокортикоиды, снижающие чувствительность макрофагов к лимфокинам и, тем самым, тормозящие образование коллагена - основного белка соединительной ткани; стабилизаторы мембран (витамины С, Р, Е), микроэлемент селен |
|
Местнораздражающая терапия |
Улучшение кровоснабжения ткани |
Средства, которые увеличивают местное кровообращение (тепло, скипидар, горчичники). Их называют иногда отвлекающими средствами |
|
Общая стимулирующая терапия |
Активация защитных сил организма |
Переливание крови; анаболические средства; средства, стимулирующие регенерацию; поливитаминные препараты, содержащие микроэлементы (центрум, поливит); средства, обеспечивающие адаптивную перестройку организма (адаптогены) - женьшень, элеутерококк, дибазол и др. |
Таким образом, принципы терапии воспалительного процесса базируются на уничтожении возбудителя (при септическом воспалении), усилении локальных и общих иммунных механизмов (за исключением аллергического воспаления) и торможении образования нефункциональной рубцовой ткани (в особенности, при хроническом воспалении в жизненно важных органах).
Глава 8. Иммунопатологические процессы Иммунные реакции
Под иммунитетом понимают систему защиты организма от всего генетически чужеродного - будь то микробы, трансплантаты (пересаженные ткани и органы) или изменившиеся в антигенном отношении собственные клетки, включая раковые или отжившие свой срок нормальные.
Прежде чем нейтрализовать, уничтожить и элиминировать (вывести) из организма носителей генетической чужеродности, их необходимо обнаружить и распознать. Все клетки индивидуального организма имеют специальную маркировку (антигены тканевой совместимости), благодаря которой они воспринимаются иммунной системой как «свои». Клетки, не имеющие такой маркировки, воспринимаются как «чужие», атакуются и уничтожаются иммунной системой. Чужеродные вещества и клетки, вызывающие специфический иммунный ответ, называются антигенами. Различают экзогенные антигены (белки, полисахариды, искусственные полимеры, вирусы, бактерии и их токсины, трансплантаты) и эндогенные антигены, к которым относятся собственные ткани организма, измененные повреждением, и мутантные клетки, постоянно появляющиеся в организме человека (в сутки образуется до 106 мутантных клеток). Таким образом, иммунная система защищает многоклеточный организм от вторжения извне и от «внутренней измены» и, тем самым, обеспечивает генетическое постоянство всех соматических клеток, составляющих конкретный индивидуальный организм.
Иммунный ответ осуществляется иммунокомпетентными клетками и продуктами их жизнедеятельности - медиаторами иммунных реакций. Различают Т- и В-системы иммунитета. Т-система обеспечивает преимущественно противоопухолевую, антивирусную защиту, а также реакции отторжения трансплантата. В-система обеспечивает, главным образом, гуморальную антибактериальную защиту и нейтрализацию токсинов. Т-система иммунитета представлена популяцией тимусзависимых лимфоцитов (Т-лимфоцитов), которые имеют разную специализацию:
-
Т-киллеры (Тк) - клетки-убийцы генетически чужеродных клеток;
-
Т-хелперы (Тх) - клетки-помощники - стимулируют посредством хелперных медиаторов образование клона антигенчувствительных Т-киллеров и В-лимфоцитов;
-
Т-супрессоры (Тс) - клетки, подавляющие посредством супрессорных медиаторов иммунный ответ.
Совместная деятельность Тх- и Тс-лимфоцитов определяет направленность, силу и продолжительность иммунного ответа. В начальный период нормального иммунного ответа превалирует активность Т-хелперов, в момент окончания - Т-супрессоров. Активность иммунокомпетентных клеток находится под контролем специальных генов иммунного ответа - Ir-генов. В частности, Ir-гены контролируют синтез антител и медиаторов иммунитета (хелперных и супрессорных).
В-система представлена популяцией В-лимфоцитов, которые, в ответ на антиген (антигенную стимуляцию), трансформируются в плазмоциты, - клетки, синтезирующие антитела (иммуноглобулины) (рис. 8.1). Фагоциты осуществляют фагоцитоз (рис. 8.2).









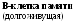

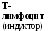

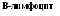
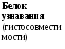

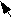





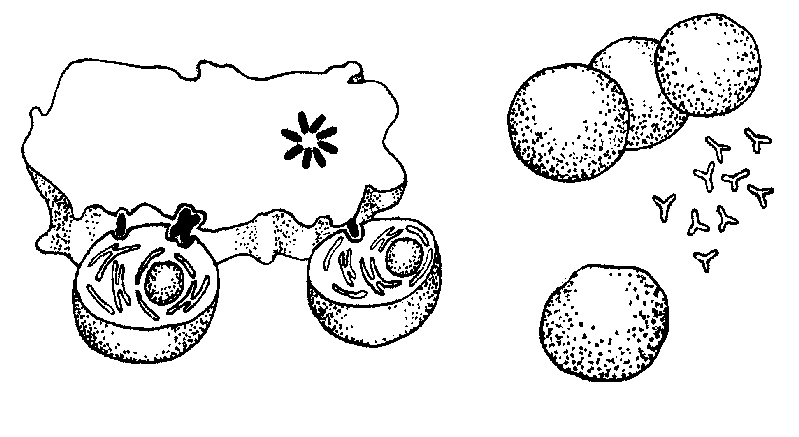
Рис. 8.1. Этапы формирования приобретённого иммунитета:
I - взаимодействие Т- и В-лимфоцитов с участием макрофага;
II - формирование клеток, хранящих информацию об антигенной структуре конкретного микроорганизма и способных вырабатывать специфические белки, связывающие микроорганизмы (антитела)
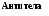




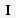

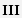
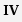






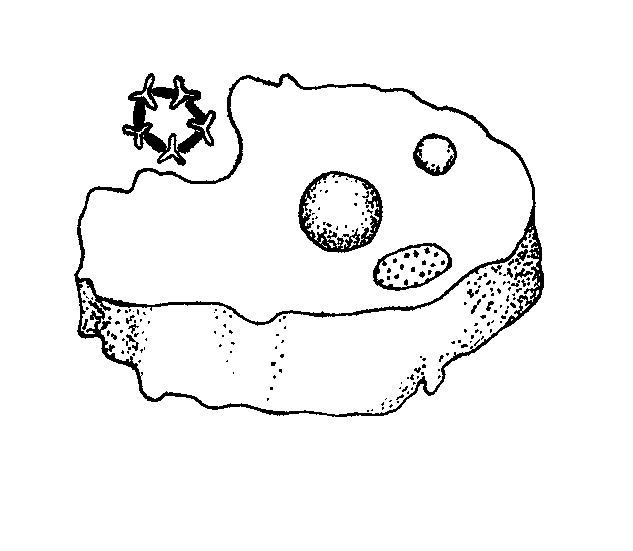
Рис. 8.2. Стадии фагоцитоза:
I - сближение фагоцита с объектом (комплексом антиген-антитело);
II - прилипание (адгезия) - способствуют опсонины;
III - захват фагоцитируемого объекта;
IV - переваривание комплекса антиген-антитело
Известны пять классов иммуноглобулинов: IgМ, IgG, IgА, IgE и IgD, которые продуцируются в строго определенной последовательности. IgM - низкоспецифичные антитела, которые вырабатываются первыми в ответ на антиген. Они образуют непрочную связь с антигеном и мобилизуют плазмоциты на продукцию высокоспецифичных антител (IgG и IgA). Смена синтеза IgM на синтез IgG и IgA происходит под влиянием лимфокинов (медиаторов), секретируемых Т-хелперами. IgG находятся в сыворотке крови и называются сывороточными антителами. Они прочно связывают антиген и являются самыми распространенными антителами против антигенной угрозы. IgA секретируются слизистыми оболочками носа, дыхательных путей, кишечника, урогенитальной системы. Они называются секреторными антителами и выполняют роль «первой линии обороны» в местах внедрения антигена. У млекопитающих они передаются от матери к ребенку через грудное молоко. IgE (реагины) синтезируются преимущественно в лимфоидной ткани слизистых оболочек и лимфатических узлах кишечника и бронхов. Они обладают высокой гомоцитотропностью (сродством к клеткам собственного организма) и поэтому могут выступать в качестве соучастников аллергических реакций. Роль IgD пока не установлена.
Действие иммуноглобулинов на антигены проявляется в следующих вариантах:
-
Агглютинация (склеивание) и иммунный лизис - растворение бактериальных антигенов. Такие иммуноглобулины называются агглютининами и бактериолизинами. Реакции иммунного лизиса происходят при участии комплемента - составной части кровяной сыворотки.
-
Цитотоксическое действие антител (цитотоксинов) - лишение клеток жизнеспособности. Эта реакция также протекает при участии комплемента.
-
Нейтрализация токсинов антителами (антитоксинами).
-
Опсонизация - усиление антителами (опсонинами) фагоцитарной активности микро- и макрофагов.
-
Преципитация - осаждение антигенов антителами.
Полноценный иммунный ответ обеспечивается кооперативным взаимодействием Т-лимфоцитов, В-лимфоцитов и макрофагов. Включение иммунных механизмов защиты начинается с момента проникновения антигена в организм. Макрофаг (моноцит) захватывает антиген, перерабатывает и выводит его антигенные детерминанты (структуры, обусловливающие антигенную уникальность и чужеродность) на свою клеточную поверхность. Обработанный таким образом антиген в 100-1000 раз более иммуногенен, чем нативный антиген. Он включает дальнейшие иммунные механизмы. Антигенные детерминанты, представленные макрофагом, распознаются В-лимфоцитами и Тх-клетками.
Последующее развитие иммунного ответа зависит от вида антигена. На экзогенные антигены (белки, полисахариды, бактерии, паразиты и т.д.) включается преимущественно система гуморального иммунитета, на эндогенные (мутантные и опухолевые клетки, клетки, измененные внешними воздействиями), а также на трансплантаты - клеточного.
При экзогенной антигенной стимуляции В-лимфоциты трансформируются в плазмоциты и начинают сразу же продуцировать низкоспецифичные IgM. Через некоторое время, под влиянием медиаторов Т-хелперов, плазмоциты переключают синтез иммуноглобулинов на высокоспецифичные к данному антигену IgG, а затем - IgA. Одновременно Тх-лимфоциты стимулируют образование клона В- лимфоцитов, в которых формируется иммунная память на данный антиген. Таким способом обеспечивается активный иммунитет.
Тх-лимфоциты стимулируют положительный хемотаксис нейтрофильных лейкоцитов (микрофагов) к месту расположения антигена, что является важным механизмом в обезвреживании бактерий.
Эндогенная антигенная стимуляция вовлекает в иммунный ответ Тк-лимфоциты. В результате кооперации макрофага, Т-хелпера и Т-киллера, последний приобретает свойства размножаться, создавая популяцию антигенчувствительных Тк-клеток, и целенаправленно уничтожать антигены. Помимо Тк-клеток цитотоксические эффекты осуществляются Нк-лимфоцитами (натуральными киллерами), которые уничтожают клеточные антигены (клетки-мишени) без предварительной кооперации (рис. 8.3).
Полноценный иммунный ответ редко осуществляется без взаимодействия его клеточного и гуморального вариантов. Так, Т-киллеры становятся антигенчувствительными, когда связываются со специфическими иммуноглобулинами, комплементарными антигенам клеток-мишений. Макрофаги, опсонизированные иммуноглобулинами, приобретают способность направленно атаковать клетки- мишени и растворять их.
Указанные механизмы иммунного ответа лежат также в основе аллергических реакций.
