- •Часть I. Механизмы хранения и реализации генетической информации 17
- •Предисловие автора
- •Часть I. Механизмы хранения и реализации генетической информации введение
- •Средний размер гаплоидного генома у некоторых групп организмов
- •Гены и хромосомы
- •Геном прокариот
- •Геном вирусов
- •Нуклеоид бактериальной клетки
- •Геном архебактерий
- •Минимальный размер генома одноклеточных организмов
- •Геном эукариот
- •Последовательности нуклеотидов эукариотического генома
- •Хроматин
- •Свойства гистонов животных
- •Роль днк-топоизомераз в обеспечении структуры и функционирования хроматина
- •Реализация генетической информации при экспрессии генов
- •Транскрипция
- •Днк-зависимые рнк-полимеразы
- •Характеристики белковых компонентов холофермента рнк-полимеразы II дрожжей
- •Единицы транскрипции (транскриптоны)
- •Этапы транскрипции
- •Субъединичный состав и характеристика основных факторов транскрипции (gtf) рнк-полимеразы II человека
- •Основные факторы элонгации рнк-полимеразы II
- •Хроматин во время транскрипции
- •Субъединичный состав и свойства белковых комплексов Swi/Snf и nurf
- •Котранскрипционные и посттранскрипционные модификации рнк
- •Процессинг рнк у бактерий
- •Редактирование пре-мРнк
- •Различные способы редактирования мРнк
- •Редактирование рнк у животных и их вирусов
- •Другие модификации эукариотических мРнк
- •Сравнение полиаденилирования мРнк у эукариот и прокариот
- •5’-Концевой сайт Точка 3’-Концевой сайт
- •5’–Экзон 1guaugu__...__uacuaac__...__(Py)nAgэкзон 2–3’
- •Механизм прямой и обратной реакций аутосплайсинга интронов группы I
- •Кэп-связывающий комплекс в роли фактора, сопрягающего основные реакции метаболизма транскриптов рнк-полимеразы II
- •Функциональная компартментализация ядра
- •Интерфазные хромосомы в ядре
- •Ядрышко
- •Пространственная организация синтеза мРнк
- •Ядерные тельца и домены
- •Компартментализованное ядро
- •Биосинтез белка рибосомами бактерий
- •Рибосомы
- •Этапы биосинтеза белка
- •Антибиотики, действующие на уровне трансляции
- •Трансляция у эукариот
- •Особенности первичной структуры эукариотических мРнк
- •Инициация биосинтеза белка эукариотическими рибосомами
- •Элонгация полипептидных цепей
- •Терминация трансляции
- •Трансляция в митохондриях
- •Трансляция в хлоропластах.
- •Основные пути регуляции экспрессии генов
- •Регуляция экспрессии генов на уровне транскрипции у прокариот
- •Регуляция на уровне инициации транскрипции
- •Регуляция синтеза рнк на уровне элонгации и терминации
- •Регуляция экспрессии генов на уровне транскрипции у эукариот
- •Передача сигнала и вторичные мессенджеры
- •Рецепторы мембран, осуществляющие трансмембранный перенос сигнала
- •Механизмы позитивной регуляции транскрипции
- •Классификация факторов транскрипции
- •Функциональные домены факторов транскрипции
- •Механизмы негативной регуляции транскрипции
- •Структура хроматина как специфический регулятор экспрессии генов
- •Импринтинг
- •Метилирование днк в регуляции транскрипции
- •Факторы транскрипции позвоночных, на активность которых оказывает влияние метилирование остатков цитозина в узнаваемых ими регуляторных последовательностях нуклеотидов
- •Посттранскрипционная регуляция экспрессии генов
- •Направленный транспорт, внутриклеточная локализация и депонирование мРнк
- •Сплайсинг рнк в регуляции экспрессии генов
- •Избирательная деградация мРнк
- •Регуляция экспрессии генов на уровне трансляции
- •Регуляция инициации трансляции
- •Регуляция элонгации синтеза полипептидных цепей
- •Регуляция терминации трансляции
- •Синтез белков, содержащих остатки селеноцистеина
- •Посттрансляционная регуляция экспрессии генов
- •Последствия фолдинга вновь синтезированных полипептидных цепей
- •Специфические протеиназы в посттрансляционном процессинге белков
- •Убиквитин-зависимая система протеолиза в регулируемой деградации белков
- •Сплайсинг белков
- •Другие посттрансляционные модификации белков
- •Воспроизведение генетической информации
- •Репликация днк
- •Белки, участвующие в репликации днк
- •Белки, входящие в состав репликативных комплексов прокариотических и эукариотических организмов
- •Репликативная вилка e. Coli и бактериофага t4
- •Особенности функционирования репликативной вилки эукариот
- •Эукариотические днк-полимеразы и их функциональные гомологи у прокариот
- •Регуляция репликации днк
- •Инициация репликации днк у e. Coli и ее регуляция
- •Регуляция репликации плазмиды ColE1
- •Особенности репликации линейных геномов
- •Линейные хромосомы бактерий
- •Репликаторы эукариот
- •Репликация теломерных участков эукариотических хромосом
- •Пространственная организация синтеза днк у эукариот
- •Защита генетической информации
- •Мутации
- •Основные источники мутаций и методы определения мутагенной активности
- •Основные классы алкилирующих агентов
- •Метаболиты нормальной микрофлоры человека, обладающие мутагенной и канцерогенной активностями
- •Sos-мутагенез у бактерий
- •Мутаторный фенотип
- •Экспансия днк
- •Адаптивные мутации
- •Механизмы защиты генома от мутаций
- •Репарация днк
- •Основные механизмы репарации поврежденной днк
- •Эксцизионная репарация в клетках животных
- •Днк-гликозилазы и эндонуклеазы клеток микроорганизмов и человека, участвующие в ber
- •Белки животных, участвующие в ner
- •Гомологичная рекомбинация в репарации днк
- •Репарация ошибочно спаренных нуклеотидов
- •Полимераза поли(adp-рибозы) в репарации днк у эукариот
- •Альтруистичная днк
- •Парадокс возможности существования многоклеточных организмов
- •Повышение информационной стабильности генома избыточными последовательностями
- •Селективная защита генов от мутаций
- •Высокоупорядоченное расположение летальных генов на хромосомах
- •Возможный смысл парадокса с
- •Современная концепция гена
- •Часть II основные направления развития прикладной молекулярной генетики Введение
- •Часть II. Искусственные генетические системы
- •Принципы генной инженерии
- •Основные ферменты, используемые в генной инженерии
- •Рестриктазы и днк-метилазы
- •Эффективность расщепления коротких последовательностей днк некоторыми распространенными рестриктазами
- •Днк- и рнк-лигазы
- •Ферменты матричного синтеза днк и рнк
- •Частота ошибок при синтезе днк, осуществляемом термостабильными днк-полимеразами in vitro при проведении пцр в оптимальных условиях
- •Другие ферменты
- •Векторы
- •Плазмидные векторы
- •Векторы на основе фага
- •Космиды и фазмиды
- •Сверхъемкие векторы yac, bac и pac
- •Интегрирующие и челночные (бинарные) векторы
- •Конструирование экспрессирующих векторов и их функционирование
- •Векторы для переноса днк в клетки животных и растений
- •Клонотеки генов
- •Получение клонотек генов
- •Введение рекомбинантных днк в клетки
- •Методы скрининга клонотек генов
- •Эукариотические системы экспрессии рекомбинантных генов, основанные на культурах клеток
- •Клетки яичников китайских хомячков (линия cho)
- •Клетки мышиной миеломы (линия Sp2/0)
- •Клетки селезенки мышей (линия mel)
- •Клетки африканской зеленой мартышки (линия cos)
- •Клетки насекомых, зараженные бакуловирусами
- •Сравнение эффективности рассмотренных систем экспрессии
- •Бесклеточные белоксинтезирующие системы
- •Прокариотические системы
- •Эукариотические системы
- •Проточные системы
- •Другие современные методы исследования генов
- •Рестрикционное картирование генов
- •"Прогулки и прыжки по хромосомам"
- •S1-картирование рнк и днк
- •Футпринтинг
- •Стратегия выделения нового гена
- •Направленный мутагенез и белковая инженерия
- •Методы направленного получения мутаций
- •Получение делеций и вставок
- •Химический мутагенез
- •Сайт-специфический мутагенез с использованием олигонуклеотидов
- •Полимеразная цепная реакция в направленном мутагенезе
- •Белковая инженерия
- •Библиотеки пептидов и эпитопов
- •Белки-репортеры в гибридных белках
- •Гибридные токсины
- •Подходы к созданию новых ферментов
- •Субтилигаза в лигировании пептидов
- •Концепция ксенобиоза
- •Антисмысловые рнк, рибозимы и дезоксирибозимы
- •Антисмысловые рнк и олигонуклеотиды
- •Механизм действия антисмысловых рнк
- •Использование антисмысловых рнк
- •Влияние экспрессии антисмысловых рнк на фенотип трансгенных мышей
- •Природные антисмысловые рнк
- •Антисмысловые рнк и патология: возможный механизм возникновения доминантных мутаций
- •Рибозимы и дезоксирибозимы
- •Типы рибозимов
- •Свойства рибозимов
- •Рибозимы как лекарственные средства
- •Репарация мутантных рнк с помощью рибозимов, осуществляющих транс-сплайсинг
- •Дезоксирибозимы
- •Аптамеры
- •Молекулы рнк у истоков жизни
- •Молекулы рнк в качестве рнк-репликаз
- •Возможность синтеза полипептидных цепей молекулами рнк
- •Трансгенные животные и растения
- •Способы получения трансгенных многоклеточных организмов
- •Экспрессия трансгенов
- •Использование трансгенов у животных
- •Исследование механизмов экспрессии генов
- •Токсигены в исследовании дифференцировки соматических клеток в онтогенезе
- •Изменение физиологического статуса лабораторных и сельскохозяйственных животных
- •Моделирование наследственных и приобретенных заболеваний человека
- •Трансгенные растения
- •Генотерапия наследственных и приобретенных заболеваний
- •Способы доставки новых генов в геном человека
- •Управление экспрессией трансгенов в клетках-мишенях
- •Современные достижения генотерапии онкологических заболеваний
- •Ближайшие перспективы использования генотерапии
- •Успехи генотерапии в модельных экспериментах
- •Проблемы, возникающие в связи с практическим применением генотерапии
- •Днк-диагностика и днк-типирование
- •Днк-диагностика наследственных и приобретенных заболеваний
- •Получение клинического генетического материала
- •Диагностика заболеваний
- •Днк-типирование
- •Днк-типирование микроорганизмов
- •Идентификация личности на основе минисателлитной днк: определение отцовства
- •Микроматрицы и микрочипы днк
- •Методы создания микроматриц днк
- •Ограничения в использовании микроматриц днк
- •Использование микроматриц днк в фундаментальных и прикладных исследованиях
- •Картирование и определение первичной структуры генома человека
- •Основные подходы к картированию генома человека
- •Генетические карты сцепления
- •Современные методы построения генетических карт сцепления
- •Пцр в исследованиях генома человека
- •Физические карты низкого разрешения
- •Физические карты высокого разрешения
- •Определение полной первичной структуры днк генома человека
- •Базы данных получаемой информации
- •Заключение
- •Рекомендуемая литература
Механизм прямой и обратной реакций аутосплайсинга интронов группы I
|
Аутосплайсинг |
Обратное лигирование |
|
GTPOH + [Экзон 1]upAИнтронGpa[Экзон 2] ↓
5’-концевого сайта сплайсинга ↓ [Экзон 1]uOH GpAИнтронGpa[Экзон 2]
↓ Лигирование экзонов ↓ [Экзон 1]upa[Экзон 2] + GpAИнтронG |
GTPOH + [Экзон 1]upAИнтронGpa[Экзон 2] ↑
интрона в прежнее место ↑ [Экзон 1]uOH GpAИнтронGpa[Экзон 2]
↑ Лигирование экзона 2 и интрона ↑ [Экзон 1]upa[Экзон 2] + GpAИнтронG |

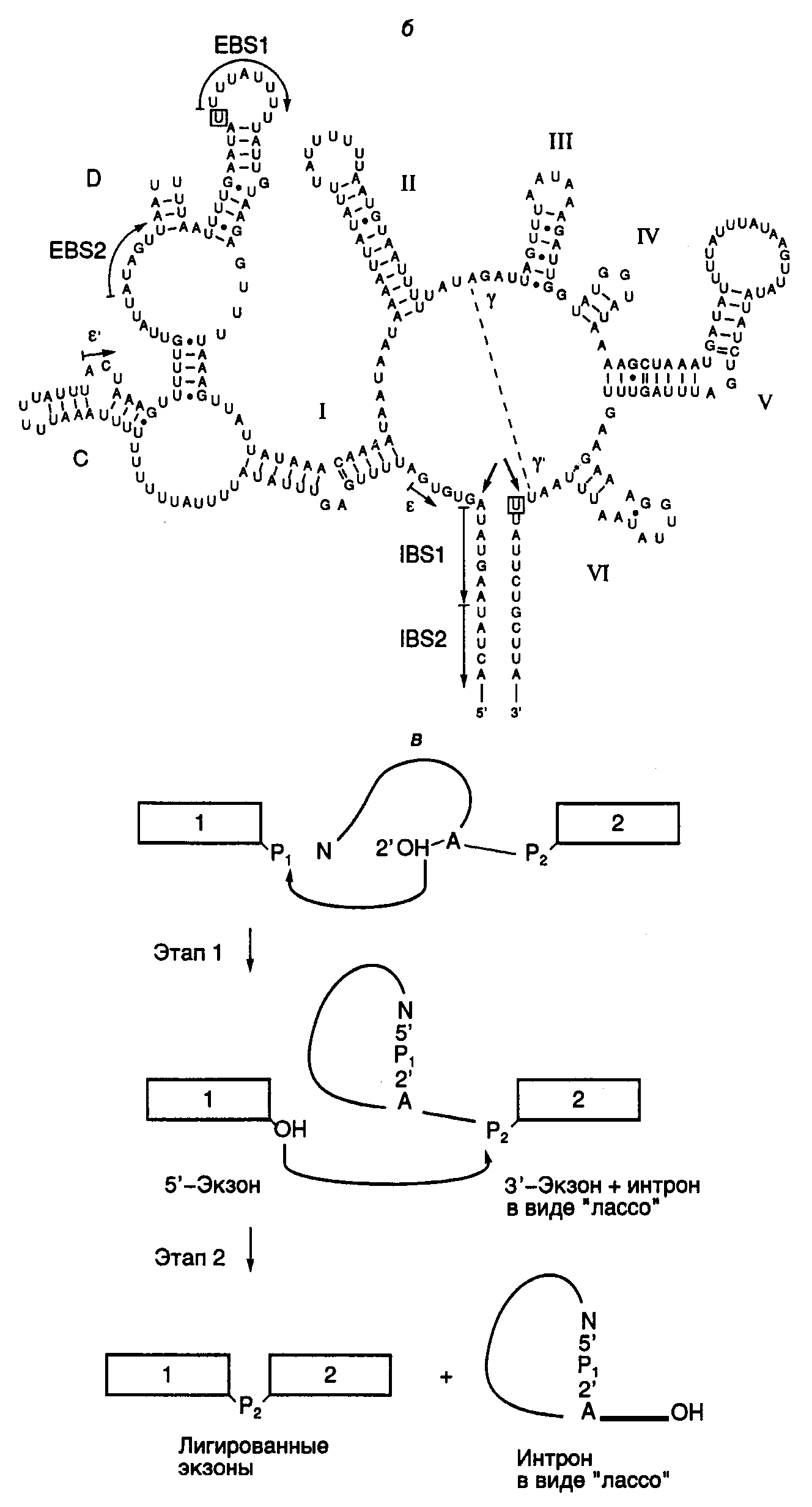
Рис. I.15. Структура интронов I-III групп и механизм аутосплайсинга
а– вторичные структуры типичных интронов типа I (Tetrahymena thermophila), II и III групп (Euglena gracilis). Стрелками обозначены 3- и 5-сайты сплайсинга, а также места интеграции твинтронов, пунктирными линиями – сайты интронов, сближенные в пространстве, EBS и IBS – соответственно сайты связывания экзонов и интронов;б– предполагаемая вторичная структура интрона группы II;в– двухэтапный механизм аутосплайсинга. Римскими цифрами обозначены предполагаемые двухцепочечные участки РНК, 1, 2 – экзоны
Строчными буквами в таблице изображены нуклеотиды, принадлежащие экзонам, а прописными – интронам. Прямая и обратная реакции не требуют белковых катализаторов. Однако в ряде случаев интроны I и II групп могут кодировать полипептид, названный матуразой (maturase, от англ. mature – созревать), который необходим для эффективного аутосплайсинга и транспозиции интронов in vivo.
Аутосплайсинг интронов группы I начинается с нуклеофильной атаки 2’-OH-группы GTP по фосфодиэфирной связи в 5’-концевом сайте сплайсинга (см. табл. I.10) (присутствие GTP в качестве кофактора необходимо для протекания данной реакции). При этом происходит освобождение 5’-концевого экзона 1. Образовавшиеся половинки молекулы удерживаются рядом друг с другом водородными связями. Освободившаяся 3’-OH-группа экзона 1 далее атакует фосфодиэфирную связь в 3’-концевом сайте сплайсинга, что сопровождается расщеплением этой связи и полным освобождением интрона. Одновременно происходит лигирование двух экзонов. Все этапы этой реакции обратимы. В обратной реакции после связывания соответствующего участка лигированных экзонов "активным центром" вырезанного интрона последний атакует своей концевой 3’-OH-группой фосфодиэфирную связь в месте стыковки экзонов, что сопровождается объединением интрона и экзона 2. На втором этапе 3’-OH-группа экзона 1 атакует фосфатную группу по первой фосфодиэфирной связи интрона, освобождая остаток G, с последующим объединением экзона 1 с остальной частью молекулы.
Аутосплайсинг интронов II и III групп протекает по другому механизму (см. рис. I.15,в). Реакция также осуществляется в два этапа. На первом этапе 2’-OH-группа аденозина, находящегося в точке разветвления интрона, вырезаемого из предшественника РНК, атакует фосфодиэфирную связь 5’-концевого сайта сплайсинга, что сопровождается освобождением экзона 1 и образованием промежуточной структуры в виде лассо. В таком промежуточном соединении 5’-концевой нуклеотид интрона соединен 2’–5’-фосфодиэфирной связью с этим остатком аденозина, образуя петлю на конце интрона. На втором этапе 3’-концевая OH-группа экзона 1 атакует 3’-концевой сайт сплайсинга. В результате происходит объединение экзонов и освобождается интрон с петлей на 5’-конце. В заключение следует отметить одно замечательное свойство этой группы реакций. Поскольку число фосфодиэфирных связей на протяжении всех преобразований остается неизменным, они не требуют затраты дополнительной энергии и протекают самопроизвольно.
Сплайсинг у ядерных пре-мРНК. Исследование механизмов сплайсинга у ядерных пре-мРНК показало, что они существенно не отличаются от только что рассмотренных механизмов, используемых для удаления интронов II и III групп, однако ряд различий имеется.
Структура интронов, удаляемых из предшественников РНК аутосплайсингом, высококонсервативна. У интронов ядерных РНК консервативны лишь короткие последовательности в окрестностях сайтов сплайсинга и точки разветвления. Вторая отличительная особенность сплайсинга у ядерных пре-мРНК – потребность в ATP и мяРНП, формирующих сплайсому. Тем не менее, одинаковые черты этих двух систем сплайсинга более существенны. Малые ядерные РНК, входящие в состав мяРНП и сплайсомы, участвуют в распознавании сайтов сплайсинга и точки разветвления, а также в правильном ориентировании экзонов по отношению друг к другу. Их OH-группы осуществляют атаку фосфодиэфирной связи 5’-концевого сайта сплайсинга на первом этапе реакции. Так же как и в случае интронов II и III групп, для вырезаемого интрона характерна структура типа лассо.
Распознавание канонических сайтов при сплайсинге ядерных пре-мРНК. Для полного прохождения всех реакций сплайсинга его аппарат (сплайсома) должен распознавать на пре-мРНК три критические последовательности нуклеотидов: 3’- и 5’-концевые сайты сплайсинга и точку разветвления. В соответствии с наиболее распространенной моделью поиска экзонов в пре-мРНК с большими интронами, аппарат сплайсинга, прежде всего, отыскивает два близкорасположенных сайта сплайсинга в нужной ориентации. Распознавание конкретной пары сайтов сплайсинга в пре-мРНК дрожжей начинается с взаимодействия по принципу комплементарности между последовательностями этих сайтов и 5’-концевыми участками мяРНК U1, входящих в состав U1-мяРНП-частиц в случае 5’-концевых сайтов сплайсинга, а также белка U2AF65, находящегося в комплексе с U2AF35, с последовательностью 3’-концевого сайта сплайсинга. Эффективность функционирования сайтов сплайсинга зависит от степени соответствия их первичной структуры консенсусным последовательностям.
Сближение двух сайтов сплайсинга, сопровождаемое выпетливанием последовательности интрона, осуществляется с участием SR-белков, обогащенных Ser и Arg, которые взаимодействуют с 70К-белком (70 кДа), входящим в состав U1-мяРНП-частицы, а также U2AF35 на другом конце интрона. Такие комплексы, образованные с участием SR-белков, получили название "коммитированных комплексов".
В то время как 5’-концевые сайты сплайсинга довольно консервативны, 3’-концевые сайты обнаруживают большую вариабельность. U1-мяРНП, находящиеся в комплексе с 5’-концевым сайтом сплайсинга, стимулируют присоединение белков U2AF к 3’-концевому сайту и способствуют правильному распознаванию соответствующего экзона в процессе, получившем название "определение экзона". Эффективное распознавание сайтов сплайсинга соответствующими белками является критическим этапом в правильном и упорядоченном удалении экзонов из пре-мРНК в процессе конститутивного сплайсинга.
Механизмы определения экзонов. Гены позвоночных, как правило, содержат большое число мелких экзонов (средняя длина 137 п.о.), разделенных протяженными последовательностями интронов, длина которых может превышать 100 т.п.о. При этом ферментные системы, осуществляющие сплайсинг, должны распознавать небольшие экзоны, затерянные среди гигантских некодирующих последовательностей, и осуществлять их правильное объединение друг с другом. Как уже упоминалось выше, канонические (консенсусные) последовательности, необходимые для распознавания экзонов, располагаются на концах интронов. Однако в отличие от соответствующих последовательностей интронов дрожжей регуляторные последовательности в окрестностях сайтов сплайсинга животных менее консервативны, и это, на первый взгляд, значительно усложняет задачу распознавания экзонов системами сплайсинга. В действительности распознавание индивидуальных сайтов сплайсинга у животных, по-видимому, не связано с независимым распознаванием канонических последовательностей в окрестностях каждого экзона. В соответствии с наиболее популярной в настоящее время моделью
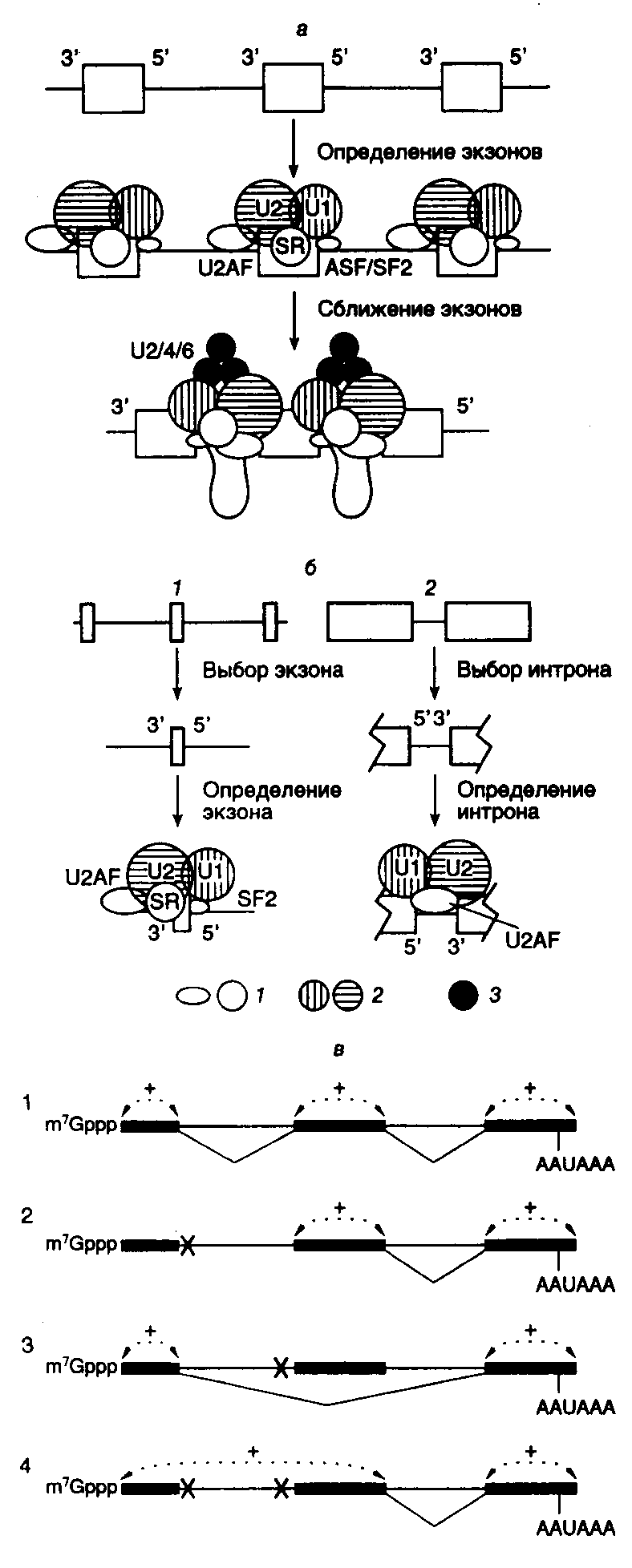
Рис. I.16. Механизм определения экзонов и интронов при сплайсинге ядерных пре-мРНК
а– определение экзонов;б– определение интронов у позвоночных (1) и низших эукариот (2),в –роль кэп-связывающего комплекса (CBC) в определении экзонов. Отмечены белки и РНК, участвующие в этом процессе в составе сплайсом: 1 – белки, 2 и 3 – мяРНП, X – мутации, инактивирующие сайты сплайсинга; + – взаимодействия, обеспечивающие распознавание экзонов; AAUAAA – поли(А)-сайт
определения экзонов у животных, взаимодействие между соседними сайтами сплайсинга в генах с короткими экзонами и длинными интронами происходит не через интроны, а через последовательности экзонов. Предполагается, что у пре-мРНК с длинными интронами система сплайсинга, прежде всего, отыскивает пару близкорасположенных сайтов сплайсинга, фланкирующих короткие последовательности экзонов (рис. I.16,а). После распознавания такой пары с ними взаимодействуют U1- и U2-мяРНП и ассоциированные факторы сплайсинга, включая факторы, распознающие 3’-концевые сайты сплайсинга – U2AF и SC35, а также фактор, узнающий 5’-концевой сайт сплайсинга – ASF/SF2. После завершения процесса определения экзона соседние экзоны входят в контакт друг с другом в результате взаимодействия между факторами, распознающими индивидуальные экзоны. Таким образом, в соответствии с этой моделью процесс сборки активной сплайсомы у позвоночных проходит в два этапа, включающие определение экзонов и их сближение между собой. В генах с небольшими интронами, например у низших эукариот, по-видимому, реализуется альтернативный механизм (см. рис. I.16,б). В этом случае первым этапом сборки сплайсомы является определение интрона.
В результате мутаций, связанных с нарушением сплайсинга, возникает, по крайней мере, четыре фенотипа: игнорирование экзона, который вырезается вместе с интронами; активация новых (криптических) сайтов сплайсинга; возникновение внутри интронов псевдоэкзонов, последовательности которых не вырезаются из пре-мРНК, и игнорирование интронов. Частоты этих мутаций составляют соответственно 51, 32, 11 и 6%. Все фенотипы, за исключением последнего, могут быть объяснены на основе обсуждаемой модели определения экзонов.
Эта же модель позволяет предсказывать максимальные и минимальные размеры экзонов в генах эукариот. Действительно, анализ длин 1600 внутренних экзонов показал, что только 3,5% из них содержат более 300 нуклеотидов и менее 1% – 400 нуклеотидов. Кроме того, доля экзонов, длина которых меньше 50 нуклеотидов, в этой выборке также незначительна. Известно, что в опытах in vitro сплайсинг резко ингибируется, если длина внутренних экзонов превышает 400 нуклеотидов или становится меньше 50 нуклеотидов. Все эти факты делают модель определения экзонов весьма правдоподобной. Более короткие экзоны, длина которых составляет 6 или 7 п.о., часто обнаруживаемые в генах белков мышц, распознаются системой сплайсинга через энхансерные регуляторные последовательности, расположенные в интронах рядом с экзонами. Механизм распознавания очень длинных экзонов остается неизвестным.

 Расщепление
Расщепление
 Интеграция
Интеграция