
- •Часть I. Механизмы хранения и реализации генетической информации 17
- •Предисловие автора
- •Часть I. Механизмы хранения и реализации генетической информации введение
- •Средний размер гаплоидного генома у некоторых групп организмов
- •Гены и хромосомы
- •Геном прокариот
- •Геном вирусов
- •Нуклеоид бактериальной клетки
- •Геном архебактерий
- •Минимальный размер генома одноклеточных организмов
- •Геном эукариот
- •Последовательности нуклеотидов эукариотического генома
- •Хроматин
- •Свойства гистонов животных
- •Роль днк-топоизомераз в обеспечении структуры и функционирования хроматина
- •Реализация генетической информации при экспрессии генов
- •Транскрипция
- •Днк-зависимые рнк-полимеразы
- •Характеристики белковых компонентов холофермента рнк-полимеразы II дрожжей
- •Единицы транскрипции (транскриптоны)
- •Этапы транскрипции
- •Субъединичный состав и характеристика основных факторов транскрипции (gtf) рнк-полимеразы II человека
- •Основные факторы элонгации рнк-полимеразы II
- •Хроматин во время транскрипции
- •Субъединичный состав и свойства белковых комплексов Swi/Snf и nurf
- •Котранскрипционные и посттранскрипционные модификации рнк
- •Процессинг рнк у бактерий
- •Редактирование пре-мРнк
- •Различные способы редактирования мРнк
- •Редактирование рнк у животных и их вирусов
- •Другие модификации эукариотических мРнк
- •Сравнение полиаденилирования мРнк у эукариот и прокариот
- •5’-Концевой сайт Точка 3’-Концевой сайт
- •5’–Экзон 1guaugu__...__uacuaac__...__(Py)nAgэкзон 2–3’
- •Механизм прямой и обратной реакций аутосплайсинга интронов группы I
- •Кэп-связывающий комплекс в роли фактора, сопрягающего основные реакции метаболизма транскриптов рнк-полимеразы II
- •Функциональная компартментализация ядра
- •Интерфазные хромосомы в ядре
- •Ядрышко
- •Пространственная организация синтеза мРнк
- •Ядерные тельца и домены
- •Компартментализованное ядро
- •Биосинтез белка рибосомами бактерий
- •Рибосомы
- •Этапы биосинтеза белка
- •Антибиотики, действующие на уровне трансляции
- •Трансляция у эукариот
- •Особенности первичной структуры эукариотических мРнк
- •Инициация биосинтеза белка эукариотическими рибосомами
- •Элонгация полипептидных цепей
- •Терминация трансляции
- •Трансляция в митохондриях
- •Трансляция в хлоропластах.
- •Основные пути регуляции экспрессии генов
- •Регуляция экспрессии генов на уровне транскрипции у прокариот
- •Регуляция на уровне инициации транскрипции
- •Регуляция синтеза рнк на уровне элонгации и терминации
- •Регуляция экспрессии генов на уровне транскрипции у эукариот
- •Передача сигнала и вторичные мессенджеры
- •Рецепторы мембран, осуществляющие трансмембранный перенос сигнала
- •Механизмы позитивной регуляции транскрипции
- •Классификация факторов транскрипции
- •Функциональные домены факторов транскрипции
- •Механизмы негативной регуляции транскрипции
- •Структура хроматина как специфический регулятор экспрессии генов
- •Импринтинг
- •Метилирование днк в регуляции транскрипции
- •Факторы транскрипции позвоночных, на активность которых оказывает влияние метилирование остатков цитозина в узнаваемых ими регуляторных последовательностях нуклеотидов
- •Посттранскрипционная регуляция экспрессии генов
- •Направленный транспорт, внутриклеточная локализация и депонирование мРнк
- •Сплайсинг рнк в регуляции экспрессии генов
- •Избирательная деградация мРнк
- •Регуляция экспрессии генов на уровне трансляции
- •Регуляция инициации трансляции
- •Регуляция элонгации синтеза полипептидных цепей
- •Регуляция терминации трансляции
- •Синтез белков, содержащих остатки селеноцистеина
- •Посттрансляционная регуляция экспрессии генов
- •Последствия фолдинга вновь синтезированных полипептидных цепей
- •Специфические протеиназы в посттрансляционном процессинге белков
- •Убиквитин-зависимая система протеолиза в регулируемой деградации белков
- •Сплайсинг белков
- •Другие посттрансляционные модификации белков
- •Воспроизведение генетической информации
- •Репликация днк
- •Белки, участвующие в репликации днк
- •Белки, входящие в состав репликативных комплексов прокариотических и эукариотических организмов
- •Репликативная вилка e. Coli и бактериофага t4
- •Особенности функционирования репликативной вилки эукариот
- •Эукариотические днк-полимеразы и их функциональные гомологи у прокариот
- •Регуляция репликации днк
- •Инициация репликации днк у e. Coli и ее регуляция
- •Регуляция репликации плазмиды ColE1
- •Особенности репликации линейных геномов
- •Линейные хромосомы бактерий
- •Репликаторы эукариот
- •Репликация теломерных участков эукариотических хромосом
- •Пространственная организация синтеза днк у эукариот
- •Защита генетической информации
- •Мутации
- •Основные источники мутаций и методы определения мутагенной активности
- •Основные классы алкилирующих агентов
- •Метаболиты нормальной микрофлоры человека, обладающие мутагенной и канцерогенной активностями
- •Sos-мутагенез у бактерий
- •Мутаторный фенотип
- •Экспансия днк
- •Адаптивные мутации
- •Механизмы защиты генома от мутаций
- •Репарация днк
- •Основные механизмы репарации поврежденной днк
- •Эксцизионная репарация в клетках животных
- •Днк-гликозилазы и эндонуклеазы клеток микроорганизмов и человека, участвующие в ber
- •Белки животных, участвующие в ner
- •Гомологичная рекомбинация в репарации днк
- •Репарация ошибочно спаренных нуклеотидов
- •Полимераза поли(adp-рибозы) в репарации днк у эукариот
- •Альтруистичная днк
- •Парадокс возможности существования многоклеточных организмов
- •Повышение информационной стабильности генома избыточными последовательностями
- •Селективная защита генов от мутаций
- •Высокоупорядоченное расположение летальных генов на хромосомах
- •Возможный смысл парадокса с
- •Современная концепция гена
- •Часть II основные направления развития прикладной молекулярной генетики Введение
- •Часть II. Искусственные генетические системы
- •Принципы генной инженерии
- •Основные ферменты, используемые в генной инженерии
- •Рестриктазы и днк-метилазы
- •Эффективность расщепления коротких последовательностей днк некоторыми распространенными рестриктазами
- •Днк- и рнк-лигазы
- •Ферменты матричного синтеза днк и рнк
- •Частота ошибок при синтезе днк, осуществляемом термостабильными днк-полимеразами in vitro при проведении пцр в оптимальных условиях
- •Другие ферменты
- •Векторы
- •Плазмидные векторы
- •Векторы на основе фага
- •Космиды и фазмиды
- •Сверхъемкие векторы yac, bac и pac
- •Интегрирующие и челночные (бинарные) векторы
- •Конструирование экспрессирующих векторов и их функционирование
- •Векторы для переноса днк в клетки животных и растений
- •Клонотеки генов
- •Получение клонотек генов
- •Введение рекомбинантных днк в клетки
- •Методы скрининга клонотек генов
- •Эукариотические системы экспрессии рекомбинантных генов, основанные на культурах клеток
- •Клетки яичников китайских хомячков (линия cho)
- •Клетки мышиной миеломы (линия Sp2/0)
- •Клетки селезенки мышей (линия mel)
- •Клетки африканской зеленой мартышки (линия cos)
- •Клетки насекомых, зараженные бакуловирусами
- •Сравнение эффективности рассмотренных систем экспрессии
- •Бесклеточные белоксинтезирующие системы
- •Прокариотические системы
- •Эукариотические системы
- •Проточные системы
- •Другие современные методы исследования генов
- •Рестрикционное картирование генов
- •"Прогулки и прыжки по хромосомам"
- •S1-картирование рнк и днк
- •Футпринтинг
- •Стратегия выделения нового гена
- •Направленный мутагенез и белковая инженерия
- •Методы направленного получения мутаций
- •Получение делеций и вставок
- •Химический мутагенез
- •Сайт-специфический мутагенез с использованием олигонуклеотидов
- •Полимеразная цепная реакция в направленном мутагенезе
- •Белковая инженерия
- •Библиотеки пептидов и эпитопов
- •Белки-репортеры в гибридных белках
- •Гибридные токсины
- •Подходы к созданию новых ферментов
- •Субтилигаза в лигировании пептидов
- •Концепция ксенобиоза
- •Антисмысловые рнк, рибозимы и дезоксирибозимы
- •Антисмысловые рнк и олигонуклеотиды
- •Механизм действия антисмысловых рнк
- •Использование антисмысловых рнк
- •Влияние экспрессии антисмысловых рнк на фенотип трансгенных мышей
- •Природные антисмысловые рнк
- •Антисмысловые рнк и патология: возможный механизм возникновения доминантных мутаций
- •Рибозимы и дезоксирибозимы
- •Типы рибозимов
- •Свойства рибозимов
- •Рибозимы как лекарственные средства
- •Репарация мутантных рнк с помощью рибозимов, осуществляющих транс-сплайсинг
- •Дезоксирибозимы
- •Аптамеры
- •Молекулы рнк у истоков жизни
- •Молекулы рнк в качестве рнк-репликаз
- •Возможность синтеза полипептидных цепей молекулами рнк
- •Трансгенные животные и растения
- •Способы получения трансгенных многоклеточных организмов
- •Экспрессия трансгенов
- •Использование трансгенов у животных
- •Исследование механизмов экспрессии генов
- •Токсигены в исследовании дифференцировки соматических клеток в онтогенезе
- •Изменение физиологического статуса лабораторных и сельскохозяйственных животных
- •Моделирование наследственных и приобретенных заболеваний человека
- •Трансгенные растения
- •Генотерапия наследственных и приобретенных заболеваний
- •Способы доставки новых генов в геном человека
- •Управление экспрессией трансгенов в клетках-мишенях
- •Современные достижения генотерапии онкологических заболеваний
- •Ближайшие перспективы использования генотерапии
- •Успехи генотерапии в модельных экспериментах
- •Проблемы, возникающие в связи с практическим применением генотерапии
- •Днк-диагностика и днк-типирование
- •Днк-диагностика наследственных и приобретенных заболеваний
- •Получение клинического генетического материала
- •Диагностика заболеваний
- •Днк-типирование
- •Днк-типирование микроорганизмов
- •Идентификация личности на основе минисателлитной днк: определение отцовства
- •Микроматрицы и микрочипы днк
- •Методы создания микроматриц днк
- •Ограничения в использовании микроматриц днк
- •Использование микроматриц днк в фундаментальных и прикладных исследованиях
- •Картирование и определение первичной структуры генома человека
- •Основные подходы к картированию генома человека
- •Генетические карты сцепления
- •Современные методы построения генетических карт сцепления
- •Пцр в исследованиях генома человека
- •Физические карты низкого разрешения
- •Физические карты высокого разрешения
- •Определение полной первичной структуры днк генома человека
- •Базы данных получаемой информации
- •Заключение
- •Рекомендуемая литература
Хроматин
Хроматином называют сложную смесь веществ, из которых построены хромосомы эукариот. Основными компонентами хроматина являются ДНК, гистоны и негистоновые белки, образующие высокоупорядоченные в пространстве структуры. Соотношение ДНК и белка в хроматине составляет ~1:1, а основная масса белка хроматина представлена гистонами. Гистоны образуют семейство высококонсервативных основных белков, которые разделяются на пять больших классов, названных H1, H2A, H2B, H3 и H4. Размер полипептидных цепей гистонов лежит в пределах ~220 (H1) и 102 (H4) аминокислотных остатков. Гистон H1 сильно обогащен остатками Lys, для гистонов H2A и H2B характерно умеренное содержание Lys, полипептидные цепи гистонов H3 и H4 богаты Arg. Внутри каждого класса гистонов (за исключением H4) на основании аминокислотных последовательностей различают несколько субтипов этих белков. Такая множественность особенно характерна для гистонов класса H1 млекопитающих. В этом случае различают семь субтипов, названных H1.1–H1.5, H1o и H1t.
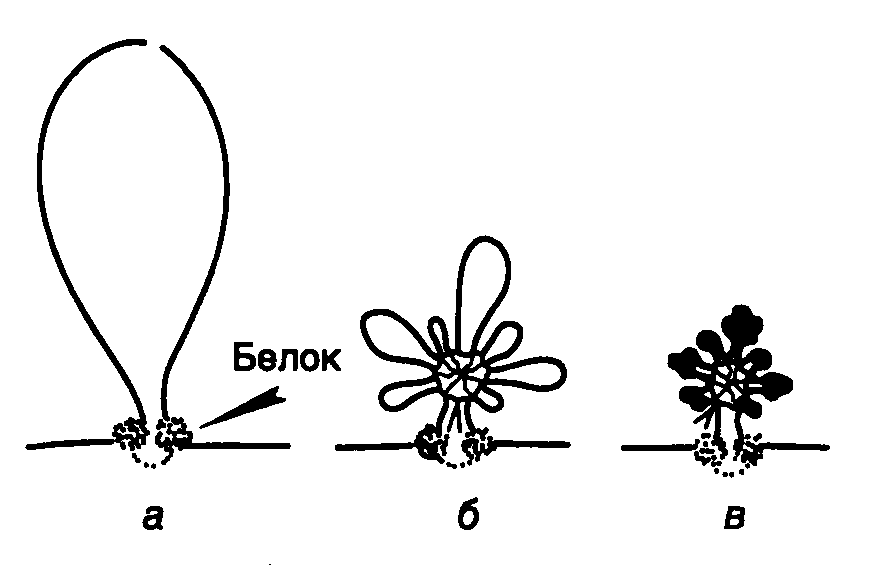
Рис. I.2. Схематическое изображение петельно-доменного уровня компактизации хроматина
а– фиксация петли хромомера на ядерном матриксе с помощью MAR/SAR-последовательностей и белков;б– "розетки", образованные из петли хромомера;в– конденсация петель "розеток" с участием нуклеосом и нуклеомеров
Важным результатом взаимодействия ДНК с белками в составе хроматина является ее компактизация. Суммарная длина ДНК, заключенной в ядре клеток человека, приближается к 1 м, тогда как средний диаметр ядра составляет 10 мкм. Длина молекулы ДНК, заключенной в одной хромосоме человека, в среднем равняется ~4 см. В то же время длина метафазной хромосомы составляет ~4 мкм. Следовательно, ДНК метафазных хромосом человека компактизована по длине, по крайней мере, в 104 раз. Степень компактизации ДНК в интерфазных ядрах значительно ниже и неравномерна в отдельных генетических локусах. С функциональной точки зрения различают эухроматин и гетерохроматин. Эухроматин характеризуется меньшей по сравнению с гетерохроматином компактизацией ДНК, и в нем главным образом локализуются активно экспрессирующиеся гены. В настоящее время широко распространено мнение о генетической инертности гетерохроматина. Поскольку его истинные функции сегодня нельзя считать установленными, эта точка зрения по мере накопления знаний о гетерохроматине может измениться. Уже сейчас в нем находят активно экспрессирующиеся гены.
Гетерохроматизация определенных участков хромосом часто сопровождается подавлением транскрипции имеющихся в них генов. В процесс гетерохроматизации могут быть вовлечены протяженные участки хромосом и даже целые хромосомы. В соответствии с этим считается, что регуляция транскрипции генов эукариот в основном происходит на двух уровнях. На первом из них компактизация или декомпактизация ДНК в хроматине может приводить к длительной инактивации или активации протяженных участков хромосом или даже целых хромосом в онтогенезе организма. Более тонкая регуляция транскрипции активированных участков хромосом достигается на втором уровне при участии негистоновых белков, включающих многочисленные факторы транскрипции.
Структурная организация хроматина и хромосом эукариот. Вопрос о структурной организации хроматина в интерфазных ядрах в настоящее время далек от своего разрешения. Это связано, прежде всего, со сложностью и динамичностью его структуры, которая легко меняется даже при незначительных экзогенных воздействиях. Большинство знаний о структуре хроматина было получено in vitro на препаратах фрагментированного хроматина, структура которого значительно отличается от таковой в нативных ядрах. В соответствии с распространенной точкой зрения различают три уровня структурной организации хроматина у эукариот: 1) нуклеосомная фибрилла; 2) соленоид, или нуклеомер; 3) петельно-доменная структура, включающая хромомеры.
Нуклеосомные фибриллы. В определенных условиях (при низкой ионной силе и в присутствии двухвалентных ионов металлов) в изолированном хроматине удается наблюдать регулярные структуры в виде протяженных фибрилл диаметром 10 нм, состоящих из нуклеосом. Эти фибриллярные структуры, в которых нуклеосомы расположены как бусы на нитке, рассматриваются в качестве низшего уровня упаковки ДНК эукариот в хроматине. Нуклеосомы, входящие в состав фибрилл, расположены более или менее равномерно вдоль молекулы ДНК на расстоянии 10–20 нм друг от друга. В состав нуклеосом входят четыре пары молекул гистонов: H2a, H2b, H3 и H4, а также одна молекула гистона H1. Данные по структуре нуклеосом в основном получены с использованием трех методов: рентгеноструктурного анализа низкого и высокого разрешения кристаллов нуклеосом, межмолекулярных сшивок белок–ДНК и расщепления ДНК в составе нуклеосом с помощью нуклеаз или радикалов гидроксила. На основании таких данных А. Клугом была построена модель нуклеосомы, в соответствии с которой ДНК (146 п.о.) в B-форме (правозакрученная спираль с шагом 10 п.о.) намотана на гистоновый октамер, в центральной части которого расположены гистоны Н3 и Н4, а на периферии – Н2а и Н2b. Диаметр такого нуклеосомного диска составляет 11 нм, а его толщина – 5,5 нм. Структура, состоящая из гистонового октамера и намотанной на него ДНК, получила название нуклеосомной кóровой частицы. Кóровые частицы отделены друг от друга сегментами линкерной ДНК. Общая длина участка ДНК, включенного в нуклеосому животных, составляет 200 (15) п.о.
Полипептидные цепи гистонов содержат структурные домены нескольких типов. Центральный глобулярный домен и гибкие выступающие N- и С-концевые участки, обогащенные основными аминокислотами, получили название плеч (arm). С-концевые домены полипептидных цепей, участвующие в гистон–гистоновых взаимодействиях внутри кóровой частицы, находятся преимущественно в виде -спирали с протяженным центральным спиральным участком, вдоль которого с двух сторон уложено по одной более короткой спирали. Все известные места обратимых посттрансляционных модификаций гистонов, происходящих на протяжении клеточного цикла или во время дифференцировки клеток, локализованы в гибких основных доменах их полипептидных цепей (табл. I.2). При этом N-концевые плечи гистонов H3 и H4 являются самыми консервативными участками молекул, а гистоны в целом – одними из наиболее эволюционно консервативных белков. С помощью генетических исследований дрожжей S. cerevisiae было установлено, что небольшие делеции и точковые мутации в N-концевых частях генов гистонов сопровождаются глубокими и разнообразными изменениями фенотипа дрожжевых клеток. Это указывает на чрезвычайную важность целостности молекул гистонов в обеспечении правильного функционирования эукариотических генов.
В растворе гистоны Н3 и Н4 могут существовать в виде стабильных тетрамеров (Н3)2(Н4)2, а гистоны Н2А и Н2В – в виде стабильных димеров. Постепенное повышение ионной силы в растворах, содержащих нативный хроматин, приводит к освобождению сначала димеров Н2А/Н2В, а затем тетрамеров Н3/Н4.
Дальнейшее уточнение тонкой структуры нуклеосом в кристаллах было проведено недавно в работе К. Люгера с соавт. (1997 г.) с помощью рентгеноструктурного анализа высокого разрешения. Было установлено, что выпуклая поверхность каждого гистонового гетеродимера в составе октамера огибается сегментами ДНК длиной 27–28 п.о., расположенными по отношению друг к другу под углом 140о, которые разделены линкерными участками длиной в 4 п.о.
В соответствии с современными данными пространственная структура ДНК в составе кóровых частиц несколько отличается от B-формы: двойная спираль ДНК перекручена на 0,25–0,35 п.о./виток двойной спирали, что приводит к образованию шага спирали, равному 10,2 п.о./виток (у В-формы в растворе – 10,5 п.о./виток). Стабильность комплекса гистонов в составе кóровой частицы определяется взаимодействием их глобулярных частей, поэтому удаление гибких плеч в условиях мягкого протеолиза не сопровождается разрушением комплекса. N-концевые плечи гистонов, по-видимому, обеспечивают их взаимодействие со специфическими участками ДНК. Так, N-концевые домены гистона Н3 контактируют с участками ДНК на входе в кóровую частицу и выходе из нее, тогда как соответствующий домен гистона Н4 связывается с внутренней частью ДНК нуклеосомы.
Упомянутые выше исследования структуры нуклеосом высокого разрешения показывают, что центральная часть сегмента ДНК длиной в 121 п.о. в составе нуклеосомы образует дополнительные контакты с гистоном H3. При этом N-концевые части полипептидных цепей гистонов H3 и H2B проходят через каналы, образуемые малыми бороздками соседних супервитков ДНК нуклеосомы, а N-концевая часть гистона H2A контактирует с малой бороздкой внешней части супервитка ДНК. В совокупности данные высокого разрешения показывают, что ДНК в составе коровых частиц нуклеосом огибает гистоновые октамеры неравномерно. Кривизна нарушается в местах взаимодействия ДНК с поверхностью гистонов, и такие изломы наиболее заметны на расстоянии 10–15 и 40 п.о. от центра супервитка ДНК.
Таблица I.2
