- •Часть I. Механизмы хранения и реализации генетической информации 17
- •Предисловие автора
- •Часть I. Механизмы хранения и реализации генетической информации введение
- •Средний размер гаплоидного генома у некоторых групп организмов
- •Гены и хромосомы
- •Геном прокариот
- •Геном вирусов
- •Нуклеоид бактериальной клетки
- •Геном архебактерий
- •Минимальный размер генома одноклеточных организмов
- •Геном эукариот
- •Последовательности нуклеотидов эукариотического генома
- •Хроматин
- •Свойства гистонов животных
- •Роль днк-топоизомераз в обеспечении структуры и функционирования хроматина
- •Реализация генетической информации при экспрессии генов
- •Транскрипция
- •Днк-зависимые рнк-полимеразы
- •Характеристики белковых компонентов холофермента рнк-полимеразы II дрожжей
- •Единицы транскрипции (транскриптоны)
- •Этапы транскрипции
- •Субъединичный состав и характеристика основных факторов транскрипции (gtf) рнк-полимеразы II человека
- •Основные факторы элонгации рнк-полимеразы II
- •Хроматин во время транскрипции
- •Субъединичный состав и свойства белковых комплексов Swi/Snf и nurf
- •Котранскрипционные и посттранскрипционные модификации рнк
- •Процессинг рнк у бактерий
- •Редактирование пре-мРнк
- •Различные способы редактирования мРнк
- •Редактирование рнк у животных и их вирусов
- •Другие модификации эукариотических мРнк
- •Сравнение полиаденилирования мРнк у эукариот и прокариот
- •5’-Концевой сайт Точка 3’-Концевой сайт
- •5’–Экзон 1guaugu__...__uacuaac__...__(Py)nAgэкзон 2–3’
- •Механизм прямой и обратной реакций аутосплайсинга интронов группы I
- •Кэп-связывающий комплекс в роли фактора, сопрягающего основные реакции метаболизма транскриптов рнк-полимеразы II
- •Функциональная компартментализация ядра
- •Интерфазные хромосомы в ядре
- •Ядрышко
- •Пространственная организация синтеза мРнк
- •Ядерные тельца и домены
- •Компартментализованное ядро
- •Биосинтез белка рибосомами бактерий
- •Рибосомы
- •Этапы биосинтеза белка
- •Антибиотики, действующие на уровне трансляции
- •Трансляция у эукариот
- •Особенности первичной структуры эукариотических мРнк
- •Инициация биосинтеза белка эукариотическими рибосомами
- •Элонгация полипептидных цепей
- •Терминация трансляции
- •Трансляция в митохондриях
- •Трансляция в хлоропластах.
- •Основные пути регуляции экспрессии генов
- •Регуляция экспрессии генов на уровне транскрипции у прокариот
- •Регуляция на уровне инициации транскрипции
- •Регуляция синтеза рнк на уровне элонгации и терминации
- •Регуляция экспрессии генов на уровне транскрипции у эукариот
- •Передача сигнала и вторичные мессенджеры
- •Рецепторы мембран, осуществляющие трансмембранный перенос сигнала
- •Механизмы позитивной регуляции транскрипции
- •Классификация факторов транскрипции
- •Функциональные домены факторов транскрипции
- •Механизмы негативной регуляции транскрипции
- •Структура хроматина как специфический регулятор экспрессии генов
- •Импринтинг
- •Метилирование днк в регуляции транскрипции
- •Факторы транскрипции позвоночных, на активность которых оказывает влияние метилирование остатков цитозина в узнаваемых ими регуляторных последовательностях нуклеотидов
- •Посттранскрипционная регуляция экспрессии генов
- •Направленный транспорт, внутриклеточная локализация и депонирование мРнк
- •Сплайсинг рнк в регуляции экспрессии генов
- •Избирательная деградация мРнк
- •Регуляция экспрессии генов на уровне трансляции
- •Регуляция инициации трансляции
- •Регуляция элонгации синтеза полипептидных цепей
- •Регуляция терминации трансляции
- •Синтез белков, содержащих остатки селеноцистеина
- •Посттрансляционная регуляция экспрессии генов
- •Последствия фолдинга вновь синтезированных полипептидных цепей
- •Специфические протеиназы в посттрансляционном процессинге белков
- •Убиквитин-зависимая система протеолиза в регулируемой деградации белков
- •Сплайсинг белков
- •Другие посттрансляционные модификации белков
- •Воспроизведение генетической информации
- •Репликация днк
- •Белки, участвующие в репликации днк
- •Белки, входящие в состав репликативных комплексов прокариотических и эукариотических организмов
- •Репликативная вилка e. Coli и бактериофага t4
- •Особенности функционирования репликативной вилки эукариот
- •Эукариотические днк-полимеразы и их функциональные гомологи у прокариот
- •Регуляция репликации днк
- •Инициация репликации днк у e. Coli и ее регуляция
- •Регуляция репликации плазмиды ColE1
- •Особенности репликации линейных геномов
- •Линейные хромосомы бактерий
- •Репликаторы эукариот
- •Репликация теломерных участков эукариотических хромосом
- •Пространственная организация синтеза днк у эукариот
- •Защита генетической информации
- •Мутации
- •Основные источники мутаций и методы определения мутагенной активности
- •Основные классы алкилирующих агентов
- •Метаболиты нормальной микрофлоры человека, обладающие мутагенной и канцерогенной активностями
- •Sos-мутагенез у бактерий
- •Мутаторный фенотип
- •Экспансия днк
- •Адаптивные мутации
- •Механизмы защиты генома от мутаций
- •Репарация днк
- •Основные механизмы репарации поврежденной днк
- •Эксцизионная репарация в клетках животных
- •Днк-гликозилазы и эндонуклеазы клеток микроорганизмов и человека, участвующие в ber
- •Белки животных, участвующие в ner
- •Гомологичная рекомбинация в репарации днк
- •Репарация ошибочно спаренных нуклеотидов
- •Полимераза поли(adp-рибозы) в репарации днк у эукариот
- •Альтруистичная днк
- •Парадокс возможности существования многоклеточных организмов
- •Повышение информационной стабильности генома избыточными последовательностями
- •Селективная защита генов от мутаций
- •Высокоупорядоченное расположение летальных генов на хромосомах
- •Возможный смысл парадокса с
- •Современная концепция гена
- •Часть II основные направления развития прикладной молекулярной генетики Введение
- •Часть II. Искусственные генетические системы
- •Принципы генной инженерии
- •Основные ферменты, используемые в генной инженерии
- •Рестриктазы и днк-метилазы
- •Эффективность расщепления коротких последовательностей днк некоторыми распространенными рестриктазами
- •Днк- и рнк-лигазы
- •Ферменты матричного синтеза днк и рнк
- •Частота ошибок при синтезе днк, осуществляемом термостабильными днк-полимеразами in vitro при проведении пцр в оптимальных условиях
- •Другие ферменты
- •Векторы
- •Плазмидные векторы
- •Векторы на основе фага
- •Космиды и фазмиды
- •Сверхъемкие векторы yac, bac и pac
- •Интегрирующие и челночные (бинарные) векторы
- •Конструирование экспрессирующих векторов и их функционирование
- •Векторы для переноса днк в клетки животных и растений
- •Клонотеки генов
- •Получение клонотек генов
- •Введение рекомбинантных днк в клетки
- •Методы скрининга клонотек генов
- •Эукариотические системы экспрессии рекомбинантных генов, основанные на культурах клеток
- •Клетки яичников китайских хомячков (линия cho)
- •Клетки мышиной миеломы (линия Sp2/0)
- •Клетки селезенки мышей (линия mel)
- •Клетки африканской зеленой мартышки (линия cos)
- •Клетки насекомых, зараженные бакуловирусами
- •Сравнение эффективности рассмотренных систем экспрессии
- •Бесклеточные белоксинтезирующие системы
- •Прокариотические системы
- •Эукариотические системы
- •Проточные системы
- •Другие современные методы исследования генов
- •Рестрикционное картирование генов
- •"Прогулки и прыжки по хромосомам"
- •S1-картирование рнк и днк
- •Футпринтинг
- •Стратегия выделения нового гена
- •Направленный мутагенез и белковая инженерия
- •Методы направленного получения мутаций
- •Получение делеций и вставок
- •Химический мутагенез
- •Сайт-специфический мутагенез с использованием олигонуклеотидов
- •Полимеразная цепная реакция в направленном мутагенезе
- •Белковая инженерия
- •Библиотеки пептидов и эпитопов
- •Белки-репортеры в гибридных белках
- •Гибридные токсины
- •Подходы к созданию новых ферментов
- •Субтилигаза в лигировании пептидов
- •Концепция ксенобиоза
- •Антисмысловые рнк, рибозимы и дезоксирибозимы
- •Антисмысловые рнк и олигонуклеотиды
- •Механизм действия антисмысловых рнк
- •Использование антисмысловых рнк
- •Влияние экспрессии антисмысловых рнк на фенотип трансгенных мышей
- •Природные антисмысловые рнк
- •Антисмысловые рнк и патология: возможный механизм возникновения доминантных мутаций
- •Рибозимы и дезоксирибозимы
- •Типы рибозимов
- •Свойства рибозимов
- •Рибозимы как лекарственные средства
- •Репарация мутантных рнк с помощью рибозимов, осуществляющих транс-сплайсинг
- •Дезоксирибозимы
- •Аптамеры
- •Молекулы рнк у истоков жизни
- •Молекулы рнк в качестве рнк-репликаз
- •Возможность синтеза полипептидных цепей молекулами рнк
- •Трансгенные животные и растения
- •Способы получения трансгенных многоклеточных организмов
- •Экспрессия трансгенов
- •Использование трансгенов у животных
- •Исследование механизмов экспрессии генов
- •Токсигены в исследовании дифференцировки соматических клеток в онтогенезе
- •Изменение физиологического статуса лабораторных и сельскохозяйственных животных
- •Моделирование наследственных и приобретенных заболеваний человека
- •Трансгенные растения
- •Генотерапия наследственных и приобретенных заболеваний
- •Способы доставки новых генов в геном человека
- •Управление экспрессией трансгенов в клетках-мишенях
- •Современные достижения генотерапии онкологических заболеваний
- •Ближайшие перспективы использования генотерапии
- •Успехи генотерапии в модельных экспериментах
- •Проблемы, возникающие в связи с практическим применением генотерапии
- •Днк-диагностика и днк-типирование
- •Днк-диагностика наследственных и приобретенных заболеваний
- •Получение клинического генетического материала
- •Диагностика заболеваний
- •Днк-типирование
- •Днк-типирование микроорганизмов
- •Идентификация личности на основе минисателлитной днк: определение отцовства
- •Микроматрицы и микрочипы днк
- •Методы создания микроматриц днк
- •Ограничения в использовании микроматриц днк
- •Использование микроматриц днк в фундаментальных и прикладных исследованиях
- •Картирование и определение первичной структуры генома человека
- •Основные подходы к картированию генома человека
- •Генетические карты сцепления
- •Современные методы построения генетических карт сцепления
- •Пцр в исследованиях генома человека
- •Физические карты низкого разрешения
- •Физические карты высокого разрешения
- •Определение полной первичной структуры днк генома человека
- •Базы данных получаемой информации
- •Заключение
- •Рекомендуемая литература
Основные классы алкилирующих агентов
|
Класс |
Представитель |
Структурная формула |
|
Иприты сернистые |
Иприт |
S(CH2CH2Cl)2 |
|
азотистые |
Азотистый иприт |
HN(CH2CH2Cl)2 |
|
Эпоксиды |
Этиленоксид |
|
|
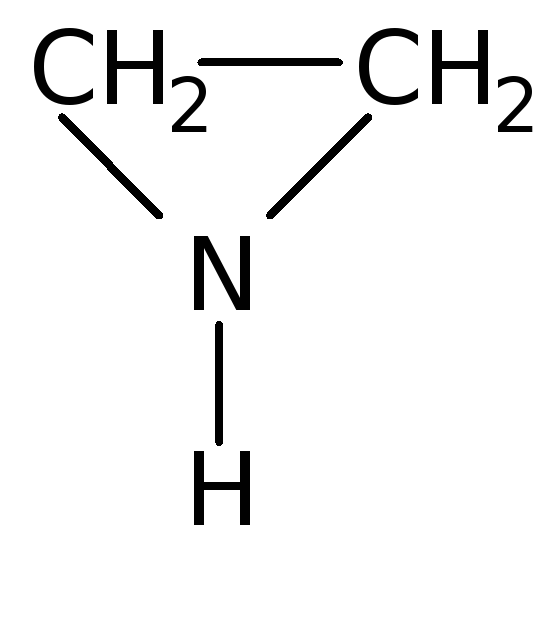
Этиленимины |
Этиленимин
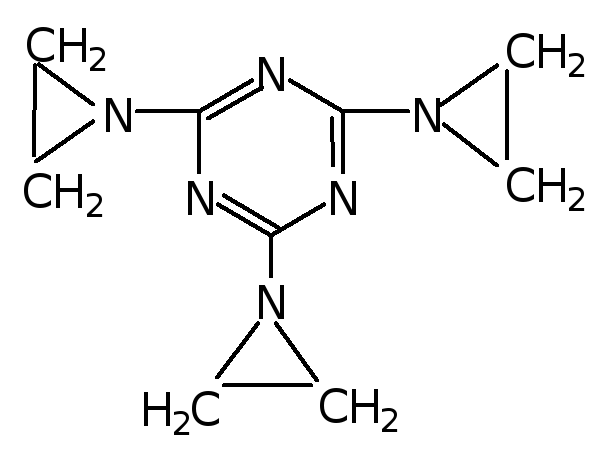
Триэтиленмеламин |
|
|
Алкилалкансульфонаты |
Этилметансульфонат |
C2H5OSO2CH3 |
|
|
Метилметансульфонат |
CH3OSO2CH3 |
|
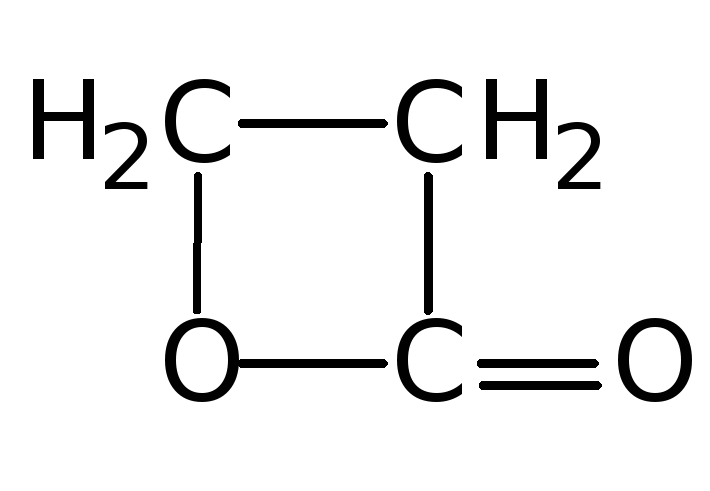
-Лактоны |
-Пропиолактон |
|
|
Диазосоединения |
Диазометан |
CH2N ═ N |
|
Нитрозосоединения |
N-Нитрозо-N-метилуретан
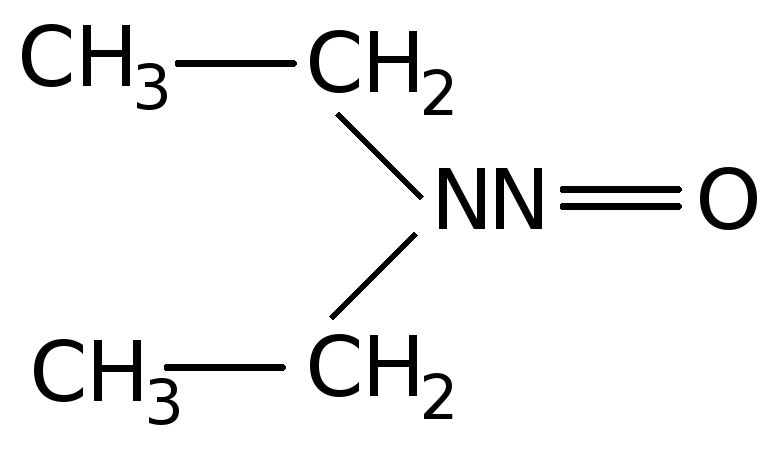
Диэтилнитрозамин
N-Метил-N-нитро-N-нитрозогуанидин |
CH3N(NO)C(=NH)NHNO2 |
Алкилирование является одной из возможных химических модификаций нуклеотидов ДНК in vivo под действием экзогенных мутагенов. Число известных химических веществ, способных вызывать модификации нуклеотидов ДНК по другим механизмам, быстро возрастает с расширением исследований в этой области. Среди таких мутагенов следует упомянуть азотистую кислоту, которая образуется из нитритов (NaNO2 и KNO2) в водных растворах при низких значениях pH. Азотистая кислота дезаминирует гуанин до ксантина, аденин до гипоксантина, а цитозин до урацила. В ДНК спаривание урацила с аденином приводит к транзициям GCAT, гипоксантин вызывает обратную транзицию ATGC, ксантин же не спаривается ни с одним из пиримидинов ДНК, и его включение оказывается летальным для клетки. Мутагенным действием обладают различные органические перекиси. Сама перекись водорода не оказывает мутагенного эффекта, но становится сильным мутагеном в сочетании с формальдегидом или ацетоном, у которых индуцирует образование свободных радикалов. Азид натрия – мощный ингибитор дыхания, также в ряде случаев обладает мутагенным действием, что связывают с накоплением в процессе метаболизма мутагенных перекисей. Перекиси индуцируют мутации и разрывы хромосом, имитируя мутагенное действие рентгеновских лучей, которые индуцируют образование различных реакционноспособных радикалов. И, наконец, среди химических мутагенов необходимо упомянуть аналоги нуклеозидов и оснований: 5-бромдезоксиуридин и 2-аминопурин, являющиеся сильными мутагенами. Спаривание с аденином 5-бромдезоксиуридина, обычно включающегося в ДНК вместо цитозина, приводит к образованию транзиций GCAT. Обратные транзиции ATGC возникают под действием 2-аминопурина.
Красители, обладающие способностью интеркалировать между основаниями ДНК, вызывают мутации со сдвигом рамки считывания. К таким красителям, в частности относятся хорошо известные бромистый этидий и производные акридина.
Промутагены, проканцерогены и их метаболическая активация. Рассмотренные выше химические соединения изначально обладают мутагенной активностью и для ее проявления не требуют каких-либо дополнительных модификаций. Однако существует множество химических соединений, которые сами по себе не проявляют мутагенную активность, но приобретают ее после серии биохимических превращений внутри организма под действием его ферментных систем. Такие химические соединения получили название промутагенов, а процесс их ферментативного превращения в мутагены – метаболической активации.
Любой организм в течение жизни подвергается непрерывной атаке экзогенными чужеродными химическими соединениями – ксенобиотиками, для защиты от накопления которых у него имеются эффективные ферментативные механизмы. Процесс метаболизма ксенобиотиков в организме традиционно разделяют на две фазы. Поскольку многие опасные для здоровья ксенобиотики гидрофобны и имеют тенденцию к накоплению в липидах клеточных мембран, обе фазы их внутриклеточного метаболизма связаны, прежде всего, с введением в их молекулы гидрофильных химических групп. Последующее повышение растворимости этих соединений в биологических жидкостях облегчает их выведение из организма. Таким образом, во время первой фазы метаболизма ксенобиотиков происходит ферментативное введение в их молекулы небольших полярных групп (например гидроксильных), что делает молекулы ксенобиотиков более водорастворимыми. С другой стороны, такие реакции подготавливают молекулы ксенобиотиков для вступления во вторую фазу метаболизма, во время которой происходит конъюгация преобразованных в первой фазе молекул ксенобиотиков с еще более полярными химическими группировками, в частности с остатками глюкуроновой кислоты, сульфатов или глицина.
Среди ферментов, принимающих участие в первой фазе метаболизма ксенобиотиков, наиболее хорошо изученными являются цитохромы группы Р-450. Эти ферменты в организме представлены большим числом (>20) изоформ, каждая из которых, как правило, обладает широкой субстратной специфичностью, а все вместе они способны метаболизировать множество экзогенных и эндогенных химических соединений. Обобщенное уравнение химической реакции, осуществляемой цитохромами Р-450, представлено ниже:
S + NAD(P)H + O2 SO +NAD(P)+ + H2O,
где S – молекула субстрата, а SO – ее окисленная форма. Таким образом, для окисления субстрата цитохром Р-450 чаще всего использует электроны свободного кислорода, поступление которых к ферменту опосредовано NAD(P)H и флавопротеиновой редуктазой. Молекулы цитохрома Р-450 интегрированы в мембраны и при гомогенизации клеток ассоциированы с фракцией микросом. На рис. I.53 представлен механизм метаболической активации 1,2-бензпирена (БП) – одного из наиболее сильных проканцерогенов. БП широко распространен в окружающей среде и в больших количествах образуется при горении нефтепродуктов, табака, а также при других термических воздействиях на органические соединения. Метаболические превращения БП по эпоксид-диольному пути начинаются с его эпоксидирования в положении 7,8 определенной изоформой цитохрома Р-450, ассоциированной с мембранами микросом. Полученный эпоксид гидролизуется эпоксидгидролазой в соответствующий диол БП. Далее под действием другой изоформы цитохрома Р-450 происходит образование предпочтительно двух диастереомеров эпоксида в положении 9,10 и других минорных производных (соединения в фигурных скобках, см. рис. I.53). Оказалось, что изомер (+)-анти-БПДЭ как in vitro, так и in vivo нестабилен и ковалентно связывается преимущественно с N2-атомом дезоксигуанозина ДНК своим С10-атомом с образованием аддуктов БПДЭ-ДНК.
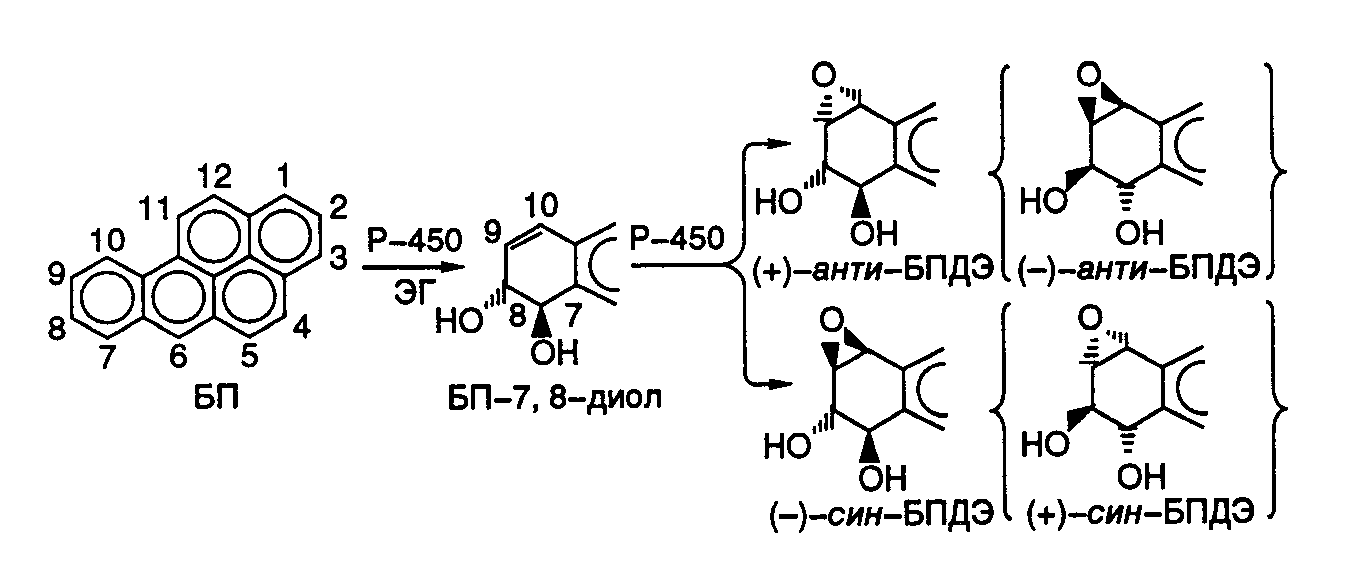
Рис. I.53. Механизм метаболической активации 1,2-бензопирена (БП) микросомами животных
БПДЭ – 9,10-эпоксид-1,2-бензопирен-7,8-дигидродиола, Р-450 – цитохром Р-450, ЭГ – эпоксидгидролаза
Механизм метаболической активации БП подробно рассмотрен здесь для иллюстрации общих принципов химического мутагенеза. Метаболическая активация ксенобиотиков с образованием реакционноспособных метаболитов является одной из основных причин генотоксичности множества химических соединений окружающей среды, с которыми организм контактирует на протяжении всей жизни. Список химических мутагенов экзогенного происхождения далеко не исчерпывается перечисленными химическими соединениями. По мере углубления исследований число известных мутагенов непрерывно растет благодаря созданию высокочувствительных методов оценки мутагенной активности. Известно, что почти все мутагены одновременно являются канцерогенами – веществами, вызывающими возникновение злокачественных опухолей, хотя обратное утверждение не всегда верно. Все это объясняет необходимость сохранения чистоты среды обитания человека, животных и растений.
Эндогенные мутагены. Выше уже упоминалось, что молекулы ДНК часто претерпевают in vivo тепловую депуринизацию, которая может быть спонтанным внутренним источником измененных нуклеотидов. Другим источником эндогенных мутаций служит самопроизвольное дезаминирование цитозина в составе ДНК с образованием урацила. 5-Метилцитозин – одно из модифицированных оснований ДНК, представляет собой "горячую точку" возникновения мутаций путем спонтанного дезаминирования, так как в результате удаления его аминогруппы образуется нормальное основание T, не распознаваемое системами репарации как мутантное.
К сожалению, не только окружающая среда может быть источником генотоксических химических соединений, отравляющих жизнь организма и нарушающих функционирование его генома. Свободные радикалы, которые образуются в организме во время нормального метаболизма, могут быть дополнительной и существенной причиной спонтанных мутаций. В частности, частота повреждений нуклеотидов ДНК, появляющихся под действием свободных радикалов кислорода, приближается к частоте мутаций, возникающих при депуринизации ДНК. В клетках свободные радикалы кислорода возникают в реакциях восстановления, в результате которых появляются чрезвычайно реакционноспособные промежуточные соединения. Наибольшую опасность для ДНК представляют радикалы гидроксила, супероксид и синглетный кислород, которые образуются в процессе дыхания, фагоцитоза и при повреждении клеток. Путем измерения содержания в моче человека 8-гидроксидезоксигуанозина и тимингликоля – основных модифицированных нуклеозидов и оснований, образующихся под действием радикалов кислорода, было установлено, что ежедневно в каждой клетке человека возникает 10000 таких модифицированных нуклеотидов, мутагенный эффект которых в настоящее время доказан.
Другим источником эндогенных мутагенов в организме является метаболизм нормальной микрофлоры. Некоторые промежуточные соединения, возникающие при метаболизме аминокислот, желчных кислот и холестерина под действием бактерий организма человека и обладающие мутагенной и канцерогенной активностью, представлены в табл. I.19. Промоторами в канцерогенезе называют вещества, не имеющие канцерогенной активности, но ускоряющие процесс канцерогенеза под действием химических веществ – истинных канцерогенов. Как видно из таблицы, достаточно широк список веществ, обладающих всеми вышеупомянутыми активностями и образующихся под действием нормальной микрофлоры человека, обитающей, в частности в его кишечнике и на слизистых оболочках. Помимо этого в результате метаболизма в бактериальных клетках происходит активация нитратов с образованием мутагенных и канцерогенных N-нитрозаминов в кишечнике, желудке и ротовой полости человека. Описан также гидролиз обезвреженных ферментами детоксикации конъюгатов истинных канцерогенов.
Таким образом, многочисленные мутагены экзогенного и эндогенного происхождения создают вокруг и внутри любого многоклеточного организма тот мутагенный фон, к которому он вынужден приспосабливаться в процессе эволюции. Мутагенный фон "среды обитания" информационных макромолекул и, прежде всего, ДНК уникален для каждого вида живых организмов в силу особенностей их метаболизма и условий жизни. В соответствии с этим каждый биологический вид для того чтобы выжить, т.е. понизить частоту мутаций в конкретных генах до приемлемого уровня, обладает системами защиты от мутаций определенной эффективности. О механизмах функционирования таких систем защиты генетической информации речь пойдет ниже. А пока рассмотрим некоторые методы определения мутагенной активности химических соединений, применяемые для мониторинга окружающей среды.
Таблица I.19