
- •Часть I. Механизмы хранения и реализации генетической информации 17
- •Предисловие автора
- •Часть I. Механизмы хранения и реализации генетической информации введение
- •Средний размер гаплоидного генома у некоторых групп организмов
- •Гены и хромосомы
- •Геном прокариот
- •Геном вирусов
- •Нуклеоид бактериальной клетки
- •Геном архебактерий
- •Минимальный размер генома одноклеточных организмов
- •Геном эукариот
- •Последовательности нуклеотидов эукариотического генома
- •Хроматин
- •Свойства гистонов животных
- •Роль днк-топоизомераз в обеспечении структуры и функционирования хроматина
- •Реализация генетической информации при экспрессии генов
- •Транскрипция
- •Днк-зависимые рнк-полимеразы
- •Характеристики белковых компонентов холофермента рнк-полимеразы II дрожжей
- •Единицы транскрипции (транскриптоны)
- •Этапы транскрипции
- •Субъединичный состав и характеристика основных факторов транскрипции (gtf) рнк-полимеразы II человека
- •Основные факторы элонгации рнк-полимеразы II
- •Хроматин во время транскрипции
- •Субъединичный состав и свойства белковых комплексов Swi/Snf и nurf
- •Котранскрипционные и посттранскрипционные модификации рнк
- •Процессинг рнк у бактерий
- •Редактирование пре-мРнк
- •Различные способы редактирования мРнк
- •Редактирование рнк у животных и их вирусов
- •Другие модификации эукариотических мРнк
- •Сравнение полиаденилирования мРнк у эукариот и прокариот
- •5’-Концевой сайт Точка 3’-Концевой сайт
- •5’–Экзон 1guaugu__...__uacuaac__...__(Py)nAgэкзон 2–3’
- •Механизм прямой и обратной реакций аутосплайсинга интронов группы I
- •Кэп-связывающий комплекс в роли фактора, сопрягающего основные реакции метаболизма транскриптов рнк-полимеразы II
- •Функциональная компартментализация ядра
- •Интерфазные хромосомы в ядре
- •Ядрышко
- •Пространственная организация синтеза мРнк
- •Ядерные тельца и домены
- •Компартментализованное ядро
- •Биосинтез белка рибосомами бактерий
- •Рибосомы
- •Этапы биосинтеза белка
- •Антибиотики, действующие на уровне трансляции
- •Трансляция у эукариот
- •Особенности первичной структуры эукариотических мРнк
- •Инициация биосинтеза белка эукариотическими рибосомами
- •Элонгация полипептидных цепей
- •Терминация трансляции
- •Трансляция в митохондриях
- •Трансляция в хлоропластах.
- •Основные пути регуляции экспрессии генов
- •Регуляция экспрессии генов на уровне транскрипции у прокариот
- •Регуляция на уровне инициации транскрипции
- •Регуляция синтеза рнк на уровне элонгации и терминации
- •Регуляция экспрессии генов на уровне транскрипции у эукариот
- •Передача сигнала и вторичные мессенджеры
- •Рецепторы мембран, осуществляющие трансмембранный перенос сигнала
- •Механизмы позитивной регуляции транскрипции
- •Классификация факторов транскрипции
- •Функциональные домены факторов транскрипции
- •Механизмы негативной регуляции транскрипции
- •Структура хроматина как специфический регулятор экспрессии генов
- •Импринтинг
- •Метилирование днк в регуляции транскрипции
- •Факторы транскрипции позвоночных, на активность которых оказывает влияние метилирование остатков цитозина в узнаваемых ими регуляторных последовательностях нуклеотидов
- •Посттранскрипционная регуляция экспрессии генов
- •Направленный транспорт, внутриклеточная локализация и депонирование мРнк
- •Сплайсинг рнк в регуляции экспрессии генов
- •Избирательная деградация мРнк
- •Регуляция экспрессии генов на уровне трансляции
- •Регуляция инициации трансляции
- •Регуляция элонгации синтеза полипептидных цепей
- •Регуляция терминации трансляции
- •Синтез белков, содержащих остатки селеноцистеина
- •Посттрансляционная регуляция экспрессии генов
- •Последствия фолдинга вновь синтезированных полипептидных цепей
- •Специфические протеиназы в посттрансляционном процессинге белков
- •Убиквитин-зависимая система протеолиза в регулируемой деградации белков
- •Сплайсинг белков
- •Другие посттрансляционные модификации белков
- •Воспроизведение генетической информации
- •Репликация днк
- •Белки, участвующие в репликации днк
- •Белки, входящие в состав репликативных комплексов прокариотических и эукариотических организмов
- •Репликативная вилка e. Coli и бактериофага t4
- •Особенности функционирования репликативной вилки эукариот
- •Эукариотические днк-полимеразы и их функциональные гомологи у прокариот
- •Регуляция репликации днк
- •Инициация репликации днк у e. Coli и ее регуляция
- •Регуляция репликации плазмиды ColE1
- •Особенности репликации линейных геномов
- •Линейные хромосомы бактерий
- •Репликаторы эукариот
- •Репликация теломерных участков эукариотических хромосом
- •Пространственная организация синтеза днк у эукариот
- •Защита генетической информации
- •Мутации
- •Основные источники мутаций и методы определения мутагенной активности
- •Основные классы алкилирующих агентов
- •Метаболиты нормальной микрофлоры человека, обладающие мутагенной и канцерогенной активностями
- •Sos-мутагенез у бактерий
- •Мутаторный фенотип
- •Экспансия днк
- •Адаптивные мутации
- •Механизмы защиты генома от мутаций
- •Репарация днк
- •Основные механизмы репарации поврежденной днк
- •Эксцизионная репарация в клетках животных
- •Днк-гликозилазы и эндонуклеазы клеток микроорганизмов и человека, участвующие в ber
- •Белки животных, участвующие в ner
- •Гомологичная рекомбинация в репарации днк
- •Репарация ошибочно спаренных нуклеотидов
- •Полимераза поли(adp-рибозы) в репарации днк у эукариот
- •Альтруистичная днк
- •Парадокс возможности существования многоклеточных организмов
- •Повышение информационной стабильности генома избыточными последовательностями
- •Селективная защита генов от мутаций
- •Высокоупорядоченное расположение летальных генов на хромосомах
- •Возможный смысл парадокса с
- •Современная концепция гена
- •Часть II основные направления развития прикладной молекулярной генетики Введение
- •Часть II. Искусственные генетические системы
- •Принципы генной инженерии
- •Основные ферменты, используемые в генной инженерии
- •Рестриктазы и днк-метилазы
- •Эффективность расщепления коротких последовательностей днк некоторыми распространенными рестриктазами
- •Днк- и рнк-лигазы
- •Ферменты матричного синтеза днк и рнк
- •Частота ошибок при синтезе днк, осуществляемом термостабильными днк-полимеразами in vitro при проведении пцр в оптимальных условиях
- •Другие ферменты
- •Векторы
- •Плазмидные векторы
- •Векторы на основе фага
- •Космиды и фазмиды
- •Сверхъемкие векторы yac, bac и pac
- •Интегрирующие и челночные (бинарные) векторы
- •Конструирование экспрессирующих векторов и их функционирование
- •Векторы для переноса днк в клетки животных и растений
- •Клонотеки генов
- •Получение клонотек генов
- •Введение рекомбинантных днк в клетки
- •Методы скрининга клонотек генов
- •Эукариотические системы экспрессии рекомбинантных генов, основанные на культурах клеток
- •Клетки яичников китайских хомячков (линия cho)
- •Клетки мышиной миеломы (линия Sp2/0)
- •Клетки селезенки мышей (линия mel)
- •Клетки африканской зеленой мартышки (линия cos)
- •Клетки насекомых, зараженные бакуловирусами
- •Сравнение эффективности рассмотренных систем экспрессии
- •Бесклеточные белоксинтезирующие системы
- •Прокариотические системы
- •Эукариотические системы
- •Проточные системы
- •Другие современные методы исследования генов
- •Рестрикционное картирование генов
- •"Прогулки и прыжки по хромосомам"
- •S1-картирование рнк и днк
- •Футпринтинг
- •Стратегия выделения нового гена
- •Направленный мутагенез и белковая инженерия
- •Методы направленного получения мутаций
- •Получение делеций и вставок
- •Химический мутагенез
- •Сайт-специфический мутагенез с использованием олигонуклеотидов
- •Полимеразная цепная реакция в направленном мутагенезе
- •Белковая инженерия
- •Библиотеки пептидов и эпитопов
- •Белки-репортеры в гибридных белках
- •Гибридные токсины
- •Подходы к созданию новых ферментов
- •Субтилигаза в лигировании пептидов
- •Концепция ксенобиоза
- •Антисмысловые рнк, рибозимы и дезоксирибозимы
- •Антисмысловые рнк и олигонуклеотиды
- •Механизм действия антисмысловых рнк
- •Использование антисмысловых рнк
- •Влияние экспрессии антисмысловых рнк на фенотип трансгенных мышей
- •Природные антисмысловые рнк
- •Антисмысловые рнк и патология: возможный механизм возникновения доминантных мутаций
- •Рибозимы и дезоксирибозимы
- •Типы рибозимов
- •Свойства рибозимов
- •Рибозимы как лекарственные средства
- •Репарация мутантных рнк с помощью рибозимов, осуществляющих транс-сплайсинг
- •Дезоксирибозимы
- •Аптамеры
- •Молекулы рнк у истоков жизни
- •Молекулы рнк в качестве рнк-репликаз
- •Возможность синтеза полипептидных цепей молекулами рнк
- •Трансгенные животные и растения
- •Способы получения трансгенных многоклеточных организмов
- •Экспрессия трансгенов
- •Использование трансгенов у животных
- •Исследование механизмов экспрессии генов
- •Токсигены в исследовании дифференцировки соматических клеток в онтогенезе
- •Изменение физиологического статуса лабораторных и сельскохозяйственных животных
- •Моделирование наследственных и приобретенных заболеваний человека
- •Трансгенные растения
- •Генотерапия наследственных и приобретенных заболеваний
- •Способы доставки новых генов в геном человека
- •Управление экспрессией трансгенов в клетках-мишенях
- •Современные достижения генотерапии онкологических заболеваний
- •Ближайшие перспективы использования генотерапии
- •Успехи генотерапии в модельных экспериментах
- •Проблемы, возникающие в связи с практическим применением генотерапии
- •Днк-диагностика и днк-типирование
- •Днк-диагностика наследственных и приобретенных заболеваний
- •Получение клинического генетического материала
- •Диагностика заболеваний
- •Днк-типирование
- •Днк-типирование микроорганизмов
- •Идентификация личности на основе минисателлитной днк: определение отцовства
- •Микроматрицы и микрочипы днк
- •Методы создания микроматриц днк
- •Ограничения в использовании микроматриц днк
- •Использование микроматриц днк в фундаментальных и прикладных исследованиях
- •Картирование и определение первичной структуры генома человека
- •Основные подходы к картированию генома человека
- •Генетические карты сцепления
- •Современные методы построения генетических карт сцепления
- •Пцр в исследованиях генома человека
- •Физические карты низкого разрешения
- •Физические карты высокого разрешения
- •Определение полной первичной структуры днк генома человека
- •Базы данных получаемой информации
- •Заключение
- •Рекомендуемая литература
Основные ферменты, используемые в генной инженерии
Рестриктазы и днк-метилазы
Среди ферментов, используемых в генной инженерии для клонирования, большое значение имеют эндонуклеазы рестрикции – рестриктазы. Эти ферменты, впервые открытые как часть системы рестрикции–модификации ДНК у бактерий, специфически гидролизуют молекулы двухцепочечных ДНК при наличии в них определенных последовательностей нуклеотидов, называемых сайтами рестрикции. В то же время метилазы используют для ограничения числа сайтов рестрикции и получения более крупных фрагментов ДНК с помощью рестриктаз.
Классификация рестриктаз. По механизму действия и молекулярной структуре различают три типа рестриктаз. Ферменты рестрикции типа I представляют собой сложные мультимерные комплексы, построенные из трех субъединиц с молекулярной массой до 300 кДа, которые обладают рестриктазной, ДНК-метилазной и АТРазной активностями. Рестриктазы типа I для проявления своей активности требуют присутствия ATP, S-аденозилметионина и ионов Mg2+, они не распознают специфические последовательности нуклеотидов и в силу этого не находят широкого применения в генной инженерии. Рестриктазы типа II узнают специфические последовательности нуклеотидов в точке расщепления ДНК или непосредственной близости от нее, требуют для проявления активности наличия в реакционной смеси ATP и ионов Mg2+ и чаще всего используются при молекулярном клонировании. Ферменты типа III также активны только в присутствии ATP и ионов Mg2+ и не проявляют абсолютной зависимости от S-аденозилметионина.

Рис. II.1. Формы разрывов двухцепочечных ДНК, образующихся под действием рестриктаз
а– 5’-выступающие (1), 3’-выступающие "липкие" (2) и "тупые" (3) концы ДНК, образующиеся под действием рестриктазBamHI,KpnI иPvuII соответственно. Стрелками обозначены места разрывов цепей ДНК, пунктирной линией – ось симметрии сайтов рестрикции;
б– лигирование с потерей сайта рестрикции
Названия рестриктаз складываются из первых букв видовых названий бактерий, в которых они обнаружены, например Eco – E. coli. В том случае, когда различные по специфичности действия рестриктазы присутствуют в клетках разных штаммов одного вида бактерий, в название рестриктазы вводят дополнительную букву, например рестриктазы Hinc и Hind выделены из бактериальных клеток Haemophilus influenzae, штаммы с и d. Цифры, следующие за буквенными обозначениями, отражают последовательность открытия соответствующих рестриктаз в клетках бактерий одного вида, например HaeI, HaeII и HaeIII из H. aegipticus.
Рестриктазы типа II – основной инструмент генной инженерии. Большинство рестриктаз типа II специфически узнают на ДНК тетра- и гексануклеотидные последовательности, а по крайней мере три из них – октануклеотиды. Чем короче олигонуклеотидная последовательность сайта рестрикции, узнаваемого рестриктазой, тем чаще он встречается в случайной последовательности нуклеотидов, в которой каждый из четырех нуклеотидов представлен с одинаковой частотой (50% А–Т-пар и 50% G–С-пар). Так, случайная тетрануклеотидная последовательность встречается в среднем через каждые 256 п.о. (44), а гексануклеотидная – через каждые 4096 п.о. (46). Однако в природных ДНК распределение нуклеотидов может заметно отличаться от случайного. Например, для эукариотических ДНК характерна низкая частота встречаемости динуклеотида CpG и соответственно сайтов рестрикции, содержащих эти динуклеотиды (рестриктазы HhaI, HpaII, TaqI, ThaI, AvaI, HaeII, HindII, SalI, SmaI, XhoI, XmaI). Существенное отклонение частоты встречаемости сайтов рестрикции от ожидаемого при случайном их распределении вдоль ДНК свойственно и хромосомам термофильных бактерий, которым, напротив, свойственно (хотя и не во всех случаях) обогащение по G–С-парам. Для большинства сайтов, узнаваемых рестриктазами типа II, характерно наличие в них симметрии второго порядка, т.е. узнаваемые ими последовательности представляют собой палиндромы, например у рестриктазы EcoRI – 5’-GAATTC-3’. Это означает, что нуклеотиды, расположенные в каждой из цепей на равном расстоянии от оси симметрии, комплементарны друг другу. Если точки расщепления противоположных цепей ДНК смещены друг относительно друга в сайте рестрикции, то образующиеся в результате рестрикции концы ДНК содержат выступающие одноцепочечные участки. Поскольку такие участки комплементарны сами себе и друг другу и могут между собой взаимодействовать, их часто называют "липкими" концами. В "липких" концах выступающим одноцепочечным участком может быть как 5’-, так и 3’-конец (рис. II.1,а). Формальным признаком образования 5’- или 3’-выступающих "липких" концов в сайтах рестрикции является расположение точки расщепления цепей ДНК в последовательности, используемой для обозначения сайта рестрикции, слева или справа от оси симметрии соответственно. У некоторых рестриктаз точки расщепления обеих цепей ДНК расположены непосредственно друг под другом в сайте рестрикции. В этом случае после расщепления ДНК "липких" концов не образуется, а получаются так называемые "тупые" концы, в которых нет выступающих одноцепочечных участков ДНК (см. рис. II.1,а). Имеется одно принципиальное функциональное различие между 5’- и 3’-выступающими "липкими" концами – последние невозможно пометить путем их достройки ДНК-полимеразой. Эту особенность следует иметь в виду при выборе рестриктаз для получения рестрикционных фрагментов ДНК, которые предполагается использовать в качестве зондов.
При конструировании рекомбинантных молекул полезно помнить, что, хотя рестриктазы BamHI, BclI, BglII и XhoII узнают разные сайты рестрикции, они образуют одни и те же "липкие" концы, GATC. То же характерно и для группы рестриктаз SalGI, XhoI и AvaI (NCGA). При лигировании (см. ниже) фрагментов ДНК, образованных рестриктазами одной из таких групп, происходит их объединение, но при этом исходные сайты рестрикции теряются, так как в результате образуется новая непрерывная последовательность нуклеотидов (см. рис. II.1,б). Сайты рестрикции для некоторых рестриктаз II типа не являются симметричными. Например, рестриктаза HgaI узнает асимметричную последовательность 5’-GACGC-3’, а одноцепочечные разрывы вносит в противоположные цепи ДНК, отступя вправо на 5 и 10 нуклеотидов соответственно:
5’-GACGC(N)5
3’-CTGCG(N)5(N)5
Последовательности нуклеотидов образующихся "липких" концов являются уникальными для каждого такого сайта рестрикции. Вследствие этого рестрикционные фрагменты ДНК, образовавшиеся под действием данной рестриктазы, в смеси соединяются друг с другом лишь в строго определенной исходной последовательности, которая задается уникальными последовательностями нуклеотидов в "липких" концах рестрикционных фрагментов ДНК. Например, при расщеплении этой рестриктазой репликативной формы ДНК фага X174 образуется 14 фрагментов, которые in vitro объединяются в правильную последовательность с образованием инфекционной X174-ДНК.
Универсальные рестриктазы для одноцепочечных ДНК. На основе рестриктаз, узнающих асимметричные последовательности нуклеотидов, разработана система, позволяющая расщеплять молекулы одноцепочечной ДНК в любой заданной точке. С этой целью синтезируется олигонуклеотид, 5’-концевая часть которого содержит сайт, узнаваемый такой рестриктазой, а последовательность нуклеотидов 3’-концевой части комплементарна участку ДНК, в который необходимо внести эндонуклеазный разрыв. В результате гибридизации олигонуклеотида с одноцепочечной ДНК образуется структура, изображенная на рис. II.2. При этом фермент взаимодействует с сайтом узнавания (участок I), а разрывы вносятся по местам, обозначенным стрелками. Таким образом, положение места эндонуклеазного расщепления будет целиком зависеть от последовательности нуклеотидов участка II синтетического олигонуклеотида, комплементарного ДНК-субстрату.
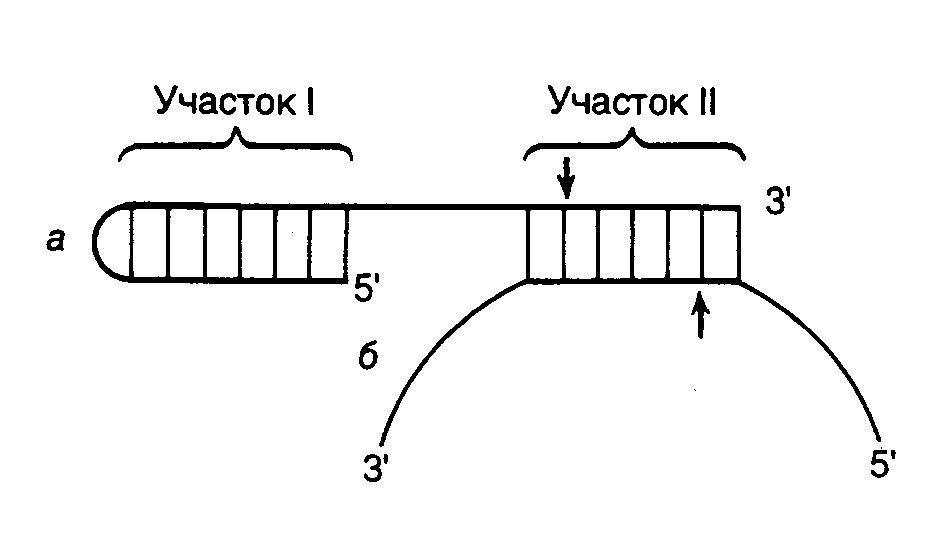
Рис. II.2. Расщепление одноцепочечной ДНК универсальной рестриктазой
а– синтетический олигонуклеотид;б– одноцепочечная ДНК.
После образования шпильки и гибридизации с одноцепочечной ДНК-мишенью олигонуклеотид образует сайт связывания рестриктазы (участок I) и сайт расщепления ДНК-ДНК-гибрида (участок II). Стрелки указывают места эндонуклеазного расщепления ДНК и олигонуклеотида
Изошизомеры. В клетках разных видов бактерий могут содержаться рестриктазы, узнающие одни и те же сайты рестрикции. Такие рестриктазы называют изошизомерами. Изошизомеры некоторых рестриктаз с успехом используются для обнаружения метилированных участков ДНК в геноме. Так, рестриктазы HhaI и HpaII расщепляют неметилированные последовательности GCGC и CCGG соответственно и утрачивают способность к расщеплению, если хотя бы один из остатков цитозина в этих сайтах метилирован. В то же время фермент MspI (изошизомер HpaII) расщепляет последовательность CCGG независимо от того, метилированы или неметилированы остатки цитозина в таком сайте. N-Метилирование остатков аденозина в ДНК можно обнаружить с помощью изошизомеров Sau3A (расщепляет как метилированные, так и неметилированные последовательности GATC), DpnI (расщепляет только метилированные последовательности GMeATC) и MboI (расщепляет только неметилированные последовательности).
Изменение специфичности действия рестриктаз в неоптимальных условиях. Рестриктазы являются высокоспецифическими ферментами. Однако для поддержания этой специфичности in vitro необходимо соблюдать в реакционной смеси оптимальные условия для действия ферментов. При нарушении таких условий у некоторых рестриктаз начинает проявляться вторичная (так называемая штриховая) активность. Так, рестриктаза EcoRI расщепляет последовательность GAATTC при pH 7,3, 100 мМ NaCl в присутствии 5 мМ MgСl2, однако при изменении значений pH, понижении концентрации NaCl или замене ионов Mg2+ на Mn2+, а также в присутствии органических растворителей у фермента появляется тенденция к расщеплению более короткой последовательности AATT (так называемая активность EcoRI). К рестриктазам, обладающим подобными свойствами, относятся также BamHI, BstI, BsuI, DdeI, HhaI, PstI, SalI, SstI, XbaI.
Действие рестриктаз на необычные субстраты. Помимо двухцепочечных ДНК многие рестриктазы способны использовать ДНК-РНК-гибриды в качестве субстрата. Это относится, в частности, к рестриктазам EcoRI, HindII, SalI, MspI, HhaI, AluI, TaqI и HaeIII. Некоторые рестриктазы, например HaeIII, HhaI и SfaI, способны расщеплять одноцепочечную ДНК фага X174, хотя и со значительно меньшей скоростью, чем соответствующую двухцепочечную RF-форму. Такая способность была продемонстрирована для некоторых других рестриктаз, а также ДНК-субстратов. Остается неясным, узнают ли эти рестриктазы истинные одноцепочечные сайты или же последовательности нуклеотидов, заключенные в элементы вторичной структуры.
С развитием метода полимеразной цепной реакции (ПЦР) (см. ниже) часто возникает необходимость расщепления рестриктазами амплифицированных олигонуклеотидов недалеко от их концов, т.е. в условиях, когда сайт рестрикции фланкирован с одного из своих концов одним или несколькими нуклеотидами. В этом случае установлена четкая зависимость способности определенных рестриктаз расщеплять сайты рестрикции от количества фланкирующих сайт нуклеотидов. Данное свойство рестриктаз объясняют, в частности тем, что на самих концах двухцепочечной молекулы ДНК происходит локальное плавление двойной спирали ДНК с образованием коротких одноцепочечных участков, захватывающих сайт узнавания рестриктазами. Частично избежать локальное плавление можно понижением температуры реакционной смеси во время проведения рестрикции таких олигонуклеотидов. Поскольку эти данные имеют большое значение для практической генной инженерии, они суммированы в табл. II.1.
Таблица II.1
