
- •УЧастина і загальна мікробіологія
- •Організація, устаткування, режим роботи бактеріологічних, імунологічних і вірусологічних лабораторій
- •Методи лабораторних досліджень
- •1. Феноловий генціанвіолет
- •Культивування мікроорганізмів
- •Екологія мікроорганізмів
- •Мікробіологічне дослідження води
- •Визначення індексу бгкп на етапах очищення
- •Дослідження мікрофлори повітря
- •Мікробіологічне дослідження грунту
- •Мікробіологічні дослідження харчових продуктів
- •Дослідження мікрофлори людини
- •Експериментальна інфекція. Використання тварин в лабораторних дослідженнях
- •Способи зараження експериментальних тварин
- •Мікробіологічне дослідження трупа
- •Визначення чутливості бактерій до антибіотиків
- •Основні набори дисків, які рекомендуються для визначення чутливості залежно від виду виділеної культури та патологічного матеріалу
- •Частина іі імунологія
- •Імунологічні методи діагностики інфекційних захворювань
- •Імунопрофілактика та імунотерапія інфекційних захворювань
- •Мікробіологічна діагностика окремих інфекційних захворювань Стафілококові інфекції
- •Захворювання, спричиненні умовно-патогенними ентеробактеріями
- •Ранова анаеробна газова інфекція
- •Бактероїдози
- •Дифтерія
- •Коклюш і паракоклюш
- •Псевдомонадні інфекції
- •Інфекції, викликані гемофільними бактеріями
- •Легіонельози
- •Лістеріоз
- •Туберкульоз
- •Лепра (проказа)
- •Мікобактеріози
- •Актиномікоз
- •Нокардіоз
- •1 2 Рис. 80. N.Asteroides: колонії (1), ланцюжки і конідії в мазку (2).
- •Сифіліс та інші трепонематози
- •Ендемічні побутові трепонематози
- •Лептоспіроз
- •Епідемічний поворотний тиф
- •Ендемічний поворотний тиф
- •Бореліоз Лайма
- •Рикетсіози
- •Епідемічний висипний тиф
- •Ендемічний висипний тиф
- •Північноазіатський рикетсіоз
- •Гарячка цуцугамуші
- •Пароксизмальний рикетсіоз
- •Трахома
- •Респіраторний хламідіоз
- •Сечостатевий хламідіоз
- •Будова і класифікація вірусів
- •Методи лабораторної діагностики вірусних інфекцій
- •Методи ідентифікації вірусів
- •Виділення та титрування бактеріофагів
- •Парагрип
- •Епідемічний паротит
- •Респіраторно-синцитіальні інфекції
- •Ентеровірусні інфекції
- •Ротавірусні гастроентерити
- •1 Ерпесвірусні інфекції
- •Простий герпес
- •Вітряна віспа - оперізуючий герпес
- •Цитомегалія
- •Аденовірусні інфекції
- •Коронавірусні інфекції
- •Гарячки Марбург і Ебола
- •Арбовірусні інфекції
- •Весняно-літній кліщовий енцефаліт
- •Японський енцефаліт
- •Гарячка Західного Нілу
- •Жовта гарячка
- •Геморагічні гарячки
- •Кримська-Конго геморагічна гарячка
- •Геморагічна гарячка з нирковим синдромом
- •Краснуха
- •Лімфоцитарний хоріоменінгіт
- •Гепатит в
- •Кандидоз
- •.Частина VI протозойні інфекції
- •Методи лабораторної діагностики
- •Малярія
Способи зараження експериментальних тварин
Для постановки біологічної проби або відтворення інфекційного захворювання у лабораторних тварин використовують різні методи введення мікроорганізмів, їх токсинів або іншого досліджуваного матеріалу: нашкірний, внутріш- ньошкірний, підшкірний, внутрішньом' язовий, внутрішньовенний, внутрішньоо- черевинний. Матеріал можна ввести в носові ходи, рот, шлунок, пряму кишку, серце, мозок, піхву, яєчко, кон'юнктиву, порожнину суглобів. Спосіб зараження залежить від типу матеріалу, ймовірних збудників чи їх токсинів і виду тварин.
Нашкірний спосіб - втирання матеріалу в депільовану (позбавлену шерсті) або скарифіковану ділянку шкіри. Втирання проводять тупим кінцем скальпеля обережно (краще під прикриттям скляної лійки). Тварину фіксують до повного висихання матеріалу. Цей спосіб використовують рідко, здебільшого для виявлення збудників, що проникають через неушкоджену шкіру (палички чуми, туляремії, лептоспіри).
Внутрішньошкірний спосіб часто використовують при введенні екзотоксинів (стафілококовий, дифтерійний) для виявлення їх дермонекротичної дії, або при постановці алергічних проб. Матеріал вводять в об 'ємі 0,1-0,2 мл тонкою голкою, користуючись туберкуліновим шприцом. Шкіру, позбавлену шерсті, протирають спиртом, розтягують великим і вказівним пальцями, голку вводять під гострим кутом зрізом доверху, матеріал треба вводити повільно. В місці ін' єкції утворюється характерний пухирець, що нагадує лимонну кірку, але він досить швидко розсмоктується (рис. 30).
Підшкірний спосіб використовується найчастіше. У місці введення після депіляції шкіру обробляють спиртом, захоплюють і підіймають двома пальцями лівої руки і в основу утвореної складки правою рукою вколюють голку шприца. Пройшовши голкою кілька міліметрів, її відхиляють в один чи другий бік, проходять глибше і повільно вводять матеріал, що міститься в шприці (рис. 31). Це робиться для того, щоб введений матеріал не витікав через прокол шкіри назовні. Складку опускають, на голку кладуть вату, змочену спиртом або розчином йоду і
швидко виймають голку. Найбільш зручне місце для підшкірного введення матеріалу в мишей і щурів - на спині біля кореня хвоста, а в гвінейських свинок та кроликів - у ділянці спини чи живота. Мишам вводять 0,5-1,0 мл матеріалу, щурам і свинкам - 1,0-1,5 мл, кроликам - не більше 3,0 мл.
Внутрішньом'язовезараження проводять у ділянку тіла з найбільш розвиненим м'язовим шаром. У кроликів, гвінейських свинок, щурів і мишей - це м'язи верхньої третини задньої лапи, у курей і голубів - грудний м'яз. Ділянку шкіри в місці ін'єкції обробляють так само, як і при підшкірному введенні. Потім великим і вказівним пальцями лівої руки захоплюють товсту м'язову складку і вводять голку майже під прямим кутом в глибину м'язів (рис. 32).
Часто цим методом користуються для експериментального відтворення анаеробних клостридіальних інфекцій.
Внутрішньоочеревинне зараження. Спочатку вистригають шерсть на животі в нижній його третині, протирають спиртом або розчином йоду. Для попередження ушкоджень кишечника тварину тримають вниз головою. З цією ж метою використовують короткі голки з притупленим кінцем. У кроликів і гвінейських свинок роблять маленький надріз шкіри (2-3 мм) у нижній третині живота збоку від середньої лінії. Під гострим кутом вводять голку між шкірою і м'язами, потім переводять її в перпендикулярне положення до очеревини, буравлячим рухом проколюють її, відчуваючи ніби "провал" у черевну порожнину, і вводять досліджуваний матеріал. На місце розрізу накладають шов або хірургічну скрепку. При зараженні мишей і щурів шерсть не голять і надріз не роблять (рис. 33).
Рис.
30.
Внутрішньошкірне
зараження гвінейської свинки.
Рис.
31.
Підшкірне
зараження гвінейської свинки.
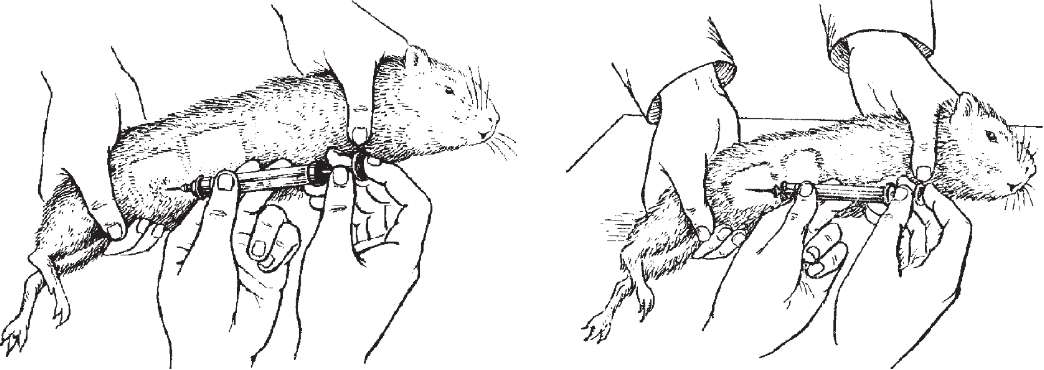
Рис.
33.
Зараження миші в черевну порожнину:
а - фіксація; б - введення.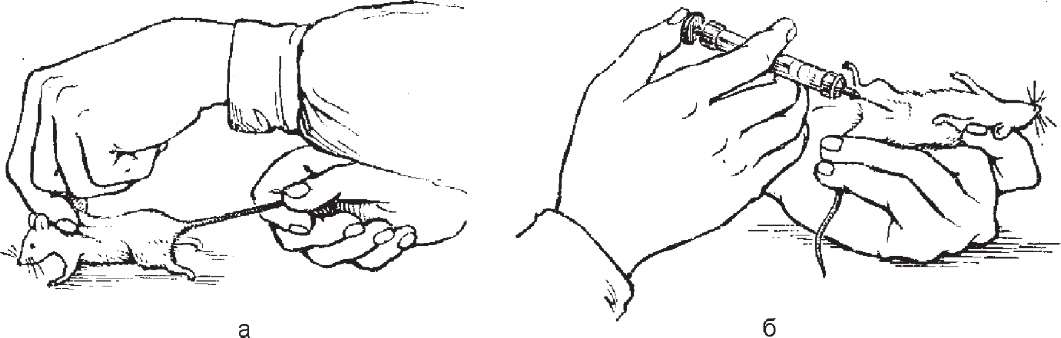
щурам - 3 мл, гвінейським свинкам - 5 мл і кроликам - 10 мл. Цей метод застосовують для швидкого відтворення інфекційного процесу. Його не слід використовувати, якщо досліджуваний матеріал містить багато сторонніх мікробів (грунт, вміст кишечника тощо), щоб не викликати смертельний перитоніт.
Внутрішньовенний спосіб введення. У різних видів тварин при цьому користуються різними венами: кроликів заражають у крайову вену вуха, мишей і щурів - у вену хвоста, гвінейських свинок - у вену стегна, попередньо надрізавши шкіру та відсепарувавши її. Для внутрішньовенних ін'єкцій використовують голки з довгим косим зрізом. Найлегше цей спосіб здійснюється на кроликах завдяки поверхневому розташуванню вушних вен. Перед введенням матеріалу тварину фіксують у спеціальному боксі (рис. 34) або обгортають рушником. Впродовж зовнішнього краю вуха вищипують шерсть, злегка вдаряють кінчиками пальців, або змазують ксилолом, щоб вени краще набрякли, протирають 70° спиртом. Помічник великим пальцем лівої руки натискає на вену біля основи вуха, щоб викликати ще більший застій крові. Голку вколюють у вену в напрямку від периферії до центру, тримаючи її майже паралельно до поверхні вуха (рис. 35).
Рис.
34.
Бокс
для фіксації кроля.
Рис.
35.
Внутрішньовенне
введення.
уколу прикладають вату, змочену спиртом, голку виймають. Кровотеча припиняється досить швидко.
При внутрішньовенному зараженні щурів і мишей користуються тонкими короткими (туберкуліновими) голками з косим зрізом. Перед введенням матеріалу хвіст тварини занурюють у теплу воду (50 °С), щоб викликати гіперемію. Корінь хвоста затискають пальцями, голку вколюють в одну з бокових вен у нижній її третині, тримаючи шприц майже паралельно осі хвоста. Голку повертають зрізом наверх. Коли вона введена у вену, перестають натискати на корінь хвоста і вводять матеріал. Цей спосіб дуже часто використовують при визначенні сили токсинів (рис. 36).
У курей і голубів зручно використовувати вени, які розташовані на внутрішній поверхні крил. Після вищипування пір'я вони стають чітко видимі.
Ентеральнезараження. Найпростіше провести зараження через рот природним шляхом, добавляючи інфекційний матеріал до корму тварин. Але при цьому досить важко точно визначити інфікуючу дозу. У зв'язку з цим частіше зараження проводять примусово. Мишу чи щура тримають вертикально (рис. 37). Культуру бактерій або інший заразний матеріал вводять за допомогою шприца, голка якого має незначну кривизну й напаяну на кінці оливу. Рот відкривають пінцетом. Кількість матеріалу, що вводять у шлунок мишей, становить 0,5-0,7 мл, для щурів - 2-3 мл.
Рис.
36.
Введення
токсину миші.

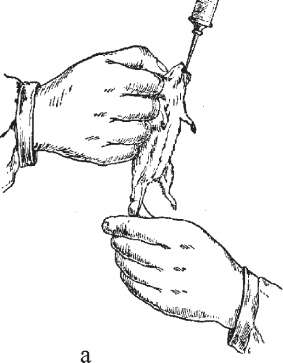
Рис.
37.
Ентеральне
зараження миші (а) і кролика (б).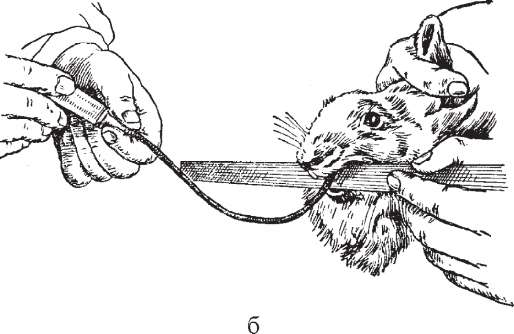
рухи, під час яких трубка легко рухається по стравоходу й потрапляє до шлунка. Зовнішній кінець катетера приєднують до шприца, наповненого певною дозою заразного матеріалу. Його повільно вводять безпосередньо у шлунок в об'ємі 2,5-3,5 мл гвінейським свинкам і 3,5-5,0 мл кроликам.
Інтраназальне зараження. Існує декілька способів зараження тварин через дихальні шляхи, при яких матеріал вводять або за допомогою інгаляції, або спеціальними зондами безпосередньо в трахею чи бронхи. Однак їх використовують рідко. Найпростішим способом, який можна відтворити в будь-якій баклабора- торії, є закапування заразного матеріалу або культури бактерій в носові ходи тварин під легким ефірним наркозом. За допомогою шприца матеріал вводять краплями в носові ходи мишей на глибину 1,0-1,5 мм, білих щурів - 2-3 мм, кроликів і гвінейських свинок - 3,5-4,0 мм. Щоб не пошкодити слизову оболонку, використовують абсолютно тупі голки. За допомогою цього методу можна заражати мишей збудником кашлюку, міксовірусами, гвінейських свинок - рикетсіями та ін. Максимальний об'єм матеріалу, що вводиться, становить для мишей 0,03-0,05 мл, для щурів - 0,05-0,1 мл, для кроликів і гвінейських свинок - до 2 мл.
Інтрацеребральне зараження. Кроликам і гвінейським свинкам роблять трепанацію черепа й заразний матеріал вводять через трепанаційний отвір безпосередньо в мозок або під тверду мозкову оболонку (субдурально). Шкіру в місці трепанації вистригають від шерсті, протирають спиртовим розчином йоду. Потім її зміщують вбік і роблять розріз довжиною 1-3 см, паралельно осі черепа трохи вище задньої орбітальної лінії. Спеціальним інструментом - трепаном - роблять у кістці круглий отвір, через який вставляють голку і легким повільним натиском на поршень шприца вводять 2-3 краплі матеріалу. Отвір у кістці закривають, змістивши на місце шкіру, на яку накладають шви.
Зараження щурів і мишей проводять без трепанації за допомогою туберкулінового шприца з тонкою, тупо обрізаною голкою. На останню надівають металеву муфточку, яка обмежує проникнення голки в мозок лише на глибину 1,5-2 мм. Мишу тримають лівою рукою так, щоб великий і вказівний пальці відтягували шкіру голови в напрямку до шиї, а між мізинцем і безім'яним пальцями утримувався хвіст. У місці проколу шкіру обробляють спиртовим розчином йоду, потім повільно вводять матеріал щоб не викликати раптово підвищення внутрішньочерепного тиску. Цей спосіб на мишах-сисунках використовують для діагностики вірусних енцефалітів, геморагічних гарячок, коксакі-інфекції та ін.
При визначенні результатів дослідів тварин, які загинули протягом першої доби, не враховують, оскільки їх загибель виникла від травматичних ушкоджень.
Зараження в передню камеру ока. При цьому способі матеріал вводять на кон'юнктиву або в передню камеру ока. Найкраще цю операцію виконати на кроликах. Попередньо в кон'юнктивний мішок закапують 2 % розчин новокаїну. Тварину фіксують спиною доверху. Через 1-2 хв тонким очним пінцетом захоплюють складку кон'юнктиви зовні від поверхневого краю рогівки. Потім вводять тонку голку в рогівку біля її краю (лімба) і просувають у центральному напрямку до тих пір, поки в просвіті голки не появиться рідина з передньої камери ока. Після витоку 2-3 крапель рідини на голку насаджують шприц і вводять інфікуючий матеріал в об'ємі не більше 0,05 мл. Голку швидко виймають, маленька ранка сама закривається. Око промивають стерильною водою або 3 % розчином борної кислоти.
З діагностичною метою часто ставлять так звану кератокон'юнктивну пробу на гвінейських свинках. З цією метою у кон 'юнктивний мішок вводять петлю агарової культури (або краплю бульйонної), не травмуючи рогівку. Одні бактерії (ши- гели) викликають кератит, інші (сальмонели) - кон'юнктивіт. Поява виразки на рогівці або її помутніння виникають на 2-5 добу. Пробу використовують для визначення належності культури до роду шигел. Такий спосіб на кролях використовують для відтворення герпетичної інфекції.
Утримання заражених тварин. Після зараження лабораторні тварини називаються "піддослідними". Їх утримують в ізольованому приміщенні (віварії), окремо від розплідника, де розміщені здорові тварини. Приміщення для піддослідних тварин повинно бути теплим (10-15 °С) і сухим. Слід пам'ятати, що кролики чутливі до вогкості, білі миші - до холоду, а гвінейські свинки і до вогкості, і до холоду. Дрібних тварин після зараження вміщують у високі скляні банки, які закривають металевими сітками, а кроликів і свинок - у клітках. Банки і клітки повинні мати етикетки з позначенням дати зараження або номер експерименту, під яким він записаний в лабораторному журналі. Тварини повинні регулярно отримувати корм із достатнім вмістом вітамінів, воду або молоко. При спостереженні за ними відмічають в'ялість, відсутність апетиту, понос, які є ранніми симптомами захворювання. При огляді тварин змушують рухатись, щоб непропустити паралічі. Щоденне спостереження дає змогу своєчасно відібрати захворілих тварин для розтину і подальших досліджень.
