
- •Основні позначення фізичних величин та формули для їх визначення
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Обчислення за рівняннями хімічних реакцій між розчином солі та металом
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Виведення молекулярної формули речовини
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Лабораторні заняття Заняття 1
- •Тема 1. Розв’язування хімічних задач як важливий метод і засіб навчання. Методика розв’язування задач за хімічною формулою та на встановлення хімічного елемента чи формули речовини (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Тема 2. Методика розв’язування задач на знаходження молекулярної формули сполуки за масою, об’ємом та кількістю речовин – продуктів згоряння (4 год.).
- •Тема 3. Методика розв’язування задач на приготування розчинів (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Тема 4. Обчислення швидкості хімічної реакції (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Тема 5. Розв’язування задач, за умовою яких реагенти містять домішки. Обчислення практичного виходу продукту реакції (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Варіант 17
- •Варіант 18
- •Варіант 19
- •Варіант 20
- •Варіант 21
- •Варіант 22
- •Варіант 23
- •Варіант 24
- •Варіант 25
- •Варіант 26
- •Варіант 27
- •Варіант 28
- •Варіант 29
- •Варіант 30
- •Варіант 31
- •Варіант 32
- •Варіант 33
- •Варіант 34
- •Варіант 35
- •Варіант 36
- •Варіант 37
- •Варіант 38
- •Варіант 39
- •Варіант 40
- •Тема 6. Розв’язування задач з використанням закону об’ємних відношень (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Тема 7. Розв’язування задач на знаходження маси, об’єму, масової чи об’ємної частки компонентів суміші (4 год.).
- •Варіант 1/7
- •Варіант 2/7
- •Варіант 3/7
- •Варіант 4/7
- •Варіант 5/7
- •Варіант 6/7
- •Варіант 7/7
- •Варіант 8/7
- •Варіант 9/7
- •Варіант 10/7
- •Варіант 11/7
- •Варіант 12/7
- •Варіант 13/7
- •Варіант 14/7
- •Варіант 15/7
- •Варіант 16/7
- •Варіант 17/7
- •Варіант 18/7
- •Варіант 19/7
- •Варіант 20/7
- •Варіант 21/7
- •Варіант 22/7
- •Варіант 23/7
- •Варіант 24/7
- •Тема 8. Обчислення за хімічними рівняннями кількості, маси, об’єму речовини, якщо один із реагентів узятий у надлишку (4 год.).
- •Варіант 1/8
- •Варіант 2/8
- •Варіант 3/8
- •Варіант 4/8
- •Варіант 5/8
- •Варіант 6/8
- •Варіант 7/8
- •Варіант 8/8
- •Варіант 9/8
- •Варіант 10/8
- •Варіант 11/8
- •Варіант 12/8
- •Варіант 13/8
- •Варіант 14/8
- •Варіант 15/8
- •Варіант 16/8
- •Варіант 17/8
- •Варіант 18/8
- •Варіант 19/8
- •Варіант 20/8
- •Варіант 21/8
- •Варіант 22/8
- •Варіант 23/8
- •Варіант 24/8
- •Варіант 25/8
- •Варіант 26/8
- •Варіант 27/8
- •Варіант 28/8
- •Варіант 29/8
- •Варіант 30/8
- •Тема 9. Розв’язування задач за рівнянням реакції заміщення між металом і розчином солі (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Варіант 17
- •Варіант 18
- •Варіант 19
- •Варіант 20
- •Контрольно-екзаменаційна робота в-1
- •Література
Варіант 4
У стані рівноваги системи N2 + 3H2 2NH3 концентрації реагуючих речовин були: С(N2) = 0,3; C(H2) = 0,9; C(NH3) = 0,4. Обчисліть, як зміниться швидкість прямої і зворотної реакції, якщо тиск збільшити в 5 разів? У якому напрямку зміститься рівновага?
Хімічна рівновага реакції CO2 + H2 CO + H2O установилась при таких концентраціях реагуючих речовин (моль/л): С(СО2) = 8; С(Н2) = 6; С(СО) = 12; С(Н2О) = 8. Рівновага системи була порушена через зменшення концентрації СО до 8 моль/л. Обчисліть, якими стали нові рівноважні концентрації реагуючих речовин після зміщення рівноваги?
Реакція проходить за рівнянням А + В С + D. Рівноважна концентрація речовини В = 0,5 моль/л, С = 0,2 моль/л. Константа рівноваги реакції 0,04. Визначте вихідні концентрації А і В.
Константа рівноваги реакції N2 + 3H2 2NH3 KC=0,1 при 673 К. Рівноважні концентрації (моль/л): С(Н2)=0,6 і С(NH3)=0,18. Обчисліть вихідну і рівноважну концентрацію азоту.
Варіант 5
Як зміниться швидкість реакції 2Fe + 3Cl22FeCl3, якщо тиск у системі збільшити в 5 разів?
Хімічна рівновага реакції СOCl2 CO + Cl2установилась при концентраціях реагуючих речовин (моль/л): С(COCl2) = 8; C(CO) = 4; C(Cl2) = 6. У рівноважну систему додали СOCl2в кількості 4 моль/л. Визначте нові рівноважні концентрації реагуючих речовин після зміщення рівноваги.
Знайдіть концентрації вихідних речовин у реакції H2+ I2
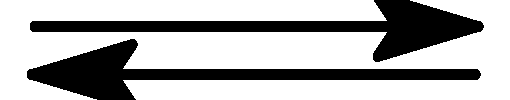 2НI, якщо рівноважні концентрації HI –
0,25 моль/л, I2– 0,05 моль/л, Н2– 0,15 моль/л.
2НI, якщо рівноважні концентрації HI –
0,25 моль/л, I2– 0,05 моль/л, Н2– 0,15 моль/л.Суміш оксиду вуглецю (ІІ) і водяної пари, що містить 50% СО і 50% Н2О (проценти за обємом), пропустили при 1400 К над залізним каталізатором. Константа рівноваги реакції СО + Н2О = СО2+ Н2дорівнює 0,5. Обчислити вихід продуктів і процентний (за обємом) склад рівноважної газової суміші.
Варіант 6
У скільки разів зросте швидкість взаємодії водню з бромом у газовій фазі, якщо концентрації вихідних речовин збільшити у 3 рази?
Хімічна рівновага реакції СOCl2CO + Cl2установилась при концентраціях реагуючих речовин (моль/л): С(COCl2) = 12; C(CO) = 8; C(Cl2) = 10. У рівноважну систему додали СО в кількості 4 моль/л. Визначте нові рівноважні концентрації реагуючих речовин після зміщення рівноваги.
Знайдіть концентрації вихідних речовин у реакції С + Н2О
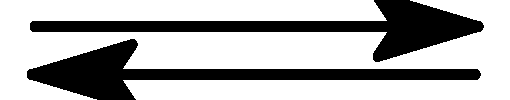 СО + Н2, якщо рівноважні концентрації
СО – 4 моль/л, С – 2 моль/л, Н2О – 1
моль/л.
СО + Н2, якщо рівноважні концентрації
СО – 4 моль/л, С – 2 моль/л, Н2О – 1
моль/л.Реакція проходить за рівнянням А + В
 С
+D.
Рівноважна концентрація речовини В =
0,5 моль/л, С = 0,2 моль/л. Константа рівноваги
реакції 0,04. Визначте вихідні концентрації
А і В.
С
+D.
Рівноважна концентрація речовини В =
0,5 моль/л, С = 0,2 моль/л. Константа рівноваги
реакції 0,04. Визначте вихідні концентрації
А і В.
Варіант 7
Реакція відбувається за рівнянням 2NO + O2 2NO2. Вихідні концентрації реагуючих речовин були (моль/л): С(NO)=0,8, C(O2)=0,6. Як зміниться швидкість реакції, якщо концентрацію кисню збільшити до 0,9 моль/л, а концентрацію нітроген(ІІ) оксиду до 1,2 моль/л?
Хімічна рівновага реакції CO2 +H2CO + H2O установилась при таких концентраціях реагуючих речовин (моль/л): С(СО2) = 9; С(Н2) = 4; С(СО) = 8; С(Н2О) = 6. Рівновага системи була порушена через зменшення концентрації СО2до 7 моль/л. Обчисліть, якими стали нові рівноважні концентрації реагуючих речовин після зміщення рівноваги?
Реакція проходить за рівнянням А2+В2 2АВ. Початкова концентрація речовини А дорівнює 0,8 моль/л, а речовини В - 1 моль/л. Через деякий час концентрація речовини А зменшилась до 0,5 моль/л. Якою в цей час була концентрація речовини В?
Константа рівноваги гомогенної системи СО(г)+Н2О(г) О2(г)+Н2(г)при 850С дорівнює 1. Обчисліть концентрації всіх речовин при рівновазі, якщо вихідні концентрації СО і Н2О відповідно становлять 3 моль/л і 2 моль/л.
