
- •Основні позначення фізичних величин та формули для їх визначення
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Обчислення за рівняннями хімічних реакцій між розчином солі та металом
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Виведення молекулярної формули речовини
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Лабораторні заняття Заняття 1
- •Тема 1. Розв’язування хімічних задач як важливий метод і засіб навчання. Методика розв’язування задач за хімічною формулою та на встановлення хімічного елемента чи формули речовини (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Тема 2. Методика розв’язування задач на знаходження молекулярної формули сполуки за масою, об’ємом та кількістю речовин – продуктів згоряння (4 год.).
- •Тема 3. Методика розв’язування задач на приготування розчинів (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Тема 4. Обчислення швидкості хімічної реакції (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Тема 5. Розв’язування задач, за умовою яких реагенти містять домішки. Обчислення практичного виходу продукту реакції (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Варіант 17
- •Варіант 18
- •Варіант 19
- •Варіант 20
- •Варіант 21
- •Варіант 22
- •Варіант 23
- •Варіант 24
- •Варіант 25
- •Варіант 26
- •Варіант 27
- •Варіант 28
- •Варіант 29
- •Варіант 30
- •Варіант 31
- •Варіант 32
- •Варіант 33
- •Варіант 34
- •Варіант 35
- •Варіант 36
- •Варіант 37
- •Варіант 38
- •Варіант 39
- •Варіант 40
- •Тема 6. Розв’язування задач з використанням закону об’ємних відношень (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Тема 7. Розв’язування задач на знаходження маси, об’єму, масової чи об’ємної частки компонентів суміші (4 год.).
- •Варіант 1/7
- •Варіант 2/7
- •Варіант 3/7
- •Варіант 4/7
- •Варіант 5/7
- •Варіант 6/7
- •Варіант 7/7
- •Варіант 8/7
- •Варіант 9/7
- •Варіант 10/7
- •Варіант 11/7
- •Варіант 12/7
- •Варіант 13/7
- •Варіант 14/7
- •Варіант 15/7
- •Варіант 16/7
- •Варіант 17/7
- •Варіант 18/7
- •Варіант 19/7
- •Варіант 20/7
- •Варіант 21/7
- •Варіант 22/7
- •Варіант 23/7
- •Варіант 24/7
- •Тема 8. Обчислення за хімічними рівняннями кількості, маси, об’єму речовини, якщо один із реагентів узятий у надлишку (4 год.).
- •Варіант 1/8
- •Варіант 2/8
- •Варіант 3/8
- •Варіант 4/8
- •Варіант 5/8
- •Варіант 6/8
- •Варіант 7/8
- •Варіант 8/8
- •Варіант 9/8
- •Варіант 10/8
- •Варіант 11/8
- •Варіант 12/8
- •Варіант 13/8
- •Варіант 14/8
- •Варіант 15/8
- •Варіант 16/8
- •Варіант 17/8
- •Варіант 18/8
- •Варіант 19/8
- •Варіант 20/8
- •Варіант 21/8
- •Варіант 22/8
- •Варіант 23/8
- •Варіант 24/8
- •Варіант 25/8
- •Варіант 26/8
- •Варіант 27/8
- •Варіант 28/8
- •Варіант 29/8
- •Варіант 30/8
- •Тема 9. Розв’язування задач за рівнянням реакції заміщення між металом і розчином солі (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Варіант 17
- •Варіант 18
- •Варіант 19
- •Варіант 20
- •Контрольно-екзаменаційна робота в-1
- •Література
Розв’язок
A: CxHyOz
x : y
: z
=
![]() 3,45:3,45:3,45 = 1:1:1
3,45:3,45:3,45 = 1:1:1
Б: CaHkOs
a : k : s =
![]() =
4,63:6,97:2,34 = 2:3:1
=
4,63:6,97:2,34 = 2:3:1
Г: CmHnOgm : n
: g =
![]() 2,985:4,48:3,73 = 1:1,5:1,25 = 4:6:5
2,985:4,48:3,73 = 1:1,5:1,25 = 4:6:5
(KOH) =CV= 20,02 = 0,04 моль
(С4Н6О5) =![]() моль
моль
Тоді це двохосновна оксикарбонова кислота. Її формула:
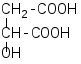
Г
Тоді речовини, згадані в умові задачі, матимуть формули: А – С4Н4О4; Б – С8Н12О4; В – С4Н5О4Br.
Рівняння реакцій:
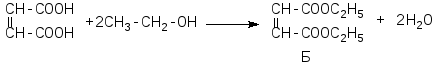

Задача 13. ГазАмає густину в 3 рази більшу за повітря. При взаємодії з водою газуАна холоді і в темноті одержують тільки кислотуБ, яка на світлі здатна перетворюватися в дві кислоти –ВіГ. Якщо розчинити у воді газА, пропущений попередньо через розжарену скляну трубку, одержують теж дві кислоти –БіВ. При взаємодії одного з продуктів термічного розкладу газуАз розчином лугу в залежності від умов одержують солі кислот абоБіВ, абоВіГ. Укажіть перелічені речовини і напишіть рівняння реакцій, якщо відомо, що одна із солей кислотиГмістить 31,8% калію і 39,2% кисню.
Розв’язок
Сіль кислоти Г – КхЕyOz. Молекула електронейтральна, тому:
![]()
0,815 +
![]() -
4,9 = 0
-
4,9 = 0
29n = 4,085a
7,1n=a
-
n
2

2
3
4
5
6
7
a
7,1
14,2
21,3
27,4
35,5
42,6
49,7
E
-
-
-
-
Cl
-
-
Г – KxClyOz
x : y : z = 0,815 : 0,816 : 2,45 = 1 : 1 : 3
KClO3
Mr(A) = 29·3 = 87 – Cl2O
A – Cl2O; Б – HClO; В – HCl; Г – HClO3
Cl2O + H2O = 2HClO
2Cl2O = 2Cl2 + O2
3HClO = 2HCl + HClO3
Cl2 + H2O = HCl + HClO
Cl2
+ KOH
![]() KCl
+ KClO + H2O
KCl
+ KClO + H2O
3Cl2
+ 6KOH
![]() 5KCl + 3H2O
5KCl + 3H2O
Задача 14. РечовинаАз відносною молекулярною масою 94 має такий процентний склад: 76,60% С, 6,38% Н, 17,02% О (за масою). РечовинаАреагує з натрієм і гідроксидом натрію. При взаємодіїАз метилхлоридом в присутності АlCl3утворюються речовиниВіС, а також хлороводень. РечовинаDз відносною молекулярною масою 92 має процентний склад: 91,30% С, 8,70% Н (за масою) і на світлі реагує з хлором з утворенням речовиниЕ, яка при гідролізі в лужному середовищі перетворюється в речовинуF, ізомерну речовинамВіС. Наведіть структурні формули речовинА, В, С, D, EiFі напишіть рівняння згаданих хімічних реакцій.
Розв’язок
(С) =
![]() ;(Н) =
;(Н) =![]() ;(О) =
;(О) =![]()
С6Н6О. Так як речовина А взаємодіє з натрієм і натрій гідроксидом, то це фенол:
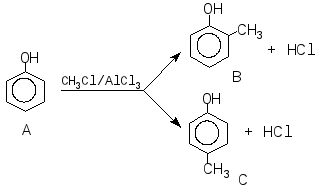
Речовина D:
(C)
=
![]() ;
(H)
=
;
(H)
=
![]() ;
D – C7H8
;
D – C7H8
Враховуючи умову задачі, речовина D– толуол.

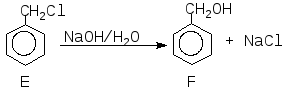
Лекція № 3. Задачі на приготування розчинів
Задача 1. Визначте масу 24,5%-ного розчину сульфатної кислоти, в якому треба розчинити 120 г сірчаного ангідриду, щоб утворився 49%-ний її розчин?
Розв’язок
Такі задачі можна розв’язувати через „правило хреста”.
Нехай є розчин масою m1, у якому масова частка розчиненої речовини W1. До цього розчину долили розчин масоюm2, у якому масова частка розчиненої речовини W2. При цьому утворився розчин масоюm3, у якому масова частка розчиненої речовини W3, причому, маса утвореного розчину буде дорівнювати сумі мас першого і другого розчинів, а маса розчиненої речовини в третьому розчині буде дорівнювати сумі мас розчиненої речовини у першому і другому розчинах.
+
= m1 W1
m1 m2 W2
m2 m3 W3
m3





Оскільки маса розчиненої речовини в третьому розчині буде дорівнювати сумі мас розчиненої речовини у першому і другому розчині, то:
W1 m1 +W2 m2 =W3 m3
Так як маса третього розчину буде дорівнювати сумі мас першого і другого розчинів, то:
W1 m1 +W2 m2 =W3 (m1+m2)
W1 m1 +W2 m2=W3 m1 +W3 m2
W1 m1 –W3 m1=W3 m2 –W2 m2
m1(W1 –W3) = m2(W3 –W2)
![]() – формула правила змішування
– формула правила змішування
Часто замість виведення формули правила змішування використовують „правило хреста”
-
W
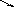 1
1
W3-W2

W3
W2

W1-W3
І спосіб.
W1=
![]()

 1W3-W2
1W3-W2
 W3
W3
W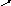 2W1-W3
2W1-W3
W1– уявна масова частка сульфатної кислоти в сірчаному ангідриді.
1
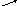 ,225
0,245
,225
0,245

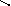 0,49
0,49
0,245 0,735
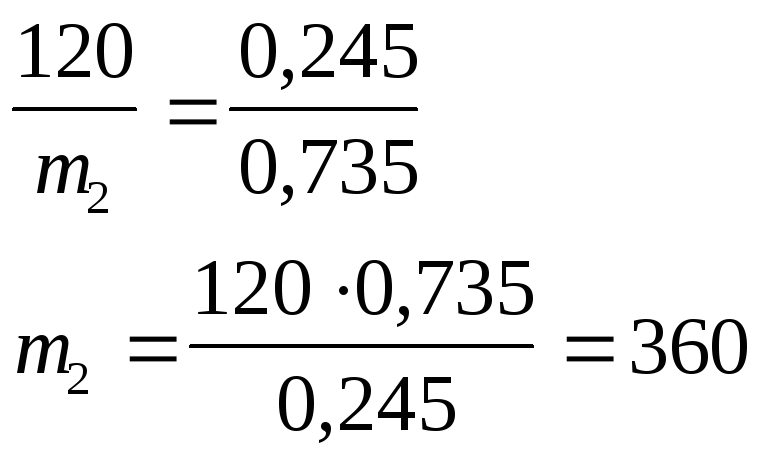
ІІ спосіб.
SO3 + H2O = H2SO4
m(р-ну H2SO4)=x; m(H2SO4) = 0,245x;
![]()
![]() моль
моль

Задача 2. Визначити масу води, в якій треба розчинити 45 г цукру, щоб одержати розчин з масовою часткою цукру 10%.
