
- •Основні позначення фізичних величин та формули для їх визначення
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Обчислення за рівняннями хімічних реакцій між розчином солі та металом
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язання
- •Розв’язок
- •Розв’язок
- •Виведення молекулярної формули речовини
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Розв’язок
- •Лабораторні заняття Заняття 1
- •Тема 1. Розв’язування хімічних задач як важливий метод і засіб навчання. Методика розв’язування задач за хімічною формулою та на встановлення хімічного елемента чи формули речовини (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Тема 2. Методика розв’язування задач на знаходження молекулярної формули сполуки за масою, об’ємом та кількістю речовин – продуктів згоряння (4 год.).
- •Тема 3. Методика розв’язування задач на приготування розчинів (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Тема 4. Обчислення швидкості хімічної реакції (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Тема 5. Розв’язування задач, за умовою яких реагенти містять домішки. Обчислення практичного виходу продукту реакції (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Варіант 17
- •Варіант 18
- •Варіант 19
- •Варіант 20
- •Варіант 21
- •Варіант 22
- •Варіант 23
- •Варіант 24
- •Варіант 25
- •Варіант 26
- •Варіант 27
- •Варіант 28
- •Варіант 29
- •Варіант 30
- •Варіант 31
- •Варіант 32
- •Варіант 33
- •Варіант 34
- •Варіант 35
- •Варіант 36
- •Варіант 37
- •Варіант 38
- •Варіант 39
- •Варіант 40
- •Тема 6. Розв’язування задач з використанням закону об’ємних відношень (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Тема 7. Розв’язування задач на знаходження маси, об’єму, масової чи об’ємної частки компонентів суміші (4 год.).
- •Варіант 1/7
- •Варіант 2/7
- •Варіант 3/7
- •Варіант 4/7
- •Варіант 5/7
- •Варіант 6/7
- •Варіант 7/7
- •Варіант 8/7
- •Варіант 9/7
- •Варіант 10/7
- •Варіант 11/7
- •Варіант 12/7
- •Варіант 13/7
- •Варіант 14/7
- •Варіант 15/7
- •Варіант 16/7
- •Варіант 17/7
- •Варіант 18/7
- •Варіант 19/7
- •Варіант 20/7
- •Варіант 21/7
- •Варіант 22/7
- •Варіант 23/7
- •Варіант 24/7
- •Тема 8. Обчислення за хімічними рівняннями кількості, маси, об’єму речовини, якщо один із реагентів узятий у надлишку (4 год.).
- •Варіант 1/8
- •Варіант 2/8
- •Варіант 3/8
- •Варіант 4/8
- •Варіант 5/8
- •Варіант 6/8
- •Варіант 7/8
- •Варіант 8/8
- •Варіант 9/8
- •Варіант 10/8
- •Варіант 11/8
- •Варіант 12/8
- •Варіант 13/8
- •Варіант 14/8
- •Варіант 15/8
- •Варіант 16/8
- •Варіант 17/8
- •Варіант 18/8
- •Варіант 19/8
- •Варіант 20/8
- •Варіант 21/8
- •Варіант 22/8
- •Варіант 23/8
- •Варіант 24/8
- •Варіант 25/8
- •Варіант 26/8
- •Варіант 27/8
- •Варіант 28/8
- •Варіант 29/8
- •Варіант 30/8
- •Тема 9. Розв’язування задач за рівнянням реакції заміщення між металом і розчином солі (4 год.).
- •Варіант 1
- •Варіант 2
- •Варіант 3
- •Варіант 4
- •Варіант 5
- •Варіант 6
- •Варіант 7
- •Варіант 8
- •Варіант 9
- •Варіант 10
- •Варіант 11
- •Варіант 12
- •Варіант 13
- •Варіант 14
- •Варіант 15
- •Варіант 16
- •Варіант 17
- •Варіант 18
- •Варіант 19
- •Варіант 20
- •Контрольно-екзаменаційна робота в-1
- •Література
Варіант 1
Суміш газів, що містила амоніак, після того, як вона була пропущена крізь розбавлений розчин сульфатної кислоти, займала 776 мл (н.у.). Знаючи, що при цьому на утворення амоній сульфату було витрачено 100 мл розчину, який містить в 1 л 4,9 г кислоти, знайдіть відсоток (за об’ємом) амоніаку в цій суміші.
Суміш азоту, нітроген(І) оксиду та нітроген(ІІ) оксиду об’ємом 264 мл пропустили через воду об’ємом 2 л. До 150 мл газів, які не поглинулися водою, добавили 48 мл кисню, після чого об’єм газів склав 165 мл. Усі виміри проводилися за однакових умов. Обчисліть об’ємну частку нітроген(І) оксиду у вихідній суміші (у %).
У скільки разів слід збільшити концентрацію водню в реакції утворення аміаку (амоніаку NH3) з простих речовин, щоб її швидкість зросла в 125 разів?
У результаті реакції між воднем і киснем у суміші цих газів об'ємом 42 мл об'єм суміші зменшився до 30 мл. Обчисліть об'єми газів у вихідній суміші, якщо після реакції вода знаходилась у пароподібному стані, а всі об'єми виміряні за однакових умов.
Варіант 2
Обчислити об’єм повітря, який необхідний для спалювання 1 м3суміші газів: 95% метану (СН4), 3% азоту, 1% етану (С2Н6) і 1% карбон(ІV) оксиду.
Є 6,3 г суміші сірки і фосфору, яку обробили надлишком концентрованої нітратної кислоти при нагріванні. У результаті реакції виділилося 24,64 л бурого газу (н.у.). Добутий газ пропустили через 949,4 г 6,5%-ного розчину калій гідроксиду. Які солі містяться в утвореному розчині і які їх масові частки? Визначити масові частки сірки і фосфору у вихідній суміші.
Визначити, як зміниться швидкість реакції утворення аміаку (амоніаку NH3) з простих речовин, якщо тиск у системі збільшити в 2 рази?
Пропускаючи через надлишок розжареного вуглецю кисень, одержали 232 л газоподібних продуктів, виміряних при t = 800C i p = 101,3 кПа. Густина одержаної суміші за воднем становила 17,2. Обчисліть об’єм кисню, що вступив у реакцію і склад (в % за об’ємом) утворених газів.
Варіант 3
До 5 л суміші вуглеводню (СхНу) й карбон(IV) оксиду додали 16 л кисню (н.у.) і суміш підпалили. Після реакції об’єм суміші складав 24 л, а після конденсації води – в два рази менше. Після цього її пропустили через розчин лугу і об’єм зменшився до 1 л. Визначте формулу вуглеводню.
При кип’ятінні розчину, який утворився в результаті змішування 10 г розчину лугу А з масовою часткою розчиненої речовини 20% і 40 г розчину солі Б з масовою часткою розчиненої речовини 10% у розчині залишається сіль В1і виділяється газ Г1. При термічному розкладі солі В1утворюється сіль В2і виділяється газ Г2. При нагріванні суміші В2і Б утворюється сіль В1, Н2О і газ Г3. При нагріванні солі Б можуть утворюватися різні продукти: при помірному нагріванні спостерігається виділення газу Г4з невеликими домішками Г5, можливий також розклад Б з вибухом з утворенням газів Г2, Г3та води. Газ Г5при певних умовах розкладається з утворенням газів Г4і Г6. Назвати всі речовини, написати рівняння всіх згаданих реакцій.
При синтезі фосгену СО + Cl2
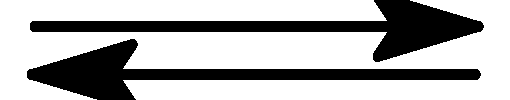 COCl2рівновага встановлюється
при таких концентраціях реагуючих
речовин (моль/л): С(Cl2) = 2,5; C(CO) =
1,8; C(COCl2) = 3,2. Визначте вихідні
концентрації карбон(ІІ) оксиду та
хлору.
COCl2рівновага встановлюється
при таких концентраціях реагуючих
речовин (моль/л): С(Cl2) = 2,5; C(CO) =
1,8; C(COCl2) = 3,2. Визначте вихідні
концентрації карбон(ІІ) оксиду та
хлору.Неон складається з двох ізотопів 20Nе i22Nе і має відносну атомну масу 20,2. Який об’єм у літрах (н.у.) припадає на ізотоп22Nе в 1 моль природного неону? Результат подайте з точністю до сотих.
