
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
4.6 Уравнение состояния двумерного газа.
В
двумерном газе действует поверхностное
давление, которое является растягивающим,
в противоположность поверхностному
натяжению, сжимающему поверхность.
Это давление равно
![]() .
При малом содержании ПАВ, т.е. в состоянии
двумерного газа
.
При малом содержании ПАВ, т.е. в состоянии
двумерного газа
![]() .
После дифференцирования получим:
.
После дифференцирования получим:
![]() (1)
(1)
Подставим уравнение (1) в уравнение Гиббса:
![]()
Площадь,
занимаемую одним молем ПАВ, обозначим
через
![]() .
Тогда
.
Тогда
![]() ;
;
![]() ;
;
![]() .
.
Это
уравнение состояния двумерного газа
аналогично уравнению газа
![]() .
.
Для реального двумерного газа справедливо уравнение Фрумкина, аналогичное уравнению Ван-дер Ваальса:
![]()
где - константа взаимодействия молекул ПАВ в поверхностном слое, - эффективная площадь сечения молекулы.
В конденсированных пленках молекулы ПАВ находятся в виде отдельных островков (жидкие пленки) или частокола Ленгмюра (твердые пленки).
4.7 Диаграммы состояния поверхностных пленок
Фазовое
состояние поверхностных пленок
описывается диаграммой состояния или
изотермой сжатия, которая может быть
построена в координатах
![]() .
.
Поверхностное давление измеряют непосредственно с помощью весов Ленгмюра. Этот метод основан на прямом измерении горизонтальной силы, которая действует на поплавок, отделяющий пленку от поверхности чистого растворителя. Современные весы позволяют определять поверхностные давления с точностью до сотых долей дины на см. В общем случае при уменьшении площади реализуются газообразное, жидкое и твердое состояние монослоя. Каждое состояние монослоя характеризуется определенной ориентацией молекул, зависящей от , адгезионных и когезионных свойств систем. В диапазоне давления и площади, занимаемой 1 молем ПАВ, отвечающем всем трем агрегатным состояниям пленки, диаграмма состояния имеет вид, показанный на рисунке 4.7.

Рис. 4.7. Диаграмма состояния поверхностных пленок.
Участок
соответствует двумерному газу и
аналогичен кривой сжатия газа. На участке
![]() происходит конденсация. В этом состоянии
пленка называется растянутой жидкой
пленкой и способна к сжатию, которому
соответствует участок
.
На участке
происходит фазовый переход, участку
происходит конденсация. В этом состоянии
пленка называется растянутой жидкой
пленкой и способна к сжатию, которому
соответствует участок
.
На участке
происходит фазовый переход, участку
![]() соответствует конденсированная
(твердая) пленка. Участку
соответствует разрушение мономолекулярной
пленки, т. е. образование капли для жидкой
пленки или многослойных образований
для твердой пленки. Поверхностные пленки
реальных ПАВ описываются диаграммами
состояния, отвечающими определенному
участку общей диаграммы состояния. Это
зависит от длины углеводородного
радикала молекулы ПАВ. Так, лауриновая
кислота
соответствует конденсированная
(твердая) пленка. Участку
соответствует разрушение мономолекулярной
пленки, т. е. образование капли для жидкой
пленки или многослойных образований
для твердой пленки. Поверхностные пленки
реальных ПАВ описываются диаграммами
состояния, отвечающими определенному
участку общей диаграммы состояния. Это
зависит от длины углеводородного
радикала молекулы ПАВ. Так, лауриновая
кислота
![]() благодаря сравнительно короткому
радикалу образует только газообразные
пленки (кривые 1, 2, 3, рис.4.8).
благодаря сравнительно короткому
радикалу образует только газообразные
пленки (кривые 1, 2, 3, рис.4.8).
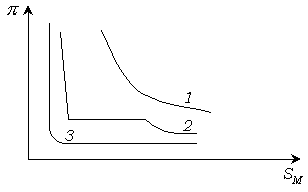
Рис.7
Рис. 4.8. Диаграммы состояния поверхностных пленок лауриновой (1), миристиновой (2) и пальмитиновой (3) кислот.
Миристиновая
кислота
![]() образует как газообразные, так и
конденсированные пленки. Пальмитиновая
кислота
образует как газообразные, так и
конденсированные пленки. Пальмитиновая
кислота
![]() при обычной температуре образует только
конденсированные пленки вследствие
большой длины углеводородного радикала.
при обычной температуре образует только
конденсированные пленки вследствие
большой длины углеводородного радикала.
4.8 Химические реакции в поверхностных пленках.
Поверхностные пленки обладают электрическим зарядом, который влияет на химические реакции, идущие по ионному механизму. К таким реакциям относится большинство жизненно важных биохимических каталитических реакций (ферментативный синтез, протеолиз, лактонизация кислот, омыление жиров).
Введение в поверхностную пленку веществ, вызывающее изменение величины или знака ее электрического потенциала, может изменить скорость химической реакции в пленках на несколько порядков. Заряд поверхности изменяет свою величину, и знак при переходе от пленок жирных кислот к пленкам, которые образуют их соли (рис.4.9)
Пленки жирных кислот, спиртов, сложных эфиров со стороны газовой фазы обладают положительным зарядом вследствие избытка электронной плотности на атомах кислорода (рис. 4.9)

Рис. 4.9.
Соли жирных кислот образуют отрицательно заряженные пленки, так как диполь карбоксильной группы перекрывается большим по величине и противоположным по направлению диполем ионной пары.
Для
кислот значения электронного потенциала
поверхности резко уменьшается, и затем
изменяют свой знак с увеличением
![]() раствора (рис.4.10 кривая 1)
раствора (рис.4.10 кривая 1)

Рис. 4.10
Для
спиртов значения
![]() уменьшаются в щелочной области в связи
с образованием алкоголятов (кривая 2),
а для сложных эфиров значение потенциала
поверхности не зависит от
(прямая 3).
уменьшаются в щелочной области в связи
с образованием алкоголятов (кривая 2),
а для сложных эфиров значение потенциала
поверхности не зависит от
(прямая 3).
