
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
1.2. Краткие исторические сведения
Среди химических наук коллоидная химия является сравнительно молодой, хотя коллоиды или коллоидные системы существуют извечно. Однако, изучение коллоидных систем началось только в XIX веке. Понятие о коллоидах возникло в 60-х годах XIX века, когда неорганическая, органическая и физическая химия были уже сформировавшимися науками. В частности, в 1861 году Бутлеровым была создана теория строения органических соединений.
В 1845 году итальянский химик Франческо Сельми, работавший в городе Болонья, получил растворы, обладающие особыми свойствами. В этих растворах медленно протекает диффузия, они не проходят сквозь тонкие пергаментные фильтры, сходящийся пучок света образует в них светящийся конус. Малейшие воздействия (перемешивание, добавление электролита) вызывают образование осадка, которое протекает без выделения заметных количеств тепла и без изменения объема системы. Это свидетельствует об отсутствии химической реакции. Сельми назвал эти растворы золями. Он получил золи серы, сернистого мышьяка, хлористого серебра. Фарадей разработал методы получения золей благородных металлов - золота и серебра. Полученные Фарадеем свыше 100 лет назад золи золота и серебра до сих пор хранятся в Лондонском музее.
Название «коллоиды» было предложено английским ученым Т. Грэмом в 1861 году и происходит от греческого слова «колла» () - клей. Грэм исследовал в основном золи органического происхождения, образующие при некоторой концентрации студневидные растворы с клеящими свойствами. К ним относятся желатин, крахмал, клей.
Становление коллоидной химии как области знания произошло тогда, когда физики и химики обратили внимание на особые свойства поверхности раздробленных, т.е. дисперсных тел. Поверхность, ранее считавшаяся лишь внешней частью предмета или тела, в науке о коллоидах предстала в виде площади, заселенной открытыми атомами.
1.3. Предмет коллоидной химии
Физическая химия интересуется преимущественно объемными свойствами фаз и изучает в основном индивидуальные вещества или истинные растворы, которые являются гомогенными системами. Двухфазные системы, изучаемые физической химией, состоят из фаз большой протяженности, в которых значение поверхности невелико. Коллоидная химия изучает поверхностные явления и гетерогенные высокодисперсные системы. Они занимают промежуточное положение между грубыми дисперсиями и истинными растворами. Если одно вещество диспергировано в другом в виде частиц, можно выделить три типа систем, размер которых убывает в ряду: грубодисперсные > микрогетерогенные > ультрадисперсные (коллоидные). Эти системы по меньшей мере двухфазны. Напомним, что фаза - совокупность частей системы, одинаковых по составу, физическим и химическим свойствам и отделенная от других частей системы поверхностью раздела. Если система содержит множество частиц одного сорта, распределенных в какой-либо среде, то такая система двухфазна.
Правильнее говорить не о геометрической поверхности, а о поверхностном слое, в котором осуществляется межфазное взаимодействие. Межфазный слой всегда снижает разность энергии фаз. Толщина этого слоя определяется радиусом действия межмолекулярных сил. Поверхностный и межфазный слой сосуществуют с объемными фазами, имеют свою фазовую диаграмму, фазовые переходы и термодинамические функции. Понятие о поверхностном или межфазном слое введено в науку Гиббсом.
Фаза, состоящая из отдельных частиц, называется дисперсной фазой. Она прерывиста, дискретна. Другая фаза, в которой распределены частицы, называется дисперсионной средой. Она является непрерывной, сплошной.
Коллоидная химия изучает особые, ультрадисперсные, т. е. сильно раздробленные вещества. Коллоидная химия имеет дело главным образом не с молекулами, а с их агрегатами.
Коллоидная химия - это наука о поверхностных явлениях и гетерогенных дисперсных системах. Две части этого определения, т. е. поверхностное явления и дисперсные системы, тесно связаны между собой. Рассмотрим причины этой взаимосвязи.
Объектами коллоидной
химии могут быть тела любой величины,
однако поверхностные явления проявляются
сильнее всего в высокодисперсных
системах: пленках, нитях, капиллярах,
мелких частицах. В этих системах наиболее
ярко проявляется все многообразие
поверхностных явлений. Это происходит
оттого, что с увеличением раздробленности
вещества возрастает доля молекул,
находящихся на поверхности. Зависимость
доли молекул, находящихся на поверхности
частицы кубической формы, от длины ребра
куба, проходит через максимум, расположенный
при
![]() (рис. 1.1). Для частицы с длиной ребра
(рис. 1.1). Для частицы с длиной ребра
![]() ,
на котором помещается
,
на котором помещается
![]() молекул, доля молекул, находящихся на
поверхности, составляет всего
молекул, доля молекул, находящихся на
поверхности, составляет всего
![]() ,
а для частицы с
,
а для частицы с
![]() (на ребре
(на ребре
![]() молекул), доля этих молекул составляет
молекул), доля этих молекул составляет
![]() .
Частицы таких размеров содержат около
половины всех молекул на поверхности,
следовательно, поверхность даже
количественно становится полноправным
партнером объемной фазы и значение
поверхностных явлений для систем,
содержащих такие частицы, очень велико.
.
Частицы таких размеров содержат около
половины всех молекул на поверхности,
следовательно, поверхность даже
количественно становится полноправным
партнером объемной фазы и значение
поверхностных явлений для систем,
содержащих такие частицы, очень велико.
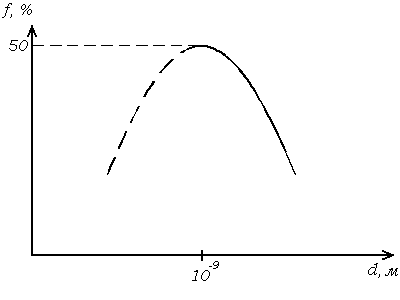
Рис. 1.1. Зависимость доли молекул, находящихся на поверхности куба, от длины ребра.
Величина поверхности
в реальных сильно раздробленных системах,
к которым относятся все композиционные
материалы, очень велика. Так, в небольшом
объеме армированного волокном пластика,
величиной
![]() ,
содержащего
,
содержащего
![]() объемных % волокна
объемных % волокна
![]() ,
поверхность раздела между волокном и
связующим равна
,
поверхность раздела между волокном и
связующим равна
![]() .
.
