
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
3.3. Типы адсорбционных зависимостей
С термодинамической точки зрения процессы адсорбции на различных границах раздела фаз не отличаются друг от друга. Наблюдаемые различия относятся к структуре адсорбционного слоя и механизму процесса адсорбции.
Основным законом, определяющим поведение компонентов при адсорбции, является закон распределения Нернста-Шилова . Величина адсорбции компонентов зависит от теммпературы и концентрации или давления.
![]()
Поэтому различают
следующие виды адсорбционных зависимостей:
или
при
![]() - изотерма адсорбции;
при
- изотерма адсорбции;
при
![]() - изобара адсобции и
- изобара адсобции и
![]() или
или
![]() - изостера адсорбции
- изостера адсорбции
Различают три вида адсорбции на различных поверхностях раздела: газа с твердым телом, раствора с твердым телом и раствора с газом.
3.4. Адсорбция газов и паров на твердом теле
Это простейший случай, удобный для теоретического рассмотрения, т.к. в адсорбционном процессе участвуют только два компонента. Когда газ или пар приводятся в контакт с чистой твердой поверхностью, некоторое количество их связывается с поверхностью в форме адсорбционного слоя. Твердое тело является адсорбентом, а газ или пар - адсорбатом. Одновременно может наблюдаться поглощение газа объемом твердого тела, т.е. абсорбция.
Степень адсорбции в состоянии равновесия зависит от температуры, давления газа и эффективной поверхности адсорбента. Поэтому лучшими адсорбентами являются высокопористые вещества, такие как активированный уголь и силикагель. Их удельная поверхность достигает 1000 м2/г. Зависимость между равновесным количеством адсорбированного газа при данной температуре и давлением газа называется изотермой адсорбции.
Адсорбция уменьшает небаланс сил притяжения, которые существуют на поверхности и, следовательно, свободную поверхностную энергию гетерогенной системы. Основное различие между твердыми и жидкими поверхностями заключается в том, что твердая поверхность неоднородна по активности и свойства ее в некоторой степени зависят от предыстории поверхности.
3.5. Адсорбция как обратимый экзотермический процесс
В адсорбционном слое
молекулы газа способны к перемещению
лишь в двух измерениях, поэтому адсорбция
газа сопровождается уменьшением
энтропии, т.е.
![]() .
Условием протекания адсорбции как
самопроизвольного процесса является
уменьшение энергии Гиббса, т. е.
.
Условием протекания адсорбции как
самопроизвольного процесса является
уменьшение энергии Гиббса, т. е.
![]() .
Из термодинамической зависимости
.
Из термодинамической зависимости
![]() следует, что теплота адсорбции должна
быть отрицательной, т. е. адсорбция газов
или паров на твердом теле всегда является
экзотермическим процессом. Поэтому
степень адсорбции газа в равновесных
условиях увеличивается с понижением
температуры. Теплота адсорбции может
быть определена прямым калориметрическим
методом и рассчитана из обратимой
изотермы адсорбции по уравнению
Менделеева-Клаузиуса-Клайперона
следует, что теплота адсорбции должна
быть отрицательной, т. е. адсорбция газов
или паров на твердом теле всегда является
экзотермическим процессом. Поэтому
степень адсорбции газа в равновесных
условиях увеличивается с понижением
температуры. Теплота адсорбции может
быть определена прямым калориметрическим
методом и рассчитана из обратимой
изотермы адсорбции по уравнению
Менделеева-Клаузиуса-Клайперона
![]()
Причиной выделения тепла при адсорбции является уменьшение энергии поверхности адсорбента.
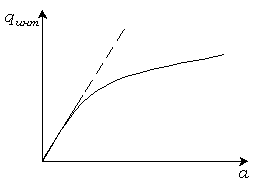
Рис. 3.1. Зависимость теплоты адсорбции от величины адсорбции.
Различают дифференциальную
и интегральную
теплоту адсорбции. Интегральная
теплота адсорбции - это общее количество
тепла, выделившееся при адсорбции
данного количества адсорбата на 1 кг
адсорбента
![]()
![]() ;
;
![]()
![]() .
Зависимость интегральной теплоты
адсорбции от величины адсорбции нелинейна
(рис. 3.1), т. к. поверхность адсорбента
энергетически неоднородна. Вначале
адсорбция идет на более активных центрах,
и выделяется больше тепла, затем
количество выделяющегося тепла снижается.
.
Зависимость интегральной теплоты
адсорбции от величины адсорбции нелинейна
(рис. 3.1), т. к. поверхность адсорбента
энергетически неоднородна. Вначале
адсорбция идет на более активных центрах,
и выделяется больше тепла, затем
количество выделяющегося тепла снижается.
Дифференциальная
теплота адсорбции - это тепло, выделившееся
при дополнительной адсорбции малого
количества адсорбата в расчете на моль
адсорбата
![]() .
Дифференциальная теплота адсорбции
характеризует не весь адсорбционный
процесс, а некоторую его стадию, для
которой адсорбция достигла величины
.
Дифференциальная теплота адсорбции с
увеличением количества адсорбированного
вещества уменьшается (рис. 3.2). В первую
очередь газ адсорбируется наиболее
активными участками поверхности, и при
этом выделяется наибольшее количество
тепла. По мере насыщения активных центров
адсорбция происходит на менее активных
участках поверхности.
.
Дифференциальная теплота адсорбции
характеризует не весь адсорбционный
процесс, а некоторую его стадию, для
которой адсорбция достигла величины
.
Дифференциальная теплота адсорбции с
увеличением количества адсорбированного
вещества уменьшается (рис. 3.2). В первую
очередь газ адсорбируется наиболее
активными участками поверхности, и при
этом выделяется наибольшее количество
тепла. По мере насыщения активных центров
адсорбция происходит на менее активных
участках поверхности.
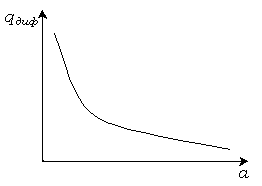
Рис. 3.2. Зависимость дифференциальной теплоты адсорбции от величины адсорбции.
При физической адсорбции значения теплоты адсорбции невелики. Так, значения дифференциальной теплоты адсорбции не превышает 10 ккал/моль. Поэтому адсорбция является обратимым процессом, находящимся в равновесии с обратным процессом десорбции: Адсорбция Десорбция
Причиной адсорбции являются межмолекулярные силы, причиной десорбции - тепловое движение молекул.

Рис. 3.3. Влияние температуры на изотерму адсорбции.
Так как адсорбция обратима, то она подчиняется правилу Ле Шателье1. При повышении температуры процесс сдвигается в сторону десорбции, идущей с поглощением тепла, т. е. адсорбция уменьшается. Адсорбция имеет отрицательный температурный коэффициент. С повышением температуры равновесные значения адсорбции уменьшаются. Изотермы адсорбции при высокой температуре расположены ниже изотермы, соответствующей более низкой температуре (рис. 3.3)
Адсорбция возрастает с увеличением теплоты адсорбции в соответствии с уравнением:
![]()
где
![]() - константа равновесия адсорбции,
- теплота адсорбции.
- константа равновесия адсорбции,
- теплота адсорбции.
