
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
6.13. Смеси ионных и неионных пав
Ионные и неионные ПАВ обладают различной растворимостью и критической концентрацией мицеллообразования (ККМ). ККМ в смесях ИПАВ и НПАВ не является аддитивной величиной, проявляется синергизм действия. На рис. 6.8 показано взаимное влияние ИПАВ – алкилсульфата натрия С18 и НПАВ – синтанола ДС-10 на ККМ в перхлорэтилене.
Ас-алкилсульфонат натрия С18
ДС-синтанол ДС-10
Композиции ИПАВ и НПАВ применяются в эмульсионной полимеризации. Снижение ККМ позволяет уменьшить количество применяемого эмульгатора. Это важно не только с экономической точки зрения, т. к. удешевляет технологию, но и с экологической точки зрения, т. к. снижает загрязнение сточных вод.
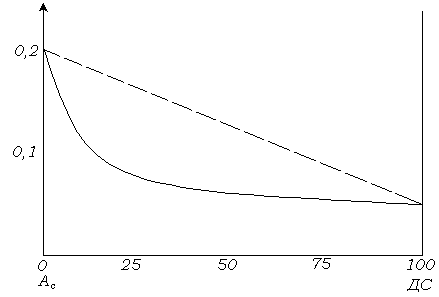
Рис. 6.8. Взаимное влияние алкилсульфата натрия С18 и синтанола ДС-10 на ККМ в перхлорэтилене.
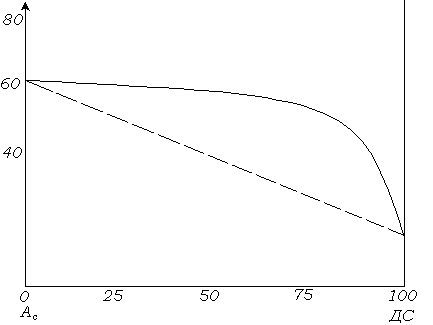
Рис. 6.9. Влияние состава бинарной смеси ПАВ на моющее действие в перхлорэтилене.
6.14. Контрольные вопросы
Отличие коллоидных ПАВ от низкомолекулярных ПАВ
Общая характеристика и применение коллоидных ПАВ
Классификация коллоидных ПАВ
Как зависит биоразлогаемость ПАВ от строения молекулы?
Приведите примеры анионных, катионных, амфолитных и неионных ПАВ
Свойства водных растворов ПАВ.
Зависимость растворимости ИПАВ от температуры. Точка Крафта.
Зависимость растворимости НПАВ от температуры. Точка помутнения и высаливания.
Гидрофильный-липофильный баланс как характеристика ПАВ.
Термодинамика образования прямых и обратных мицелл.
Строение мицелл коллоидных ПАВ.
Солюбилизация мицеллами углеводородов в водной среде и воды в углеводородной среде.
Микроэмульсии. Мицеллярный катализ.
Основные факторы моющего действия растворов коллоидных ПАВ.
VII. Получение дисперсных систем
7.1. Введение
Дисперсные системы занимают промежуточное положение между макроскопическими гетерогенными системами и молекулярными растворами - гомогенными системами. Это позволяет получать дисперсные системы двумя путями: диспергированием макроскопических фаз (диспергационный путь образования) и конденсацией из истинных растворов или однокомпонентных гомогенных систем (конденсационное образование). В большинстве случаев образование дисперсных систем требует затраты работы, либо подводимой из вне, например в виде механической энергии, либо за счет протекания внутренних, в частности химических, процессов в самой системе. Возникшие таким образом дисперсные системы являются термодинамически неравновесными и требуют для своего сколько-нибудь длительного существования специальной стабилизации. Их называют лиофобными.
Существуют также дисперсные системы способные возникать в результате самопроизвольного (т.е. без затраты подводимой из вне механической работы) диспергирования макроскопоческой фазы. Такие системы термодинамически равновесны и не нуждаются в дополнительной стабилизации. Их называют лиофильными. К ним относятся растворы высокомолекулярных соединений, мицелярные растворы поверхностно-активных веществ. Основным свойством лиофобных дисперсных систем, как уже отмечалось, является их термодинамическая неустойчивость. Она связана с большим запасом свободной поверхностной энергии на развитой межфазной поверхности. Наличие большой поверхностной энергии обусловлено коллоидным состоянием, точнее высокой дисперсностью и гетерогенностью системы, что следует из фундаментального уравнения Гиббса для гетерогенных систем. При постоянных температурах и составе поверхностная энергия определяется произведением поверхностного натяжения на площадь поверхности :
![]() (7.1)
(7.1)
Поэтому в них самопроизвольно происходит процесс слипания частиц дисперсной фазы – коагуляция.
Для придания устойчивости против слипания – агрегативной устойчивости – необходимо создавать на поверхности частиц защитные слои: двойные электрические слои, приводящие к возникновению электростатического отталкивания (ионно-электростатический фактор устойчивости). Этот фактор реализуется при введении в коллоидную систему электролитов, имеющих в своем составе один из ионов, входящих в состав агрегата дисперсной фазы коллоидной системы или изоформный ему.
При введении в коллоидную систему поверхностно-активных веществ и высокомолекулярных соединений образуются сольватные или адсорбционно-сольватные слои, которые в силу своих особых структурно-механических свойств препятствуют соприкосновению и слипанию частиц (структурный фактор устойчивости)
