
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
1.4. Физические и химические поверхностные явления
Поверхностные явления чрезвычайно распространены и могут иметь физическую и химическую природу.
К физическим поверхностным явлениям и процессам относятся капиллярные явления на поверхности капли или пузырька, изотермическая перегонка, смачивание, коалесценция, коагуляция, а в твердых телах - когезия, адгезия, трение. В качестве примера физического поверхностного явления можно привести существование капиллярного давления на поверхности капли или пузырька, вызванного кривизной поверхности. Поверхность жидкости состоит из молекул, находящихся в несимметричном силовом поле. Притяжение со стороны жидкости не компенсируется притяжением со стороны менее плотной фазы - пара. Равнодействующая межмолекулярных сил, действующих на одну молекулу, не равна нулю и направлена в сторону более плотной фазы - жидкости (рис. 1.2).
Равнодействующая всех
сил, направленная нормально к поверхности
и рассчитанная на
![]() ,
называется молекулярным или внутренним
давлением, которое измеряется в
,
называется молекулярным или внутренним
давлением, которое измеряется в
![]() или
или
![]() .
Для полярных жидкостей внутреннее
давление очень велико. Для воды оно
превышает
.
Для полярных жидкостей внутреннее
давление очень велико. Для воды оно
превышает
![]() (гигапаскаля),
что соответствует 11 тыс. атмосфер.
(гигапаскаля),
что соответствует 11 тыс. атмосфер.
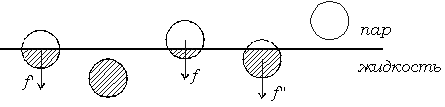
Рис. 1.2. Межмолекулярные взаимодействия в конденсированной фазе.
Наличие кривизны
приводит к изменению внутреннего
давления. При вогнутой поверхности (![]() )
внутреннее давление будет меньше, а при
выпуклой (
)
внутреннее давление будет меньше, а при
выпуклой (![]() )
больше, чем в случае плоской поверхности.
Величина
)
больше, чем в случае плоской поверхности.
Величина
![]() ,
равная разности давлений в соседних
фазах, разделенных искривленной
поверхностью, называется капиллярным
давлением. По закону Лапласа
,
равная разности давлений в соседних
фазах, разделенных искривленной
поверхностью, называется капиллярным
давлением. По закону Лапласа
![]() .
В зависимости от знака кривизны
капиллярное давление может увеличивать
или уменьшать внутреннее давление.
.
В зависимости от знака кривизны
капиллярное давление может увеличивать
или уменьшать внутреннее давление.
По величине поднятия или опускания жидкости в капиллярах можно определять поверхностное натяжение жидкостей, которое рассчитывается по формуле Жюрена:
![]() (3.1.)
(3.1.)
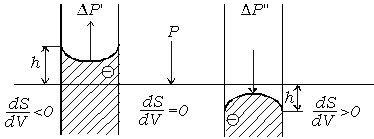
Рис. 1.3. Капиллярное давление
Капиллярное давление проявляется при сушке влажных дисперсных структур. У искривленной поверхности изменяется химический потенциал, что приводит к увеличению давления насыщенного пара над выпуклой поверхностью жидкой капли и его уменьшению над вогнутой поверхностью. Изменение давления насыщенного пара описывается уравнением Томсона - (Кельвина):
![]() ;
;
![]() , (3.2)
, (3.2)
где
![]() и
и
![]() - давление насыщенного пара над ровной
и искривленной поверхностью,
- давление насыщенного пара над ровной
и искривленной поверхностью,
![]() - мольный объем
жидкости.
- мольный объем
жидкости.
Величина
![]() характеризует кривизну поверхности
сферической частицы. Чем больше кривизна,
тем легче молекулы отрываются от
поверхности и интенсивнее протекает
испарение капель. Вследствие этого над
мелкими каплями упругость пара больше,
чем над крупными. Поэтому в атмосфере
насыщенного пара мелкие капли переходят
в крупные вследствие изотермической
перегонки. Изменение химического
потенциала вследствие кривизны
поверхности приводит к росту растворимости
с увеличением дисперсности, которое
описывается уравнением
Гиббса-Фрейндлиха-Оствальда:
характеризует кривизну поверхности
сферической частицы. Чем больше кривизна,
тем легче молекулы отрываются от
поверхности и интенсивнее протекает
испарение капель. Вследствие этого над
мелкими каплями упругость пара больше,
чем над крупными. Поэтому в атмосфере
насыщенного пара мелкие капли переходят
в крупные вследствие изотермической
перегонки. Изменение химического
потенциала вследствие кривизны
поверхности приводит к росту растворимости
с увеличением дисперсности, которое
описывается уравнением
Гиббса-Фрейндлиха-Оствальда:
![]() (3.3)
(3.3)
Вследствие этого растворимость мелких твердых частиц больше, чем крупных. Происходит процесс растворения мелких частиц и рекристаллизации их на крупных, то есть изотермическая переконденсация, описываемая уравнением:
![]() (3.4)
(3.4)
При спекании металлических порошков происходит постепенная ликвидация пор. Над малой порой повышена концентрация микропустот (вакансий) в частицах. Это приводит к их диффузии от малых пор к большим и к поверхности раздела металла с воздухом. Под действием лапласовых сил поры исчезают, заполняются металлом. Этот процесс сопровождается уменьшением поверхности раздела фаз.
Другими примерами физических поверхностных явлений являются смачивание и, как следствие этого, существование вогнутого и выпуклого менисков жидкости и перемещение жидкости в капилляре. В дисперсных системах смачивание уменьшает взаимодействие частиц. Если частицы имеют ультрамикроскопические размеры, то смачивание способствует образованию золей. Когда частица достаточно велика и оседает, смачивание способствует скольжению частиц друг относительно друга, приводя к более плотной упаковке осадка. Если смачивание неполное, то при взаимодействии частиц происходит преобразование пространственных структур (каркасов и рыхлых осадков).
При смачивании процесс сопровождается изменением свойств поверхности. Поверхность твердое тело - газ заменяется поверхностью твердое тело - жидкость, поверхностное натяжение уменьшается.
К физическим поверхностным явлениям относятся также образование и рост зародышей в растворе и диспергирование.
Примерами химических поверхностных явлений являются адсорбция и коррозия. Тончайшие слои адсорбированного вещества изменяют свойства поверхности - ее смачивание, возможность взаимодействия с другими веществами. В коллоидных системах, обладающих большой поверхностью, роль адсорбции особенно велика. При адсорбции на поверхность из объемной фазы диффундирует тот компонент, который уменьшает поверхностное натяжение.
Рассмотрение этих примеров показывает, что все поверхностные явления протекают с уменьшением поверхности или поверхностного натяжения.
