
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
9.7. Турбидиметрический метод определения коллоидных частиц.
9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
Размер частиц можно определить двумя методами: нефелометрическим и турбидиметрическим. Методом нефелометрии измеряют непосредственно интенсивность света, рассеянного под некоторым углом к падающему лучу света. Методом турбодиметрии измеряют ослабление интенсивности света, проходящего через дисперсную систему. Метод турбидиметрии основан на том, что при прохождении света через коллоидный раствор, содержащий малые прозрачные частицы, поглощение практически отсутствует и ослабление интенсивности падающего света равно полной интенсивности света, рассеянного коллоидным раствором во всех направлениях (полное светорассеяние). Для систем, содержащих частицы с размерами значительно меньше длины световой волны, величина полного светорассеяния подчиняется уравнению Рэлея. В этом случае, измерив фотометром или колориметром ослабление интенсивности падающего света и воспользовавшись уравнением Рэлея, можно определить средний размер частиц.
Рассмотрим поглощение
света 1 см3
вещества, то
есть
![]() ,
,
тогда уравнение примет вид:
,
,
тогда уравнение примет вид:

Рис. 9.5.
![]() ;
;
![]() (9.11)
(9.11)
Закон сохранения энергии в данном случае приводит к равенству:
![]() (9.12)
(9.12)
где
,
![]() ,
– интенсивности соответственно
прошедшего, рассеянного и падающего
света.
,
– интенсивности соответственно
прошедшего, рассеянного и падающего
света.
Преобразуем это уравнение, поделив на :
![]() (9.13)
(9.13)
![]() (9.14)
(9.14)
где – мутность.
![]() (9.15)
(9.15)
![]() (9.16)
(9.16)
С другой стороны
![]() ,
следовательно,
,
следовательно,
![]() (9.17).
(9.17).
Запишем уравнение в общем виде:
![]()
Выразим через оптическую плотность:
![]() ;
;
![]() (9.18)
(9.18)
Для дисперсных систем со сферическими частицами уравнение Рэлея можно записать в таком виде:
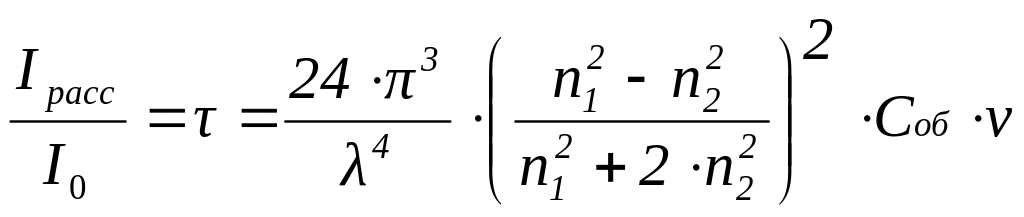 (9.19)
(9.19)
где
- полная интенсивность света, рассеянного
1 см3
системы;
![]() – объемная доля дисперсной фазы;
– объемная доля дисперсной фазы;
![]() – объем частицы, см3.
– объем частицы, см3.
Отсюда можно вычислить объем частиц:
![]() (9.20)
(9.20)
где
 (9.21)
(9.21)
Уравнение Рэлея
справедливо лишь для разбавленных
растворов, так как оно не учитывает
вторичного рассеяния света и взаимодействия
между частицами. Поэтому для определения
размера частиц следует найти
для ряда растворов с разной кратностью
разбавления и экстраполировать величину
![]() до
до
![]() .
.
![]() (9.22)
(9.22)
Весьма удобным объектом исследования оптических свойств коллоидных систем являются латексы, представляющие модель гидрофобных золей. Они являются двухфазными и трехкомпонентными системами, состоящими из полимерных частиц ультрамикроскопических размеров, взвешенных в серуме – водном растворе стабилизатора. В качестве стабилизатора применяют различные поверхностно-активные вещества (соли жирных и сульфокислот).
9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
Интенсивность света, рассеянного разбавленной дисперсной системой, а также угловое распределение рассеянного света (индикатрисса рассеяния) зависят от значений двух безразмерных параметров и . Параметр характеризует отклонение свойств частицы от свойств среды и определяется уравнением
![]() (9.23)
(9.23)
где
![]() - отношение показателя преломления
дисперсной фазы к показателю преломления
дисперсионной среды.
- отношение показателя преломления
дисперсной фазы к показателю преломления
дисперсионной среды.
Параметр характеризует отношение радиуса частицы к длине волны :
![]() (9.24)
(9.24)
Для частиц, размер
которых не превышает
![]() длины волны падающего света, при условии
отсутствия поглощения света и вторичного
светорассеяния справедливо уравнение
Рэлея.
длины волны падающего света, при условии
отсутствия поглощения света и вторичного
светорассеяния справедливо уравнение
Рэлея.
Для частиц, размер которых равен длине световой волны или больше ее, определение размеров частиц по светорассеянию может быть осуществлено исходя из общей теории своторассеяния.
В случае, когда радиус
составляет от одной десятой до одной
третьей длины световой волны, и показатели
преломления частиц и среды не слишком
различаются (![]() ),
определение размеров частиц дисперсных
систем проводят по методу К. С. Шифрина
и И. Я. Слонима. Согласно этому методу,
мутность зависит от параметров
и
следующим образом:
),
определение размеров частиц дисперсных
систем проводят по методу К. С. Шифрина
и И. Я. Слонима. Согласно этому методу,
мутность зависит от параметров
и
следующим образом:
![]() (9.25)
(9.25)
а при
![]()
![]() (9.26)
(9.26)
где
– мутность системы, см-1;
– объемная доля дисперсной фазы;
![]() – характеристическая мутность.
– характеристическая мутность.
При
![]() (т. е.
(т. е.
![]() )
можно использовать уравнение Рэлея
(частицы видны в микроскоп).
)
можно использовать уравнение Рэлея
(частицы видны в микроскоп).
Зависимость мутности от параметра описывается уравнением
![]() (9.27)
(9.27)
Значение показателя
степени
в этом уравнении в свою очередь зависит
от
;
с увеличением
значение
уменьшается, стремясь в пределе к 2 для
частиц, радиус которых больше длины
волны. При малых значениях
соблюдается уравнение Рэлея и при
![]() .
.
Исходя из теории Шифрина, можно определить размер частиц по характеристической мутности. Для этого измеряют значение оптической плотности серии разбавленных растворов и вычисляют мутность по уравнению:
(9.28)
С помощью графической
экстраполяции находят значение
характеристической мутности. Подставляя
найденное значение
,
а также значение
и
в формулу (9.26), определяют значение
![]() и по таблице значение
.
По уравнению (9.24) вычисляют радиус
частицы.
и по таблице значение
.
По уравнению (9.24) вычисляют радиус
частицы.
С увеличением размеров частиц закон Рэлея перестает соблюдаться и интенсивность рассеянного света становится обратно пропорциональной длине волны в степени меньшей, чем четвертая. Если размер (диаметр) частиц составляет от 1/10 до 1/3 длины световой волны, и показатели преломления частиц и среды не сильно различаются, для описания светорассеяния в системе можно воспользоваться эмпирическим уравнением, предложенным Геллером:
![]() и
и
![]() (9.29)
(9.29)
где и – константы, не зависящие от длины волны.
Зависимость
![]() (или
(или
![]() )
от
)
от
![]() в соответствии с уравнением
и
представляет собой прямую линию, тангенс
угла наклона которой равен показателю
степени
с минусом. Значение показателя
в этих уравнениях зависит от соотношения
между размером частиц и длиной волны
падающего света, характеризуемого
параметром
.
в соответствии с уравнением
и
представляет собой прямую линию, тангенс
угла наклона которой равен показателю
степени
с минусом. Значение показателя
в этих уравнениях зависит от соотношения
между размером частиц и длиной волны
падающего света, характеризуемого
параметром
.
Показатель степени
в уравнениях
и
находят на основе турбидиметрических
данных. Для этого экспериментально
измеряют оптическую плотность системы
при различных длинах волн и строят
график зависимости в координатах
![]() .
Показатель
определяют по тангенсу угла наклона
полученной прямой. По значению
находят соответствующее значение
параметра
,
а затем по формуле
.
Показатель
определяют по тангенсу угла наклона
полученной прямой. По значению
находят соответствующее значение
параметра
,
а затем по формуле
![]() рассчитывают средний радиус частиц
исследуемой дисперсной системы.
рассчитывают средний радиус частиц
исследуемой дисперсной системы.
Следует отметить, что этот метод, как и уравнение Рэлея, применим только для «белых» золей, то есть для дисперсных систем, не поглощающих свет (метод базируется только на светорассеянии).
