
- •I. Введение
- •1.1. Место коллоидной химии в общей системе наук
- •1.2. Краткие исторические сведения
- •1.3. Предмет коллоидной химии
- •1.4. Физические и химические поверхностные явления
- •1.5. Основные признаки объектов коллоидной химии
- •1.6. Фундаментальные особенности ультрадисперсного (коллоидного) состояния вещества
- •1.7. Влияние дисперсности на свойства вещества
- •1.8. Значение коллоидной химии в природе и технике
- •II. Поверхностные явления и адсорбция
- •2.1. Классификация поверхностных явлений
- •2.2. Основы термодинамики поверхностного слоя
- •2.3. Интенсивные свойства гетерогенных систем
- •2.4. Экстенсивные свойства гетерогенных систем
- •2.5. Метод избыточных величин Гиббса
- •2.8. Уравнение Гиббса для плоского поверхностного слоя
- •2.9. Понятие об адсорбции
- •III. Адсорбция на различных границах раздела
- •3.1. Понятие об адсорбции
- •3.2 Количественные характеристики адсорбции
- •3.3. Типы адсорбционных зависимостей
- •3.4. Адсорбция газов и паров на твердом теле
- •3.5. Адсорбция как обратимый экзотермический процесс
- •3.6. Физическая адсорбция и хемосорбция
- •3.7. Значение координационных связей при хемосорбции
- •3.8. Природа адсорбционных сил
- •3.9. Изотермы адсорбции
- •3.10. Кинетика адсорбции
- •3.11. Классическая теория адсорбции
- •3.11.1. Теория мономолекулярной адсорбции Ленгмюра
- •Вывод уравнения Ленгмюра.
- •Анализ уравнения Ленгмюра
- •Полимолекулярная (потенциальная) теория адсорбции Поляни
- •3.11.3. Теория Брунауэра, Эииета и Теллера (бэт).
- •3.11.4. Схема полимолекулярной адсорбции
- •4.1 Поведение растворенных веществ на границе раствора с газом
- •4.2 Поверхностная активность.
- •4.3 Поверхностно – инактивные вещества
- •4.4 Вывод адсорбционного уравнения Гиббса
- •4.5 Строение адсорбционного слоя пав на границе раствора с газом
- •4.6 Уравнение состояния двумерного газа.
- •4.7 Диаграммы состояния поверхностных пленок
- •4.8 Химические реакции в поверхностных пленках.
- •4.9 Самоорганизованные монослои и пленки, перенесенные на твердую подложку с поверхности вода-воздух (пленки Ленгмюра –Блоджетт).
- •4.10 Двухсторонние пленки
- •4.11 Вид изотермы поверхностного натяжения. Уравнение Шишковского
- •4.12 Связь уравнений Ленгмюра и Гиббса с помощью уравнения Шишковского
- •4.13 Вывод уравнения Ленгмюра при совместном решении уравнений Гиббса и Шишковского
- •4.14 Правило Траубе
- •V. Адсорбция на границе раздела твердое тело – раствор
- •5.1. Введение
- •5.2. Правило вытеснения
- •5.3. Когезия и адгезия
- •5.4. Смачивание и растекание
- •5.5. Практическое значение смачивания
- •5.6. Правило выравнивания полярностей
- •5.7. Адсорбция полимеров из растворов на твердой поверхности
- •VI. Коллоидные пав
- •6.1. Введение
- •6.2. Производство и применение пав
- •6.3. Биоразлагаемость и токсичность
- •6.4. Классификация и общая характеристика пав
- •6.5. Свойства водных растворов пав. Мицеллообразование
- •6.6. Влияние различных факторов на ккм
- •6.6.1. Влияние длины углеводородного радикала
- •6.6.2. Влияние строения углеводородного радикала
- •6.6.3. Влияние добавок электролитов
- •6.6.4. Влияние полярных органических веществ
- •6.7. Термодинамика мицеллообразования в водной среде
- •6.8. Зависимость растворимости пав в воде от температуры
- •6.9. Мицеллообразование в неводных средах
- •6.10. Оценка дифильных свойств пав
- •6.11. Солюбилизация
- •6.12. Физико-химия моющего действия
- •6.13. Смеси ионных и неионных пав
- •6.14. Контрольные вопросы
- •VII. Получение дисперсных систем
- •7.1. Введение
- •7.2. Конденсационные способы образования дисперсных систем
- •Реакция обмена
- •Реакции восстановления
- •Реакция окисления
- •Гидролиз солей
- •Конденсация паров
- •Замена растворителя
- •7.3. Строение мицелл различных золей
- •Типы потенциалопределяющих ионов
- •Принципы построения формулы мицелл
- •7.4. Диспергационные методы получения дисперсных систем
- •7.4.1. Механическое диспергирование
- •7.4.2. Эффект Ребиндера и его роль в диспергировании
- •7.4.3. Физико-химическое дробление осадков (пептизация)
- •7.5. Образование лиофильных коллоидных систем
- •VIII. Молекулярно-кинетические свойства коллоидных систем
- •8.1. Введение
- •8.2. Броуновское движение
- •8.2.1. Природа броуновского движения
- •8.2.2. Общенаучное значение броуновского движения
- •8.2.3. Средний сдвиг частицы
- •8.3. Диффузия
- •8.3.1. Выражения для идеальной диффузии. Первый и второй законы Фика
- •8.3.2. Градиент концентрации при диффузии
- •8.3.3. Диффузия и проницаемость
- •8.4. Седиментация и методы седиментационного анализа
- •8.4.1. Гипсометрический закон
- •8.4.2. Седиментационное уравнение незаряженной частицы
- •8.4.3. Ультрацентрифуга
- •8.4.4. Скоростное ультрацентрифугирование
- •8.4.5. Равновесное ультрацентрифугирование
- •8.5. Контрольные вопросы
- •IX. Оптические свойства коллоидных систем.
- •9.1. Явления, наблюдаемые при взаимодействии видимого света с веществом.
- •9.2. Рэлеевское рассеяние света.
- •9.3. Рассеяние малыми частицами.
- •9.4. Рассеяние большими частицами.
- •9.5. Анализ уравнения Рэлея.
- •9.6. Поглощение света дисперсными системами.
- •9.7. Турбидиметрический метод определения коллоидных частиц.
- •9.7.1. Дисперсные системы, подчиняющиеся уравнению Рэлея.
- •9.7.2. Дисперсные системы, не подчиняющиеся уравнению Рэлея.
- •9.8. Световая микроскопия.
- •9.8.1. Световая микроскопия.
- •9.8.2. Темнопольная микроскопия.
- •9.8.3. Электронная микроскопия Предел разрешения электронного микроскопа.
- •Взаимодействие электронов с объектом.
- •Характеристики изображения.
- •Типы электронных микроскопов.
- •Основные части электронного микроскопа и их назначение.
- •Образцы для просвечивающей электронной микроскопии.
- •Методы препарирования образцов.
- •X. Электроповерхностные свойства дисперсных систем
- •10.1. Значение электрокинетических явлений в природе и технике
- •10.3. Связь поверхностного натяжения с электрическим потенциалом. Уравнение Липпмана.
- •Строение двойного электрического слоя.
- •10.5. Изменение потенциала в дэс с изменением расстояния от поверхности.
- •10.6. Внутренняя часть дэс
- •10.7. Электрокинетические явления.
- •10.8. Уравнение Гельмгольца-Смолуховского для определения -потенциала.
- •10.9. Влияние электролитов на двойной электрический слой.
- •10.10. Влияние концентрации электролита.
- •10.11.Влияние валентности противоиона на дэс.
- •10.12. Влияние радиуса иона на дэс.
- •Перезарядка золей индифферентными электролитами
- •Действие неиндифферентных электролитов на двойной электрический слой
- •Влияние температуры и разбавления на дэс
- •XI. Устойчивость и коагуляция коллойдных систем
- •11.1. Понятие об устойчивости
- •11.2. Расклинивающее давление
- •11.3. Теория агрегативной устойчивости и коагуляции лиофобных дисперсных систем (теория длфо)
- •11.4. Кинетический подход к устойчивости дисперсных систем
- •11.5. Природа сил, действующих между частицами.
- •Силы отталкивания
- •11.6.Коагуляция.
- •11.7. Механизм коагуляции электролитами по теории длфо.
- •11.8. Коагулирующее действие электролитов.
- •11.9. Правила коагуляции электролитами.
- •XII. Структурно–механические свойства дисперсных систем
- •12.1. Основные понятия. Реология как метод исследования структуры дисперсных систем
- •12.2. Идеальные законы реологии
- •12.3. Моделирование реологических свойств тел
- •12.8. Реологические свойства твердообразных тел
- •XIII. Растворы высокомолекулярных соединений. Основные положения статистики полимерных цепей
- •13.1. Гибкость и размеры цепи
- •13.2. Количественные характеристики размеров макромолекул
- •13.3. Свойства Гауссова клубка
- •13.4. Состояния полимеров в растворе
- •13.5. Термодинамика растворения полимеров
- •13.6. Набухание как первая стадия растворения
- •13.7. Разбавленные растворы полимеров
- •13.8. Осмотическое давление растворов
- •13.9. Термодинамическое сродство растворителя к полимеру
- •13.10. Взаимодействия в растворах полимеров
- •13.11. Концентрированные растворы полимеров
- •13.12. Термодинамическая равновесность растворов полимеров и подчинение их правилу фаз
7.4.3. Физико-химическое дробление осадков (пептизация)
Пептизацией называют расщепление на первичные частицы под действием внешней среды агрегатов, возникающих в результате обратимой коагуляции дисперсных систем. Существуют три способа перевода осадка в коллоидный раствор.
Адсорбционная пептизация. В этом случае отталкивание частиц осадка друг от друга вызывается ДЭС, образующимся на поверхности частиц при адсорбции ионов добавляемого электролита-стабилизатора.
Пептизация путем поверхностной диссоциации. Связана с образованием ДЭС методом поверхностной модификации. Пептизатор здесь способствует процессу диссоциации с поверхности, вызывая образование растворимых соединений на поверхности частиц.
Пептизация путем промывания осадка. Применяется в том случае, когда на поверхности частиц в осадке есть двойные электрические слои, но они сжаты вследствие большой концентрации электролита. При промывании такого осадка водой концентрация электролита в нем уменьшается, двойные слои увеличивают свою толщину; силы электростатического отталкивания между частицами будут действовать на более далеких расстояниях и вызовут коллоидное растворение осадка.
Пептизация протекает с определенной скоростью, которая, как правило, возрастает с повышением температуры.
При пептизации наблюдается характерная зависимость между количествами пептизированного вещества, взятого осадка и пептизатора. Эту закономерность называют правилом осадка Оствальда. Она заключается в том, что при постоянном содержании пептизатора с возрастанием количества взятого для пептизации осадка количество осадка, перешедшего в раствор, сначала увеличивается, а затем уменьшается (рис. 7.6) .
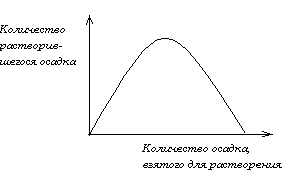
Рис. 7.6. Зависимость количества растворившегося осадка от количества осадка, взятого для растворения.
Такую зависимость можно объяснить тем, что для коллоидного диспергирования необходимо определенное количество пептизатора. При малых количествах осадка его достаточно для образования адсорбционного слоя на каждой частице. С увеличением количества осадка, взятого для пептизации – пептизатор распределяется по большому количеству частиц. На каждой частице его становится все меньше и, наконец, его не достаточно для образования устойчивой системы, поэтому количество пептизированного осадка уменьшается, и пептизация может совсем не происходить.
Отсюда следует, что пептизация резко отличается от обычного растворения, в котором после достижения насыщения содержание растворенного вещества перестает зависеть от количества вещества, взятого для растворения.
Пептизация имеет большое значение в технике при изготовлении суспензии глин, цементов, в препаративной коллоидной химии при получении золей. Однако в ряде производств пептизация может играть и отрицательную роль, так, например, при извлечении сахара возможна нежелательная пептизация пектина и других веществ, содержащихся в растительных тканях.
7.5. Образование лиофильных коллоидных систем
Многие коллоидные системы могут возникать спонтанно, или самопроизвольно. Эти системы называются лиофильными коллоидными системами, так как взаимодействие между веществом дисперсной фазы и средой достаточно большое.
Образование термодинамически устойчивых дисперсных систем, как и истинных растворов, происходит самопроизвольно, сопровождаясь уменьшением свободной энергии.
Изменение свободной энергии при самопроизвольном диспергировании может быть выражено следующим образом:
![]() (7.15)
(7.15)
При добавлении объем
системы не меняется и
![]() .
Поверхность при диспергировании
увеличивается, т.е.
.
Поверхность при диспергировании
увеличивается, т.е.
![]() .
Энтропия системы при дроблении также
возрастает:
.
Энтропия системы при дроблении также
возрастает:
![]() .
.
Для самопроизвольного
протекания процесса должно выполняться
условие
![]() .
Это условие будет выполнимо, если
возрастание свободной энергии из-за
увеличения поверхности при диспергировании
будет меньше убыли свободной энергии
из-за возрастания энтропии:
.
Это условие будет выполнимо, если
возрастание свободной энергии из-за
увеличения поверхности при диспергировании
будет меньше убыли свободной энергии
из-за возрастания энтропии:
![]() (7.16)
(7.16)
Изменение поверхности
пропорционально числу частиц n,
умноженному на размер частиц в квадрате
![]() .
Изменение энтропии
.
Изменение энтропии
![]() ,
т.е. кинетической энергии частиц, где
,
т.е. кинетической энергии частиц, где
![]() - безмерный коэффициент, равный ~ 30.
- безмерный коэффициент, равный ~ 30.
![]() (7.17)
(7.17)
Из этого уравнения можно получить критическое значения поверхностного натяжения:
![]() (7.18)
(7.18)
для частиц
![]() ,
,
![]() .
.
Самопроизвольное
диспергирование возможно для коллоидных
систем, в которых
![]() .
.
Несмотря на большую
межфазную поверхность в лиофильных
дисперсных системах, малое межфазное
натяжение обуславливает сравнительно
небольшую поверхностную энергию, которая
способна компенсироваться энтропийной
составляющей. Малое значение
![]() возможно только при значительном
межфазном взаимодействии, характерном
для жидких сред. Поэтому термодинамически
устойчивыми свободно-дисперсионными
системами могут быть только системы
с жидкой дисперсной средой.
возможно только при значительном
межфазном взаимодействии, характерном
для жидких сред. Поэтому термодинамически
устойчивыми свободно-дисперсионными
системами могут быть только системы
с жидкой дисперсной средой.
При самопроизвольном диспергировании образуются дисперсные системы, характеризующиеся кривыми распределения с некоторым наиболее вероятным радиусом, т. е. существует оптимальная дисперсность. Дальнейшее диспергирование, вплоть до молекул, невозможно, так как состояние с оптимальной дисперсностью более выгодно, чем состояние двух сопряженных сплошных фаз или состояние истинного раствора. По мнению Ребиндера, термодинамическая устойчивость двухфазных дисперсных систем определяется двумя условиями: достаточно низким межфазным поверхностным натяжением и быстрым его ростом с уменьшением радиуса частиц.
Наиболее типичными представителями лиофильных коллоидных систем являются растворы коллоидных ПАВ и высокомолекулярных соединений, а также водные дисперсии эмульсолов (углеводородов с большим содержанием (10-20%) мыл или мылоподобных поверхностно-активных веществ). Эмульсолы применяют в качестве смазочно-охлаждающих жидкостей (СОЖ) при холодной обработке металлов.
