
- •Коллоидная химия
- •1.Коллоидные системы и предмет коллоидной химии
- •1.1. Коллоидные системы
- •1.2. Предмет коллоидной химии
- •Первый вариант количественной оценки - основной
- •Например, у частицы кубической формы с размером ребра
- •1.3. Классификация дисперсных систем
- •Классификация коллоидных систем по агрегатному состоянию фаз
- •2. Физическая химия поверхностных явлений
- •2.1. Межмолекулярные связи
- •Отличия молекулярных сил притяжения от химических:
- •Вклад различных видов энергии в общую энергию притяжения молекул
- •2.2.1. Определения поверхностного натяжения
- •1. Поверхностное натяжение численно равно работе обратимого изотермического образования единицы поверхности
- •2.2.3. Факторы, влияющие на величину поверхностного натяжения
- •1. Температура т
- •Поверхностное натяжение веществ на границе с воздухом
- •3) Природа контактирующих фаз
- •2.2.4. Экспериментальные методы определения поверхностного натяжения
- •2.3. Внутренняя (полная) удельная поверхностная энергия
- •Термодинамические характеристики поверхности некоторых жидкостей на границе их с воздухом
- •2.4. Адсорбция
- •2.4.1. Основные понятия и определения
- •2.4.2.1.Уравнение Ленгмюра(*)
- •Основные положения теории Ленгмюра:
- •Экспериментальное определение констант уравнения Ленгмюра
- •Правило Дюкло — Траубе:
- •Экспериментальное определение геометрических размеров молекулы пав
- •2.4.2.3. Изотермы адсорбции на неоднородной поверхности
- •А) теория Поляни(*)
- •Основные положения теории Поляни:
- •Основные положения теории бэт
- •Основные характеристики адсорбентов
- •Классификация адсорбентов:
- •2. По полярности
- •3. По размеру пор
- •2.4.5.2. Влияние кривизны поверхности на равновесие фаз
- •2.4.5.3. Капиллярные явления
- •2.4.5.4.Теория капиллярной конденсации
- •Условия действия капиллярных сил
- •2.4.5.5. Классификация изотерм адсорбции
- •2.4.6. Адсорбция из растворов на твердых адсорбентах
- •2.4.6.1. Молекулярная адсорбция
- •2.4.6.1.2. Основные закономерности адсорбции из растворов неэлектролитов на поверхности твердых адсорбентов)
- •2. Природа растворителя
- •3. Влияние природы адсорбента
- •4. Влияние природы адсорбтива
- •2.4.6.1.2. Основные закономерности адсорбции из растворов электролитов на поверхности твердых адсорбентов.
- •2.4.6.1.3. Ионно-обменная адсорбция
- •2.5. Смачивание. Адгезия. Когзия
- •2.5.1. Адгезия. Когзия
- •Механизм процесса адгезии
- •Несколько механизмов и теорий адгезии
- •2.5.2. Краевой угол смачивания и работа адгезии
- •2.5.3. Избирательное смачивание
- •2.5.4. Инверсия смачиваемости поверхности
- •2.5.5. Количественные характеристики процесса смачивания поверхности.
- •Qсм и b порошкообразных веществ
- •2.5.6. Измерение краевого угла смачивания
- •Использование пав для изменения смачиваемости поверхности
- •Избирательное смачивание
- •3. Молекулярно-кинетические свойства дисперсных систем
- •3.2. Диффузия в коллоидных системах
- •3.3. Седиментация суспензий
- •3.3. Седиментационно-диффузионное равновесие. Седиментационная устойчивость
- •Седиментационная устойчивость
- •4. Модель реального тела. Модель Бингама(*) – вязкопластическое тело
- •Лекция 9. .4.3. Реологические свойства реальных тел
- •Классификация тел по их реологическим свойствам
- •Вязкость агрегативно устойчивых дисперсных систем
- •4.3.2.Реологические свойства структурированных жидкообразных систем
- •Электрические свойства коллоидных растворов (золей)
- •5.1. Электрокинетические явления
- •5.2. Механизм образования дэс
- •4. Поляризация поверхности за счёт внешнего электрического поля.
- •5.3. Строение дэс
- •5.4. Факторы, влияющие на величину ζ-потенциала:
- •5.5.3. Влияние температуры на электрокинетический потенциал
- •5.5.4. Влияние рН среды
- •5.5.5. Экспериментальное определение - потенциала
- •6.Коагуляция и устойчивость дисперсных систем
- •6.1. Устойчивость дисперсных систем
- •6.2. Факторы агрегативной устойчивости
- •6.3. Ионный фактор стабилизации дисперсных систем Теория устойчивости лиофобных золей длфо
- •6.4. Коагуляция лиофобных дисперсных систем
- •6.4.1. Основные закономерности электролитной коагуляции
- •6.4.2. Кинетика электролитной коагуляции
- •6.4.3. Частные случаи электролитной коагуляции
- •6.4.4. Коллоидная защита
- •7. Лиофильные дисперсные системы. Коллоидные поверхностно-активные вещества
- •Классификация и общая характеристика пав
- •Коллоидные пав
- •2. Гидрофильно-липофильный баланс
- •Групповые числа атомных группировок
- •Применение пав
- •3. Строение мицелл пав. Солюбилизация
- •Факторы, влияющие на ккм
- •1) В растворах ипав ↑ Сэл-та ↓ ккм.
- •2) Добавление органических веществ в водные растворы пав по-разному влияет на ккм:
- •3). Влияние температуры т.
- •Значение мицеллярных растворов
- •Лиофобные дисперсные системы. Эмульсии
- •Классификация
- •Устойчивость и стабилизация эмульсий
- •Эмульгаторы
- •Механизм стабилизации:
3). Влияние температуры т.
Наблюдается различный характер влияния Т на ИПАВ и НИПАВ.
Увеличение Т на растворы ИПАВ усиливает тепловое движение и препятствует агрегации молекул, но интенсивное движение уменьшает гидратацию полярных групп и способствует их объединению.
Многие ПАВ с большим R из-за плохой растворимости не образуют мицеллярных растворов. Однако при изменении Т растворимость ПАВ может возрасти и обнаруживается МЦО.
Т, при кот. увеличивается растворимость ИПАВ из-за образования МЦ, называется точкой Крафта (обычно 283-293 К).
Т. Крафта не совпадает с ТПЛ тв. ПАВ, а лежит ниже, т.к. в набухшем геле ПАВ гидратировано и это облегчает плавление.
С,моль/л ПАВ+раствор
р аст-моть МЦ+р-р
аст-моть МЦ+р-р
К КМ
КМ
р-р

Т
Рис. 7.2. Фазовая диаграмма раствора коллоидного ПАВ вблизи точки Крафта
Для получения ПАВ с низким значение точки Крафта:
а) вводят дополнительный СН3 – или боковые заместители;
б) вводят непредельную связь «=»;
в) полярный сегмент (оксиэтиленовый) между ионной группой и цепью.
Выше точки К рафта МЦ ИПАВ распадаются на более мелкие ассоциаты – происходит демицеллизация.
(Мицеллообразование происходит в определенном для каждого ПАВ интервале температур, важнейшими характеристиками которого являются точка Крафта и точка помутнения.
Точка Крафта- нижний температурный предел мицеллообразования ионогенных ПАВ, обычно она равна 283 – 293К; при температурах ниже точки Крафта растворимость ПАВ недостаточна для образования мицелл.
Точка помутнения- верхний температурный предел мицеллообразования неионогенных ПАВ, обычные ее значения 323 – 333 К; при более высоких температурах система ПАВ - растворитель теряет устойчивость и расслаивается на две макрофазы.)
2) ↑ Т в растворах НИПАВ ↓ ККМ за счет дегидратации оксиэтиленовых цепочек.
В растворах НИПАВ наблюдается температура помутнения – верхний температурный предел МЦО НИПАВ (323-333 К), при более высоких Т система теряет устойчивость и расслаивается на две фазы.
Термодинамика и механизм мицеллообразования (МЦО)
(Истинная растворимость ПАВ обусловлена увеличением энтропии Sпри растворении и в меньшей мере взаимодействием с молекулами воды.
Для ИПАВ характерна диссоциация в воде, Sрастворения их значительна.
НИПАВ слабо взаимодействуют с Н2О, их растворимость меньше при том же R. Чаще ∆Н>0, поэтому растворимость ↑ при ↑Т.
Малая растворимость ПАВ проявляется в «+» поверхностной активности, а с ↑С - в значительной ассоциации молекул ПАВ, переходящей в МЦО. )
Рассмотрим механизм растворения ПАВ. Он состоит из 2 стадий: фазового перехода и взаимодействия с молекулами растворителя – сольватацией (водой и гидратацией):
∆Нф.п. >0 ∆Sф.п. >0 ∆Нраств. ><0
∆Нсольват. <0 ∆S сольват.<0 ∆Sраств. ><0
∆G= ∆Нраств. - Т∆Sраств. <0
Для ИПАВ:
∆Нсольват. большое по величине, ∆Нраств. <0, ∆Sраств. >0 и ∆G раств. <0
Для НИПАВ ∆Нраств. ≥0, поэтому при ↑Т растворимость ↑ за счет энтропийной составляющей.
Для процесса МЦО характерно ∆НМЦО. <0, ∆S МЦО<0 из-за экранирования полярными группами углеводородных радикалов:
∆GМЦО= ∆НМЦО. - Т∆SМЦО . <0 за счет энергетической составляющей
Методы определения ККМ
Основаны на регистрации резкого изменения физико-химических свойств растворов ПАВ в зависимости от их концентрации (мутности τ, поверхностного натяжения σ, эквивалентной электропроводности λ, осмотического давления π, показателя преломления n).
Обычно на этих кривых есть излом, т.к. одна ветвь кривой отвечает молекулярному состоянию растворов – вторая часть – коллоидному.
Значения ККМ для данной системы ПАВ - растворитель могут различаться при определении их тем или иным экспериментальным методом или при использовании того или иного способа математической обработки опытных данных.
Все экспериментальные методы определения ККМ (их известно более 70) разделяют на две группы. К одной группе относят методы, не требующие введения в систему ПАВ - растворитель дополнительных веществ. Это построение изотерм поверхностного натяжения = f(C) или = f(lnC); измерение электропроводности ( и ) раствора ПАВ; изучение оптических свойств - показателя преломления растворов, светорассеяния; изучение спектров поглощения и спектров ЯМР и др. Хорошо определяется ККМ при построении зависимости растворимости ПАВ от величины 1/T (обратной температуры). Просты и надежны методы потенциометрического титрования и поглощения ультразвука и др.
Вторая группа методов измерения ККМ основана на добавлении в растворы дополнительных веществ и их солюбилизации (коллоидном растворении) в мицеллах ПАВ, которую можно регистрировать с использованием спектральных методов, флуоресценции, ЭПР и др. Ниже приводится краткое описание некоторых методов определения ККМ из первой группы.
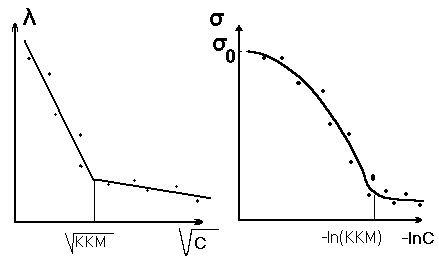
Рис. 7.2. Определение ККМ кондуктометрическим методом (слева).
Рис.7.3.Определение ККМ методом измерения поверхностного натяжения
Кондуктометрический
метод определения ККМ применяется для
ионогенных ПАВ. Если бы в водных растворах
ионогенных ПАВ, например, олеата натрия
или калия отсутствовало мицеллообразование,
то в согласии с уравнением Кольрауша(),
экспериментальные точки зависимости
эквивалентной электропроводности от
концентрации C в координатах
= f(![]() )
ложились бы вдоль прямой (рис. 7.2). Это
выполняется при малых концентрациях
ПАВ (10-3
моль/л), начиная с ККМ, формируются ионные
мицеллы, окруженные диффузным слоем
противоионов, ход зависимости
= f(
)
ложились бы вдоль прямой (рис. 7.2). Это
выполняется при малых концентрациях
ПАВ (10-3
моль/л), начиная с ККМ, формируются ионные
мицеллы, окруженные диффузным слоем
противоионов, ход зависимости
= f(![]() )
нарушается и на линии наблюдается излом.
)
нарушается и на линии наблюдается излом.
Другой метод определения ККМ основан на измерении поверхностного натяжения водных растворов ПАВ, которое уменьшается с ростом концентрации вплоть до ККМ, а затем остается практически постоянным. Этот метод применим как для ионогенных, так и для неионогенных ПАВ. Для определения ККМ опытные данные по зависимости от C обычно представляют в координатах = f(lnC) (рис. 7.3).
Изотермы σ=f(C) отличаются от изотерм истинных растворов ПАВ более резким ↓σ с ↑С и наличием излома в области малых концентраций (около 10-3 – 10-6 моль/л), выше которых σ остается постоянной. Более резко эта точка ККМ выявляется на изотерме σ=f ln(C) в соответствии с
-dσ= Σ Γidμi, для данного компонента μi = μiо + RT ln ai dμi = μiо + RT dln ai
![]() =
- Γi
=
- Γi
![]() = - Γi
RT
= - Γi
RT
График зависимости показателя преломления n от концентрации раствора ПАВ представляет собой ломаную линию из двух отрезков, пересекающихся в точке ККМ (рис. 7.4). По этой зависимости можно определить ККМ ПАВ в водных и неводных средах.
В области ККМ истинный (молекулярный) раствор переходит в коллоидный раствор, при этом резко возрастает светорассеяние системы (каждый мог наблюдать рассеяние света на пылинках, взвешенных в воздухе). Для определения ККМ методом светорассеяния измеряют оптическую плотность системы D в зависимости от концентрации ПАВ (рис.7.5), ККМ находят из графика D = f(C).

Рис. 7.4. Определение ККМ методом измерения показателя преломления n.
Рис. 7.5. Определение ККМ методом светорассеяния (справа).
