
- •Коллоидная химия
- •1.Коллоидные системы и предмет коллоидной химии
- •1.1. Коллоидные системы
- •1.2. Предмет коллоидной химии
- •Первый вариант количественной оценки - основной
- •Например, у частицы кубической формы с размером ребра
- •1.3. Классификация дисперсных систем
- •Классификация коллоидных систем по агрегатному состоянию фаз
- •2. Физическая химия поверхностных явлений
- •2.1. Межмолекулярные связи
- •Отличия молекулярных сил притяжения от химических:
- •Вклад различных видов энергии в общую энергию притяжения молекул
- •2.2.1. Определения поверхностного натяжения
- •1. Поверхностное натяжение численно равно работе обратимого изотермического образования единицы поверхности
- •2.2.3. Факторы, влияющие на величину поверхностного натяжения
- •1. Температура т
- •Поверхностное натяжение веществ на границе с воздухом
- •3) Природа контактирующих фаз
- •2.2.4. Экспериментальные методы определения поверхностного натяжения
- •2.3. Внутренняя (полная) удельная поверхностная энергия
- •Термодинамические характеристики поверхности некоторых жидкостей на границе их с воздухом
- •2.4. Адсорбция
- •2.4.1. Основные понятия и определения
- •2.4.2.1.Уравнение Ленгмюра(*)
- •Основные положения теории Ленгмюра:
- •Экспериментальное определение констант уравнения Ленгмюра
- •Правило Дюкло — Траубе:
- •Экспериментальное определение геометрических размеров молекулы пав
- •2.4.2.3. Изотермы адсорбции на неоднородной поверхности
- •А) теория Поляни(*)
- •Основные положения теории Поляни:
- •Основные положения теории бэт
- •Основные характеристики адсорбентов
- •Классификация адсорбентов:
- •2. По полярности
- •3. По размеру пор
- •2.4.5.2. Влияние кривизны поверхности на равновесие фаз
- •2.4.5.3. Капиллярные явления
- •2.4.5.4.Теория капиллярной конденсации
- •Условия действия капиллярных сил
- •2.4.5.5. Классификация изотерм адсорбции
- •2.4.6. Адсорбция из растворов на твердых адсорбентах
- •2.4.6.1. Молекулярная адсорбция
- •2.4.6.1.2. Основные закономерности адсорбции из растворов неэлектролитов на поверхности твердых адсорбентов)
- •2. Природа растворителя
- •3. Влияние природы адсорбента
- •4. Влияние природы адсорбтива
- •2.4.6.1.2. Основные закономерности адсорбции из растворов электролитов на поверхности твердых адсорбентов.
- •2.4.6.1.3. Ионно-обменная адсорбция
- •2.5. Смачивание. Адгезия. Когзия
- •2.5.1. Адгезия. Когзия
- •Механизм процесса адгезии
- •Несколько механизмов и теорий адгезии
- •2.5.2. Краевой угол смачивания и работа адгезии
- •2.5.3. Избирательное смачивание
- •2.5.4. Инверсия смачиваемости поверхности
- •2.5.5. Количественные характеристики процесса смачивания поверхности.
- •Qсм и b порошкообразных веществ
- •2.5.6. Измерение краевого угла смачивания
- •Использование пав для изменения смачиваемости поверхности
- •Избирательное смачивание
- •3. Молекулярно-кинетические свойства дисперсных систем
- •3.2. Диффузия в коллоидных системах
- •3.3. Седиментация суспензий
- •3.3. Седиментационно-диффузионное равновесие. Седиментационная устойчивость
- •Седиментационная устойчивость
- •4. Модель реального тела. Модель Бингама(*) – вязкопластическое тело
- •Лекция 9. .4.3. Реологические свойства реальных тел
- •Классификация тел по их реологическим свойствам
- •Вязкость агрегативно устойчивых дисперсных систем
- •4.3.2.Реологические свойства структурированных жидкообразных систем
- •Электрические свойства коллоидных растворов (золей)
- •5.1. Электрокинетические явления
- •5.2. Механизм образования дэс
- •4. Поляризация поверхности за счёт внешнего электрического поля.
- •5.3. Строение дэс
- •5.4. Факторы, влияющие на величину ζ-потенциала:
- •5.5.3. Влияние температуры на электрокинетический потенциал
- •5.5.4. Влияние рН среды
- •5.5.5. Экспериментальное определение - потенциала
- •6.Коагуляция и устойчивость дисперсных систем
- •6.1. Устойчивость дисперсных систем
- •6.2. Факторы агрегативной устойчивости
- •6.3. Ионный фактор стабилизации дисперсных систем Теория устойчивости лиофобных золей длфо
- •6.4. Коагуляция лиофобных дисперсных систем
- •6.4.1. Основные закономерности электролитной коагуляции
- •6.4.2. Кинетика электролитной коагуляции
- •6.4.3. Частные случаи электролитной коагуляции
- •6.4.4. Коллоидная защита
- •7. Лиофильные дисперсные системы. Коллоидные поверхностно-активные вещества
- •Классификация и общая характеристика пав
- •Коллоидные пав
- •2. Гидрофильно-липофильный баланс
- •Групповые числа атомных группировок
- •Применение пав
- •3. Строение мицелл пав. Солюбилизация
- •Факторы, влияющие на ккм
- •1) В растворах ипав ↑ Сэл-та ↓ ккм.
- •2) Добавление органических веществ в водные растворы пав по-разному влияет на ккм:
- •3). Влияние температуры т.
- •Значение мицеллярных растворов
- •Лиофобные дисперсные системы. Эмульсии
- •Классификация
- •Устойчивость и стабилизация эмульсий
- •Эмульгаторы
- •Механизм стабилизации:
Лекция 6
2.5. Смачивание. Адгезия. Когзия
Понятия смачивания, адгезии, когезии, растекания относятся к межфазным взаимодействиям, которые наблюдаются между конденсированными фазами.
2.5.1. Адгезия. Когзия
Адгезия —межфазное взаимодействие конденсированных тел разной природы (прилипание).
Адгезия может возникнуть между ж1/ж2, ж/т, т1/т2(в этом случае одна из фаз была ранее в жидком состоянии). Адгезия — результат стремления системы к уменьшению поверхностной энергии, поэтому адгезия — самопроизвольный процесс при соответствующих условиях.
Адгезия характеризуется работой адгезии — Wa.
Работа адгезиихарактеризует прочность связи и численно равна работе обратимого изотермического разрыва адгезионного соединения единичной площади.
Полная работа адгезии Ws= WaS (2.115)
Получим соотношение между работой адгезии и поверхностным натяжением взаимодействующих компонентов.
Представим себе 2 контактирующие фазы в конденсированном состоянии, имеющие на границе раздела с воздухом единичную площадь S=1 (2 ж1/ж2или ж/т) — процесс, обратный рассмотрению образования поверхностного натяжения:


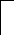








 σж/г
σт/г
σж/г
σт/г

 +
2
+
2



 3
σт/ж
3
σт/ж
Рис.2.39. Образование адгезионного соединения
∆G=Gкон-Gнач= σт/ж - σж/г - σт/г (2.116)
Согласно термодинамике полезная работа (в нашем случае Wa) совершается за счет убыли энергии, поэтомуWa= -∆G, поэтому
Wa= σт/г+ σж/г - σт/ж —уравнение Дюпре(*) (2.117)
Из уравнения Дюпре следует, что чем больше работа адгезии, тем меньше тж. Действительно, чем сильнее межмолекулярные взаимодействия жидкости и твердого тела, тем меньше нескомпенсированность сил в их поверхностном слое и тем меньше межфазное натяжение тж.
От работы адгезии надо отличать понятие адгезионной прочности Wп— работы разрушения соединения :Wп=Wa+Wдеф
Wдеф— может быть очень велика и отличаться отWa вnраз.
Когезия — внутрифазное взаимодействие, обусловленное силами межмолекулярного притяжения различной природы, характеризуется работой когезииWк.
Работа когезии Wкопределяется величиной обратимой изотермической работы разрыва тела по сечению единичной площади.
При обсуждении понятия поверхностного натяжения мы говорили, что эта величина характеризует межмолекулярное взаимодействие внутри фазы и равна работе образования площади, равной единице.
При разрыве тела образуется 2 единичных площади, поэтому
Wк=2 σж/г (2.118)
Когезия отражает межмолекулярное взаимодействие и характеризуется такими параметрами, как Е парообразования, Ткип, Е крист.решетки и т.д.
Механизм процесса адгезии
Процесс адгезии делят на 2 стадии:
1) диффузионная(транспортная) молекул адгезива к поверхности субстрата и их ориентация в пространстве.
Увеличить скорость можно за счет ↑Е, Т, Р, перевода адгезива в жидкое состояние растворением или плавлением.
2) непосредственное взаимодействие адгезива и субстрата за счет различных сил взаимодействия — В-д-В., хим., электростат. и т.д. Ковалентные связи действуют на расстоянии, меньшем 0,5 нм, ионные и В-д-в наr=1 - 100 нм. Контакт возможен, поэтому только при взаимодействии жидких фаз.
