
- •Коллоидная химия
- •1.Коллоидные системы и предмет коллоидной химии
- •1.1. Коллоидные системы
- •1.2. Предмет коллоидной химии
- •Первый вариант количественной оценки - основной
- •Например, у частицы кубической формы с размером ребра
- •1.3. Классификация дисперсных систем
- •Классификация коллоидных систем по агрегатному состоянию фаз
- •2. Физическая химия поверхностных явлений
- •2.1. Межмолекулярные связи
- •Отличия молекулярных сил притяжения от химических:
- •Вклад различных видов энергии в общую энергию притяжения молекул
- •2.2.1. Определения поверхностного натяжения
- •1. Поверхностное натяжение численно равно работе обратимого изотермического образования единицы поверхности
- •2.2.3. Факторы, влияющие на величину поверхностного натяжения
- •1. Температура т
- •Поверхностное натяжение веществ на границе с воздухом
- •3) Природа контактирующих фаз
- •2.2.4. Экспериментальные методы определения поверхностного натяжения
- •2.3. Внутренняя (полная) удельная поверхностная энергия
- •Термодинамические характеристики поверхности некоторых жидкостей на границе их с воздухом
- •2.4. Адсорбция
- •2.4.1. Основные понятия и определения
- •2.4.2.1.Уравнение Ленгмюра(*)
- •Основные положения теории Ленгмюра:
- •Экспериментальное определение констант уравнения Ленгмюра
- •Правило Дюкло — Траубе:
- •Экспериментальное определение геометрических размеров молекулы пав
- •2.4.2.3. Изотермы адсорбции на неоднородной поверхности
- •А) теория Поляни(*)
- •Основные положения теории Поляни:
- •Основные положения теории бэт
- •Основные характеристики адсорбентов
- •Классификация адсорбентов:
- •2. По полярности
- •3. По размеру пор
- •2.4.5.2. Влияние кривизны поверхности на равновесие фаз
- •2.4.5.3. Капиллярные явления
- •2.4.5.4.Теория капиллярной конденсации
- •Условия действия капиллярных сил
- •2.4.5.5. Классификация изотерм адсорбции
- •2.4.6. Адсорбция из растворов на твердых адсорбентах
- •2.4.6.1. Молекулярная адсорбция
- •2.4.6.1.2. Основные закономерности адсорбции из растворов неэлектролитов на поверхности твердых адсорбентов)
- •2. Природа растворителя
- •3. Влияние природы адсорбента
- •4. Влияние природы адсорбтива
- •2.4.6.1.2. Основные закономерности адсорбции из растворов электролитов на поверхности твердых адсорбентов.
- •2.4.6.1.3. Ионно-обменная адсорбция
- •2.5. Смачивание. Адгезия. Когзия
- •2.5.1. Адгезия. Когзия
- •Механизм процесса адгезии
- •Несколько механизмов и теорий адгезии
- •2.5.2. Краевой угол смачивания и работа адгезии
- •2.5.3. Избирательное смачивание
- •2.5.4. Инверсия смачиваемости поверхности
- •2.5.5. Количественные характеристики процесса смачивания поверхности.
- •Qсм и b порошкообразных веществ
- •2.5.6. Измерение краевого угла смачивания
- •Использование пав для изменения смачиваемости поверхности
- •Избирательное смачивание
- •3. Молекулярно-кинетические свойства дисперсных систем
- •3.2. Диффузия в коллоидных системах
- •3.3. Седиментация суспензий
- •3.3. Седиментационно-диффузионное равновесие. Седиментационная устойчивость
- •Седиментационная устойчивость
- •4. Модель реального тела. Модель Бингама(*) – вязкопластическое тело
- •Лекция 9. .4.3. Реологические свойства реальных тел
- •Классификация тел по их реологическим свойствам
- •Вязкость агрегативно устойчивых дисперсных систем
- •4.3.2.Реологические свойства структурированных жидкообразных систем
- •Электрические свойства коллоидных растворов (золей)
- •5.1. Электрокинетические явления
- •5.2. Механизм образования дэс
- •4. Поляризация поверхности за счёт внешнего электрического поля.
- •5.3. Строение дэс
- •5.4. Факторы, влияющие на величину ζ-потенциала:
- •5.5.3. Влияние температуры на электрокинетический потенциал
- •5.5.4. Влияние рН среды
- •5.5.5. Экспериментальное определение - потенциала
- •6.Коагуляция и устойчивость дисперсных систем
- •6.1. Устойчивость дисперсных систем
- •6.2. Факторы агрегативной устойчивости
- •6.3. Ионный фактор стабилизации дисперсных систем Теория устойчивости лиофобных золей длфо
- •6.4. Коагуляция лиофобных дисперсных систем
- •6.4.1. Основные закономерности электролитной коагуляции
- •6.4.2. Кинетика электролитной коагуляции
- •6.4.3. Частные случаи электролитной коагуляции
- •6.4.4. Коллоидная защита
- •7. Лиофильные дисперсные системы. Коллоидные поверхностно-активные вещества
- •Классификация и общая характеристика пав
- •Коллоидные пав
- •2. Гидрофильно-липофильный баланс
- •Групповые числа атомных группировок
- •Применение пав
- •3. Строение мицелл пав. Солюбилизация
- •Факторы, влияющие на ккм
- •1) В растворах ипав ↑ Сэл-та ↓ ккм.
- •2) Добавление органических веществ в водные растворы пав по-разному влияет на ккм:
- •3). Влияние температуры т.
- •Значение мицеллярных растворов
- •Лиофобные дисперсные системы. Эмульсии
- •Классификация
- •Устойчивость и стабилизация эмульсий
- •Эмульгаторы
- •Механизм стабилизации:
3.3. Седиментационно-диффузионное равновесие. Седиментационная устойчивость
Процесс седиментации постепенно приводит дисперсную систему к упорядоченному состоянию, т.к. оседающие частицы располагаются в соответствии с их размерами. Через какое-то время все частицы могли бы осесть, но этому препятствует броуновское движение и диффузия, стремящиеся распределить все частицы равномерно по всему объему.
Между процессами диффузии и седиментации устанавливается седиментационно-диффузионное равновесие, которое характеризуется однородным распределением частиц по высоте столба. Под действием силы тяжести (или силы Архимеда) начнётся седиментация частиц. Седиментационный поток направлен ко дну сосуда, и он равен:
![]() ,
(3.14)
,
(3.14)
где U – скорость движения частиц, – плотность частиц фазы, 0 – плотность среды, r – радиус частицы, С – концентрация частиц в сосуде, g – ускорение свободного падения.
Седиментация
приведет к тому, что у дна сосуда
концентрация частиц фазы станет выше,
чем в верхней его части. В результате
возникнет градиент концентрации частиц
фазы по высоте h
сосуда:
![]() .
Появление градиента концентрации
приведёт к диффузии частиц, диффузионный
потокJd
направлен вверх и он равен:
.
Появление градиента концентрации
приведёт к диффузии частиц, диффузионный
потокJd
направлен вверх и он равен:
![]() (3.15
)
(3.15
)
Чем интенсивнее идет седиментация, тем больше становится градиент концентрации и тем значительней диффузионный поток. Наконец, при каком-то градиенте концентрации (распределении частиц фазы по высоте сосуда) скорости обоих потоков сравняются (в любом поперечном сечении сосуда число частиц, опускающихся вниз равно их числу, поднимающемуся вверх). Установившееся состояние системы носит название седиментационно-диффузионного равновесия.
С увеличением радиуса jсед увеличивается (т.к. пропорционаленr2), а диффузионный поток уменьшается (т.к. пропорционален 1/r), jсед >> jd, который можно не учитывать.
Если jd>>jсед(для ультрамикрогетерогенных систем), седиментацией можно пренебречь.
Если приравнять скорости потоков:
![]() =
=
![]() (3.16)
(3.16)
вместо Dподставить его выражение из (3.6), принять, что частицы имеют сферическую форму, и проинтегрировать полученное уравнение, то можно получить закон распределения частиц по высоте в равновесном состоянии, аналогичный известной барометрической формуле Лапласа(36)для газов в атмосфере:
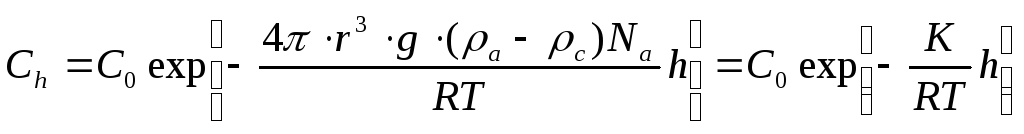 (3.17)
(3.17)
Здесь Сh – концентрация частиц фазы на высоте сосуда h, С0 – концентрация частиц у дна сосуда.
Если вместо концентрации дисперсной фазы С записать давление Р, то получим известную барометрическую формулу Лапласа(*), характеризующую распределение давление газа по высоте. Уравнение Лапласа называетсягипсометрическим законом (hypsos – высота).Для золей наблюдается более резкая зависимость концентрации по высоте, чем для молекул газа.
Рассмотрим результаты расчетов.
Высоту, на которой концентрация молекул или частиц уменьшается в 2 раза, обозначим через h1/2:
|
r
|
0,27 нм (газ) |
230 нм сусп. гуммигута |
М=40000а.е.м. Р-р макромолекул |
1,86 нм золь золота |
|
h1/2
|
5-5,5 км |
30 мкм |
20 м |
2,15 м |
Гипсометрический закон Лапласа был экспериментально подтвержден Перреном(*)(1910). Он изучал в вертикальном микроскопе распределение суспензии гуммигута сr=212 нм. Через каждые 30 мкм число частиц в поле зрения уменьшалось ровно в 2 раза.
По формуле Лапласа было рассчитано значение числа Авогадро NA= 6,82 1023 .
За эти опыты, доказывающие победу атомизма и отличавшиеся остроумием, точностью и простотой, Перрену в 1926 г. была присуждена Нобелевская премия.
Следует отметить, что седиментационо - диффузионное равновесие устанавливается очень медленно: время установления пропорционально 1/r2. В опытах Перрена постоянные значения Сh/С0 устанавливались лишь в течение недели.
