
- •Коллоидная химия
- •1.Коллоидные системы и предмет коллоидной химии
- •1.1. Коллоидные системы
- •1.2. Предмет коллоидной химии
- •Первый вариант количественной оценки - основной
- •Например, у частицы кубической формы с размером ребра
- •1.3. Классификация дисперсных систем
- •Классификация коллоидных систем по агрегатному состоянию фаз
- •2. Физическая химия поверхностных явлений
- •2.1. Межмолекулярные связи
- •Отличия молекулярных сил притяжения от химических:
- •Вклад различных видов энергии в общую энергию притяжения молекул
- •2.2.1. Определения поверхностного натяжения
- •1. Поверхностное натяжение численно равно работе обратимого изотермического образования единицы поверхности
- •2.2.3. Факторы, влияющие на величину поверхностного натяжения
- •1. Температура т
- •Поверхностное натяжение веществ на границе с воздухом
- •3) Природа контактирующих фаз
- •2.2.4. Экспериментальные методы определения поверхностного натяжения
- •2.3. Внутренняя (полная) удельная поверхностная энергия
- •Термодинамические характеристики поверхности некоторых жидкостей на границе их с воздухом
- •2.4. Адсорбция
- •2.4.1. Основные понятия и определения
- •2.4.2.1.Уравнение Ленгмюра(*)
- •Основные положения теории Ленгмюра:
- •Экспериментальное определение констант уравнения Ленгмюра
- •Правило Дюкло — Траубе:
- •Экспериментальное определение геометрических размеров молекулы пав
- •2.4.2.3. Изотермы адсорбции на неоднородной поверхности
- •А) теория Поляни(*)
- •Основные положения теории Поляни:
- •Основные положения теории бэт
- •Основные характеристики адсорбентов
- •Классификация адсорбентов:
- •2. По полярности
- •3. По размеру пор
- •2.4.5.2. Влияние кривизны поверхности на равновесие фаз
- •2.4.5.3. Капиллярные явления
- •2.4.5.4.Теория капиллярной конденсации
- •Условия действия капиллярных сил
- •2.4.5.5. Классификация изотерм адсорбции
- •2.4.6. Адсорбция из растворов на твердых адсорбентах
- •2.4.6.1. Молекулярная адсорбция
- •2.4.6.1.2. Основные закономерности адсорбции из растворов неэлектролитов на поверхности твердых адсорбентов)
- •2. Природа растворителя
- •3. Влияние природы адсорбента
- •4. Влияние природы адсорбтива
- •2.4.6.1.2. Основные закономерности адсорбции из растворов электролитов на поверхности твердых адсорбентов.
- •2.4.6.1.3. Ионно-обменная адсорбция
- •2.5. Смачивание. Адгезия. Когзия
- •2.5.1. Адгезия. Когзия
- •Механизм процесса адгезии
- •Несколько механизмов и теорий адгезии
- •2.5.2. Краевой угол смачивания и работа адгезии
- •2.5.3. Избирательное смачивание
- •2.5.4. Инверсия смачиваемости поверхности
- •2.5.5. Количественные характеристики процесса смачивания поверхности.
- •Qсм и b порошкообразных веществ
- •2.5.6. Измерение краевого угла смачивания
- •Использование пав для изменения смачиваемости поверхности
- •Избирательное смачивание
- •3. Молекулярно-кинетические свойства дисперсных систем
- •3.2. Диффузия в коллоидных системах
- •3.3. Седиментация суспензий
- •3.3. Седиментационно-диффузионное равновесие. Седиментационная устойчивость
- •Седиментационная устойчивость
- •4. Модель реального тела. Модель Бингама(*) – вязкопластическое тело
- •Лекция 9. .4.3. Реологические свойства реальных тел
- •Классификация тел по их реологическим свойствам
- •Вязкость агрегативно устойчивых дисперсных систем
- •4.3.2.Реологические свойства структурированных жидкообразных систем
- •Электрические свойства коллоидных растворов (золей)
- •5.1. Электрокинетические явления
- •5.2. Механизм образования дэс
- •4. Поляризация поверхности за счёт внешнего электрического поля.
- •5.3. Строение дэс
- •5.4. Факторы, влияющие на величину ζ-потенциала:
- •5.5.3. Влияние температуры на электрокинетический потенциал
- •5.5.4. Влияние рН среды
- •5.5.5. Экспериментальное определение - потенциала
- •6.Коагуляция и устойчивость дисперсных систем
- •6.1. Устойчивость дисперсных систем
- •6.2. Факторы агрегативной устойчивости
- •6.3. Ионный фактор стабилизации дисперсных систем Теория устойчивости лиофобных золей длфо
- •6.4. Коагуляция лиофобных дисперсных систем
- •6.4.1. Основные закономерности электролитной коагуляции
- •6.4.2. Кинетика электролитной коагуляции
- •6.4.3. Частные случаи электролитной коагуляции
- •6.4.4. Коллоидная защита
- •7. Лиофильные дисперсные системы. Коллоидные поверхностно-активные вещества
- •Классификация и общая характеристика пав
- •Коллоидные пав
- •2. Гидрофильно-липофильный баланс
- •Групповые числа атомных группировок
- •Применение пав
- •3. Строение мицелл пав. Солюбилизация
- •Факторы, влияющие на ккм
- •1) В растворах ипав ↑ Сэл-та ↓ ккм.
- •2) Добавление органических веществ в водные растворы пав по-разному влияет на ккм:
- •3). Влияние температуры т.
- •Значение мицеллярных растворов
- •Лиофобные дисперсные системы. Эмульсии
- •Классификация
- •Устойчивость и стабилизация эмульсий
- •Эмульгаторы
- •Механизм стабилизации:
Правило Дюкло — Траубе:
Это правило работает в растворах гомологических рядов ПАВ и формулируется следующим образом:
С увеличением длины углеводородного радикала на одну группу СН2, поверхностная активность растет в гомологическом ряду в 3 — 3,5 раза.
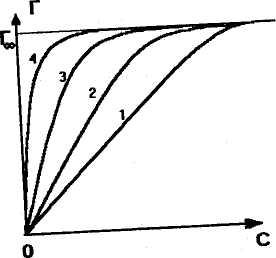
Проиллюстрируем это правило графически:
σ

а б
Обратим внимание на то, что значение Г∞ для одного гомологического ряда остаетсяпостоянным. Это объясняется тем, что емкость монослоя в этом случае зависит только от площади, которую занимает молекула ПАВ в этом слое. В рядах карбоновых кислот, спиртов эта площадь определяется величиной полярной группы, одинаковой для всего ряда ПАВ.
Это правило соблюдается для истинно растворимых ПАВ. Т.к. поверхностная активность определяется для бесконечно разбавленных систем, то легко объяснить ее зависимость от длины углеводородного радикала. Чем длиннее радикал, тем сильнее выталкивается молекула ПАВ из водного раствора, т.к. встраивание радикала в воду увеличивает ΔG, и процесс выхода молекул на поверхность энергетически очень выгоден.
Уравнение Шишковского(*)
Для случая адсорбции молекул ПАВ на границе раздела фаз можно использовать оба предложенных уравнения адсорбции на однородной поверхности. Приравняем их друг другу:
![]() =
=![]() (2.56)
(2.56)
Разделим переменные и проинтегрируем эти уравнения:
![]()
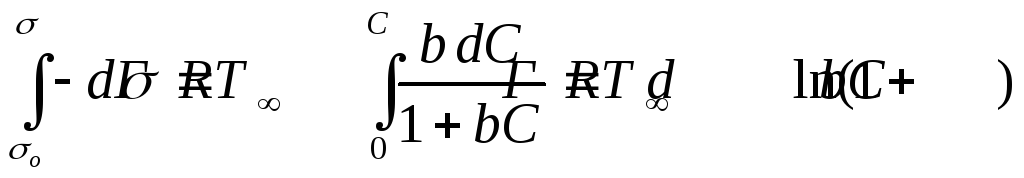 ,
(2.57)
,
(2.57)
отсюда
![]()
![]() , (2.58)
, (2.58)
Так
как в растворах ПАВ вследствие их высокой
поверхностной активности значения
абсолютной адсорбции Апрактически
равны избыточной адсорбцииГ, поэтому
выведенное уравнение может быть записано
и в виде:![]() . (2.59)
. (2.59)
Полученное уравнение носит название уравнения Шишковского. Первоначально оно было выведено им эмпирически для описания зависимости поверхностного натяжения от концентрации ПАВ:
![]() ,
(2.60)
,
(2.60)
В уравнение (2.60) входят коэффициенты В и А, физический смысл которых виден из выше выведенного уравнения (2.59).
Связь между поверхностным натяжением и адсорбцией можно проследить в уравнении Фрумкина(*):
![]() , (2.61)
, (2.61)
из которого следует, что при одинаковой адсорбции все гомологи уменьшают поверхностное натяжение на одну и ту же величину ∆σ.
Различие поверхностной активности в гомологическом ряду ПАВ обусловлено различной особенностью их к адсорбции, т.е. одно и то же значение Г достигается для короткоцепочечных ПАВ при значительно больших С, чем для длинноцепочечных ПАВ. Но если концентрации у гомологов таковы, что их адсорбции одинаковы, то они понижают σ на одну и ту же величину.
Экспериментальное определение геометрических размеров молекулы пав
Покажем, что, зная значение емкости монослоя, можно рассчитать So— площадь, занимаемую полярной группы иδ— длину углеводородного радикала молекулы ПАВ. Рассчитанные данные можно сравнить с независимо определенными другими методами.








![]() ,
,
Площадь,
занимаемая полярной группой
![]() (2.62)
(2.62)
Объем, занимаемый одной молекулой V1 = δ So (2.63)
Молярную массу монослоя можно определить по формуле:
М=ρ δ So Na, (2.64)
где ρ — плотность ПАВ, Na— число Авогадро(*). А так как
So *Na =1/Г∞, то длина углеводородного радикала может быть определена исходя из уравнения:
![]() . (2.65)
. (2.65)
Многочисленные экспериментальные проверки полученного уравнения показали хорошее согласие значений δ, вычисленных по приведенному уравнению и измеренных другими методами.
Лекция 5
