- •Гоу впо «московский государственный медико-стоматологический университет федерального агенства по здравоохранению и социальному развитию»
- •Тема 3. Барьерные функции организма и их нарушения 18
- •Тема 4. Патофизиология острого повреждения клетки
- •Тема 5. Острое воспаление ........25
- •Тема 6. Нарушение течения раневого процесса .......31
- •Тема 11. Гипоксия 50
- •Часть II. Частная патофизиология 53
- •Тема 12. Патофизиология системы крови 53
- •Тема 13. Патофизиология свертывающей системы крови gj
- •Тема 14. Патофизиология внешнего и тканевого дыхания 68
- •Тема 15. Недостаточность сердца и нарушение электрогенеза миокарда 73
- •Тема 16. Патофизиология желудочно-кишечного тракта 85
- •Тема 17. Патофизиология печени 8?
- •Часть I. Общая патофизиология
- •Тема 1. Моделирование болезней и патологических процессов
- •Тема 2. Патологическая физиология периферического кровообращения
- •Занятие 1. Артериальная и венозная гиперемия
- •Тема 3. Барьерные функции организма и их нарушения
- •Внутренние (гистогематические) барьеры (ггб)
- •Тема 4. Патофизиология острого повреждения клетки
- •Тема 5. Острое воспаление
- •Особенности воспалительных процессов в челюстно-лицевой области
- •Воспаление пульпы зуба (пульпит)
- •Занятие 1. Сосудистые изменения при воспалении
- •Занятие 2. Нарушение обмена веществ и механизмы защиты при воспалении
- •Тема 6. Нарушение течения раневого процесса
- •Занятие. Нарушение заживления кожной раны
- •Тема 7. Аллергия
- •Занятие 1. Патогенез аллергии немедленного типа
- •Тема 8. Патофизиология злокачественного роста
- •Тема 9. Лихорадка
- •Тема 10. Патофизиология водного обмена. Отек
- •Занятие. Патогенез отеков
- •Тема 11. Гипоксия
- •Занятие. Патогенез гипоксической гипоксии
- •Часть II. Частная патофизиология
- •Тема 12. Патофизиология системы
- •Класс морфологически дифференцированных клеток гранулопоэза
- •Плазматические клетки
- •Периферическая кровь при гиперхромных анемиях
- •Костный мозг при гиперхромных анемиях
- •Содержание гемоглобина (в процентах по Сали) / удвоенные две цифры числа эритроцитов
- •Тема 13. Патофизиология свертывающей системы крови
- •Воспроизведение механической желтухи
- •Опыт I. Определение времени рекальцификации плазмы
- •Тема 14. Патофизиология внешнего и тканевого дыхания
- •Тема 15. Недостаточность сердца и нарушение электрогенеза
- •Миокарда
- •Занятие 1. Экспериментальная недостаточность сердца
- •Занятие 3. Патология сердечного ритма
- •Изучение типических электрокардиограмм
- •Нарушение автоматизма
- •Нарушение возбудимости
- •Нарушение проводимости
- •Мерцание и трепетание предсердий
- •Желудочковым комплексом)
- •Тема 16. Патофизиология желудочно-кишечного тракта
- •Занятие. Патогенез острого гастрита
- •Занятие 2. Патогенез острого энтерита
- •Тема 17. Патофизиология печени
- •Занятие. Нарушения функции печени при экспериментальном гепатите. Патогенное действие желчи
- •Тема 18. Патофизиология почек
- •Тема 19.Патофизиология нервной системы
- •Тема 20. Патофизиология зубочелюстной системы. Патология пародонта
- •Занятие. Экспериментальный пародонтоз
- •Тема 21. Клеточные механизмы антимикробной защиты полости рта
- •Тема 22.Патофизиология эндокринной
Перепонку
отмывают водой и после восстановления
кровотока наносят на нее 5% раствор НО.
Через 20-30 сек. кислоту смывают водой и
вновь действуют на перепонку адреналином.
Отмечают отсутствие эффекта адреналина
на сосуды в зоне воспаления. Анализируют
результаты, делают выводы.
Опыт
4. Паралич сосудодвигателыгых нервов
воспаленной ткани. Демонстрация.
У
кролика (лучше белой масти) с обеих
сторон на шее отпрепаровывают
сосудисто-нервные пучки, симпатические
нервы берут на лигатуры и перерезают.
Возникает артериальная нейро-паралитическая
гиперемия обоих ушей. Затем одно ухо
опускают в
стакан
с горячей водой (60-70"С), развивается
острое воспаление. Отмечают, что
воспалительная гиперемия отличается
от артериальной нейропаралитической
гиперемии - при воспалительной
гиперемии
резче выражено расширение сосудов и
рисунок их смазан вследствие расширения
капиллярной сети.
Поочередно
раздражают индукционным током (или
пощипывая пинцетом) периферические
концы перерезанных симпатических
нервов с той и другой стороны, наблюдая
за изменением окраски ушей. Раздражение
симпатического нерва со стороны
неповрежденного уха вызывает сужение
сосудов и побледнение уха. Раздражение
симпатического нерва со стороны
воспаленного уха не приводит к
изменению просвета сосудов, поскольку
при воспалении происходит выключение
вазоконстрикторов.
Затем
кролику внутривенно вводят 0,2 мл 0,1%
раствора адреналина. Контрольное ухо
становится бледным из-за спазма
сосудов (сосудосуживающий эффект
адреналина). Воспаленное ухо остается
по-прежнему красным, так как в
очаге
воспаления снижается чувствительность
сосудов к адреналину.
Опыт
1.
Определение
рН гнойного и ихорозного экссудата
электрометрическим методом с помощью
лабораторного рН-метра
Принцип
электрометрического метода определения
рН и регистрации электродвижущей силы
основан на измерении силы, зависящей
от активности ионов водорода в испытуемом
растворе. При погружении электрода
рН-метра в исследуемую жидкость между
поверхностью электрода и раствором
происходит ионный обмен и возникает
разность потенциалов, которая
регистрируется по шкале прибора,
градуированного в единицах рН.
Занятие 2. Нарушение обмена веществ и механизмы защиты при воспалении


Правила
работы на рН — метре изложены в
специальной инструкции.
Подготовив
прибор к работе, определяют рН исследуемых
жидкостей - фильтратов гнойного и
ихорозного экссудата, а также сыворотки
крови. После каждого определения
необходимо тщательно промывать электроды
в дистиллированной воде. После окончания
работы электроды отмывают и выключают
рН-метр.
Анализируют
полученные результаты, делают выводы.
Опыт
2. Определение протеолитической
активности гнойного экссудата
В
8 пронумерованных пробирок наливают
по 1 мл 0,1% раствора яичного альбумина.
В первые 7 пробирок прибавляют
свежеприготовленный фильтрат гнойного
экссудата в возрастающем количестве:
в первую пробирку - одну каплю, в каждую
последующую на две капли больше.
Физиологическим раствором выравнивают
объемы во всех пробирках. В восьмую
(контрольную) пробирку наливают
только 13 капель физиологического
раствора (см. схему).
Схема
определения протеолитической
активности
гнойного
экссудата
компонент
№
пробирки
1
2
3
4
5
6
7
Ц 0,1%
р-р яичного альбумина
I
I
I
I
I
1
I
1 фильтрат
гнойного экссудата
1
3
5
7
9
11
13
_ физиологический
раствор
12
10 оо
6
4
2
-
13
Содержимое
пробирок встряхивают и ставят в термостат
(37°С) на 30 минут. Затем во все пробирки
прибавляют по одной-две капли 20% раствора
сульфосалициловой кислоты (реактив на
белок).
По
степени выпадения осадка судят о
переваривающей способности гнойного
экссудата. В контрольной пробирке № 8
отмечается осаждение альбумина (раствор
мутный). В пробирках, где произошло
полное расщепление альбумина, осадка
нет (раствор прозрачный). Определяют
протеолитическую активность гнойного
экссудата, выраженную в количестве
капель гноя, необходимого для полного
расщепления 1 мл 0,1 % альбумина в течение
30 минут при 37°С. Анализируют результаты,
делают выводы.
Опыт
3.
Макрофагоцитоз.
Фагоцитоз птичьих эритроцитов в брюшной
полости морской свинки
За
24-48 часов до опыта в брюшную полость
морской свинки вводят 15 мл стерильного
мясо-пептонного бульона, который
вызывает асептическое воспаление
брюшины. Развивается характерное
для серозных оболочек экссудативное
воспаление и в
брюшной
полости накапливается экссудат,
содержащий большое количество подвижных
фагоцитов (макрофагов). Свинку привязывают
брюшком кверху и вводят в брюшную
полость 5 мл 2% взвеси птичьих эритроцитов
в физиологическом растворе, подогретом
до 37-38°С. Через 15-20 мин делают пункцию
брюшной полости и пастеровской пипеткой
набирают перитонеальную жидкость,
состоящую из смеси экссудата и взвеси
птичьих эритроцитов. Каплю этой жидкости
помещают на предметное стекло, делают
мазок, высушивают его на воздухе и
фиксируют в 50% смеси спирта и эфира в
течение трех минут. После фиксации
мазок подсушивают на воздухе и красят
по Романовскому (азур-эозин) в течение
20-25 минут. Препарат тщательно промывают
проточной водой и просушивают
фильтровальной бумагой. Подготовленный
мазок рассматривают под микроскопом
с иммерсионной системой (ок. X 90). В
препарате обнаруживают значительное
количество фагоцитов - макрофагов
(в случае развития гнойного воспаления
- нейтрофилов) и птичьих эритроцитов,
которые хорошо видны благодаря наличию
в них ядра. В препарате находят все
стадии фагоцитоза, начиная с аттракции
и частичного поглощения эритроцита
фагоцитом и кончая обнаружением в
фагоците остатков ядра, что указывает
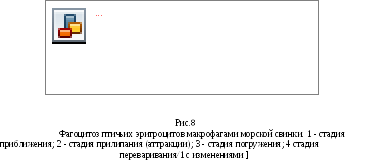
на завершение фагоцитоза. (Рис.8).
Подсчитывают
фагоцитарное число. Для этого находят
в мазке 100 макрофагов и сосчитывают
число
поглощенных ими эритроцитов. Полученное
количество эритроцитов, разделенное
на число
1 2 3 4
подсчитанных
фагоцитов (100)
и
составляют фагоцитарное число. При
подсчете фагоцитарного
числа
следует сосчитать все фагоциты,
попадающие в поле зрения.
Результаты
опыта записывают. Зарисовывают стадии
фагоцитоза. Обсуждают и делают выводы.
Опыт
4. Барьерная функция воспалительного
очага
Фагоцитоз,
нарушения микроциркуляции, повышение
проницаемости стенок сосудов и
сорбционных свойств поврежденных
тканей формируют барьерные функции
воспалительного очага, в котором
скапливаются и обезвреживаются
циркулирующие в крови различные
токсические вещества, микробы,
продукты их жизнедеятельности.
Для
демонстрации этого эффекта за несколько
дней до опыта крысе вводят под кожу
бедра 0,5-1
мл
стерильной 50%
эмульсии
скипидара в вазелиновом или растительном
масле, в результате чего в месте
введения развивается острое гнойное
асептическое воспаление. Вторая крыса
служит контролем. За 24-48
часов
до занятия обеим крысам внутривенно
вводят 2-3
мл
1%
раствора
коллоидной краски - три Пановой
сини
на физиологическом растворе. На занятии
наблюдают, что у опытной крысы свободные
от шерсти участки тела почти не окрашены,
т. е, вся краска скопилась в зоне
воспаления в результате повышения
проницаемости биологических мембран
в очаге воспаления, венозного
застоя, лимфостаза и фагоцитоза.
Свободные от шерсти участки тела
контрольной крысы равномерно окрашены
в синий цвет. Обсуждают результаты,
делают выводы.
Занятие
3.
СИСТЕМНЫЕ
ИЗМЕНЕНИЯ В ОРГАНИЗМЕ ПРИ ВОСПАЛЕНИИ
Опыт
1. Изменения в периферической крови при
развитии острого воспалительного
процесса у кролика
Для
опыта берут двух кроликов: одному из
них за три-пять дней до занятия вводят
под кожу бедра 3
мл
стерильной 50%
эмульсии
скипидара в растительном масле, в
результате чего развивается гнойное
асептическое воспаление. Второй кролик
используется в качестве контроля. У
обоих
кроликов измеряют ректальную температуру
и берут кровь из краевой вены уха для
определения количества лейкоцитов
и СОЭ.
Методика
подсчета лейкоцитов. В смеситель для
лейкоцитов набирают кровь до метки
0,5; кончик смесителя вытирают ваткой и
заполняют его 2%
раствором
подкрашенной уксусной кислоты до метки
«II» (уксусная кислота разрушает
эритроциты). Смеситель встряхивают в
течение 1-2
мин.
Первую каплю из смесителя сбрасывают,
а следующую небольшую каплю вносят в
предварительно подготовленную камеру
Горяева.